Рсв 2019 нулевая: Нулевой рсв-1 за 9 месяцев 2019
Заполняйте РСВ за I квартал 2019 года с помощью удобных инструментов в Экстерне
Импортируйте данные всех сотрудников в раздел 3 за один клик
— Загрузка данных из СЗВ-М
В форме РСВ по каждому работнику заполняется раздел 3, где необходимо указать все его реквизиты: ФИО, ИНН, СНИЛС, дату рождения и пол, а также код страны гражданства и код вида документа, удостоверяющего личность. Количество застрахованных лиц в разделе 1 зависит от количества разделов 3 с признаком «застрахован» в строках 160-180.
В Экстерне появилась возможность не только обновить уже имеющиеся в системе личные данные сотрудников, но и быстро добавить новых сотрудников за весь отчетный период с помощью загрузки файлов СЗВ-М.
Теперь при загрузке сведений по сотрудникам из СЗВ-М будут создаваться анкеты новых сотрудников с указанием их персональных данных — ФИО, СНИЛС, ИНН, если таких сотрудников нет в разделе 3. В то время как раньше только обновлялись существующие данные.
Новая возможность особенно актуальна для организаций с высокой текучкой кадров или которые выполняют сезонные работы. Загружать данные новых сотрудников удобно именно на основе СЗВ-М, потому что этот отчет ежемесячный и в нем, как правило, содержатся самые актуальные сведения по сотрудникам.
— Импорт из 2-НДФЛ 5.06
Кроме того, теперь в Экстерне вы можете импортировать в РСВ данные сотрудников из файла 2-НДФЛ формата 5.06, ранее импорт был только из файлов формата 5.04 и 5.05.
Экстерн напомнит об изменениях в порядке заполнения РСВ за I квартал 2019 г.
C 1 января 2019 года отменены пониженные тарифы страховых взносов для ряда плательщиков на упрощенной системе налогообложения и упразднены результаты аттестации рабочих мест. ФНС рекомендует:
- в приложении 1 вместо упраздненных кодов указывать код тарифа плательщика «01»;
- в подразделе 3.
 2.1 раздела 3 указывать соответствующий код категории застрахованного лица «НР», «ВЖНР», «ВПНР»;
2.1 раздела 3 указывать соответствующий код категории застрахованного лица «НР», «ВЖНР», «ВПНР»; - не применять коды тарифа 08, 09, 12, которые указывались в расчетах в 2017–2018 гг.;
- при заполнении подраздела 1.3.2 приложения 1 к разделу 1 расчета по страховым взносам в поле «002» не применять коды основания для заполнения 2 и 3.
Также с 2019 года не заполняются приложение 6 и приложение 8. Подробнее см. Письмо ФНС РФ от 26.12.2018 № БС-4-11/25633@.
В связи с этими изменениями в Экстерне были исключены указанные тарифы и коды из справочников. Теперь, если в справочнике указать несуществующий тариф или код, Экстерн покажет подсказку с объяснением, почему это ошибка:
При входе в приложения, которые не надо заполнять, вы увидите пояснение:
Если загрузить файл с этими приложениями, то появится ошибка:
Легко заполняйте нулевой РСВ
НК РФ не освобождает от обязанности сдавать РСВ, если организация или ИП не ведут финансово-хозяйственную деятельность (Письмо ФНС от 03. 04.2017 № БС-4-11/6174). Представляя расчеты с нулевыми показателями, плательщики тем самым заявляют об отсутствии в конкретном периоде выплат и сумм страховых взносов, подлежащих уплате. Это позволяет налоговым органам отделить плательщиков, не производящих выплат физлицам и не осуществляющих финансово-хозяйственную деятельность, от плательщиков, которые нарушают установленный НК РФ срок представления расчета.
04.2017 № БС-4-11/6174). Представляя расчеты с нулевыми показателями, плательщики тем самым заявляют об отсутствии в конкретном периоде выплат и сумм страховых взносов, подлежащих уплате. Это позволяет налоговым органам отделить плательщиков, не производящих выплат физлицам и не осуществляющих финансово-хозяйственную деятельность, от плательщиков, которые нарушают установленный НК РФ срок представления расчета.
Поэтому, если в отчетном периоде вы не делали отчислений за сотрудников, в Экстерне вы можете подготовить нулевой расчет по страховым взносам. Для этого в редакторе формы в левом нижнем углу перейдите в «… Еще действия» и выберите кнопку «Подготовить нулевой отчет»:
Нажав на кнопку, вы увидите лайтбокс подтверждения. Если подтвердить действие, Экстерн меняет данные в полях, которые должны быть заполнены нулями, на нули. Другие поля остаются без изменения.
Если численность работников у организации (ИП), сдающей нулевой расчет, меньше 25 человек, ей разрешается сдать отчет на бумаге (п. 10 ст. 431 НК РФ). Подготовив РСВ в Экстерне, вы можете распечатать заполненную форму с двумерным штрихкодом, чтобы ФНС могла считать все данные.
10 ст. 431 НК РФ). Подготовив РСВ в Экстерне, вы можете распечатать заполненную форму с двумерным штрихкодом, чтобы ФНС могла считать все данные.
Удобная работа с фильтрами и массовые операции по сотрудникам
Теперь в Экстерне вы можете отфильтровать сотрудников сразу по нескольким признакам, а также выбрать, по каким сотрудникам искать: по всем сотрудникам или по выбранным галочкой «Выбраны в отчет».
Также появились новые значения фильтра:
- корректируемые — сотрудники, у которых номер корректировки >0;
- с выплатами и начислениями — сотрудники, у которых есть ненулевые суммы хотя бы в одном из столбцов 210, 220, 230 или 240.
Галочка массового выбора теперь работает по найденным (уже отфильтрованным) сотрудникам. То есть вы можете отфильтровать нужных сотрудников, а затем массово выбрать их галочкой и выполнить массовое действие: проставить номера корректировки, перевести поля в режим авторасчета сумм, поменять код категории, удалить выплаты и взносы.
Примеры массовых действий по выбранными сотрудникам:
- Если вы загружаете данные из другого отчетного ПО, Экстерн проверит их и покажет, где есть ошибки. Чтобы исправить их, выберите галочками в фильтре сотрудников с ошибками, с предупреждениями и с выплатами по дополнительным тарифам, затем сформируйте файл Excel и сверьте суммы и коды тарифов. В зависимости от причины ошибки в Экстерне можно будет массово выполнить следующие действия по отфильтрованным сотрудникам: «Заменить код дополнительного тарифа», «Перевести все поля в режим авторасчета сумм».
- Если вам надо проставить номера корректировки у корректируемых сотрудников, отфильтруйте корректируемых сотрудников галочкой массового выбора или отметив галочкой нужных сотрудников самостоятельно, после этого выполните массовое действие «Указать номер корректировки».
- Чтобы избежать ошибок в расчете, необходимо тщательно проверять СНИЛС, ФИО и суммы по сотрудникам. Для удобства в Экстерне можно отфильтровать сотрудников с одинаковыми СНИЛС.
 Если в выборку попали сотрудники с одинаковыми СНИЛС, ошибочно внесенные в список, или была допущена ошибка при заполнении, то пользователь может сразу исправить ошибку. Более подробно про подачу корректировок читайте в справке.
Если в выборку попали сотрудники с одинаковыми СНИЛС, ошибочно внесенные в список, или была допущена ошибка при заполнении, то пользователь может сразу исправить ошибку. Более подробно про подачу корректировок читайте в справке.
Как ТСЖ оставить РСВ при отсутствии выплат
ФНС разъяснила, нужно ли ТСЖ (ТСН) сдавать расчет по страховым взносам при отсутствии выплат физлицам в течение расчетного (отчетного) периода или в последние три его месяца.
В письме от 22.04.2021 № БС-3-11/3059@ ведомство напоминает, что плательщиками страховых взносов признаются, в частности организации, производящие выплаты и иные вознаграждения физлицам, в том числе товарищества собственников недвижимости (ТСН) и товарищества собственников жилья (ТСЖ).
При этом в целях начисления страховых взносов руководители организаций, являющиеся единственными участниками (учредителями), членами организаций, в том числе председатели ТСЖ и ТСН, признаются застрахованными лицами.
НК РФ не освобождает плательщиков страховых взносов от представления расчетов в случае неосуществления организацией финансово-хозяйственной деятельности.
В случае отсутствия в течение того или иного расчетного (отчетного) периода выплат в пользу физических лиц, подлежащих обязательному социальному страхованию, нужно представить в налоговый орган в установленный срок расчет с нулевыми показателями.
С отчетности за I квартал 2020 года расчет по страховым взносам представляется по форме, утвержденной приказом ФНС от 18.09.2019 № ММВ-7-11/470@ (с изменениями и дополнениями).
Если в последние три месяца расчетного (отчетного) периода работодатель фактически не осуществлял выплаты и иные вознаграждения в пользу физических лиц (в отношении всех работников), он вправе представить в составе расчета титульный лист, раздел 1 без приложений, раздел 3 «Персонифицированные сведения о застрахованных лицах».
В связи с этим в случае, если ТСЖ (ТСН) фактически не осуществлялись выплаты и иные вознаграждения в пользу физических лиц в последние три месяца расчетного (отчетного) периода, в составе расчета представляется заполненный в установленном порядке раздел 3 на председателя ТСЖ (ТСН).
Сдача нулевой бухгалтерской и налоговой отчетности в Москве заказать онлайн
Данная политика конфиденциальности разработана в соответствии с законодательством Российской Федерации.
Все лица, заполнившие сведения, составляющие персональные данные на данном сайте, а также разместившие иную информацию обозначенными действиями, подтверждают свое согласие на обработку персональных данных без передачи третьим лицам.
Под персональными данными понимается нижеуказанная информация: общая информация (имя, телефон, адрес электронной почты, ИНН).
Клиенты направляют свои персональные данные для возможности связи
с ними со стороны владельца сайта и для осуществления обмена
информацией в рамках предлагаемых услуг.
Клиент, принимая положения настоящего документа, выражает свою заинтересованность и полное согласие, что обработка его персональных данных может включать в себя следующие действия: сбор, систематизацию, накопление, хранение, уточнение (обновление, изменение), использование, уничтожение.
Клиент гарантирует: информация, им предоставленная, является полной, точной и достоверной; при предоставлении информации не нарушается действующее законодательство Российской Федерации, законные права и интересы третьих лиц; вся предоставленная информация заполнена в отношении себя лично.
Владелец сайта гарантирует неразглашение полученных персональных данных и их безопасность.
Нулевой РСВ на единственного учредителя
Письмо Министерства финансов РФ
№ 03-15-06/10549 от 13. 02.2019
02.2019
Департамент налоговой и таможенной политики рассмотрел обращение от 17.12.2018 по вопросам о признании организации – общества с ограниченной ответственностью плательщиком страховых взносов, в котором единственный участник общества является генеральным директором, не получающим выплаты и вознаграждения, а также о правомерности представления обществом отчетности по страховым взносам и сообщает следующее.
Согласно статье 11 Налогового кодекса Российской Федерации (далее – Кодекс) организации – это юридические лица, образованные в соответствии с законодательством Российской Федерации.
Исходя из положений подпункта 1 пункта 1 статьи 419 Кодекса плательщиками страховых взносов признаются лица, являющиеся страхователями в соответствии с федеральными законами о конкретных видах обязательного социального страхования, в частности организации.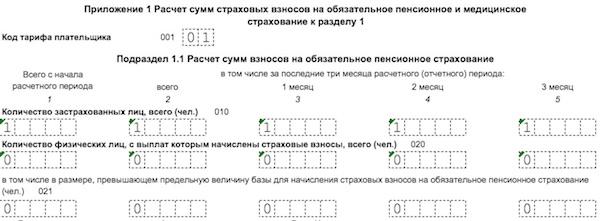
Пунктом 1 статьи 420 Кодекса определено, что объектом обложения страховыми взносами для плательщиков страховых взносов – организаций признаются выплаты и иные вознаграждения, начисляемые ими в пользу физических лиц, подлежащих обязательному социальному страхованию в соответствии с федеральными законами о конкретных видах обязательного социального страхования, в частности, в рамках трудовых отношений.
В соответствии с пунктом 1 статьи 7 Федерального закона от 15.12.2001 N 167-ФЗ «Об обязательном пенсионном страховании в Российской Федерации», пунктом 1 части 1 статьи 2 Федерального закона от 29.12.2006 N 255-ФЗ «Об обязательном социальном страховании на случай временной нетрудоспособности и в связи с материнством» и пунктом 1 статьи 10 Федерального закона от 29.11.2010 N 326-ФЗ «Об обязательном медицинском страховании в Российской Федерации» в числе лиц, работающих по трудовому договору, указаны руководители организаций, являющиеся единственными участниками (учредителями), членами организаций, собственниками их имущества, которые относятся к застрахованным лицам по упомянутым видам обязательного социального страхования.
Следовательно, руководитель организации, являющийся единственным участником, признается застрахованным лицом по обязательному социальному страхованию.
Также пунктом 7 статьи 431 Кодекса предусмотрена обязанность плательщиков страховых взносов – организаций, производящих выплаты и иные вознаграждения физическим лицам, представлять в установленном порядке не позднее 30-го числа месяца, следующего за расчетным (отчетным) периодом, в налоговый орган по месту учета расчет по страховым взносам (далее – Расчет).
В составе Расчета, наряду с данными о начисленных и уплаченных страховых взносах, содержатся персонифицированные сведения о застрахованных лицах в системе обязательного пенсионного страхования (персональные данные, указываемые в общей части индивидуального лицевого счета застрахованного лица), наличие которых необходимо при подтверждении пенсионных прав этих лиц для назначения им страховой пенсии.
Порядок заполнения Расчета утвержден приказом ФНС России от 10. 10.2016 N ММВ-7-11/511@.
10.2016 N ММВ-7-11/511@.
Вне зависимости от осуществляемой деятельности плательщики страховых взносов должны включить в состав Расчета в соответствии с порядком заполнения:
– титульный лист;
– раздел 1 «Сводные данные об обязательствах плательщика страховых взносов»;
– подраздел 1.1 «Расчет сумм страховых взносов на обязательное пенсионное страхование» и подраздел 1.2 «Расчет сумм страховых взносов на обязательное медицинское страхование» приложения 1 к разделу 1;
– приложение 2 «Расчет сумм страховых взносов на обязательное социальное страхование на случай временной нетрудоспособности и в связи с материнством» к разделу 1;
– раздел 3 «Персонифицированные сведения о застрахованных лицах».
Дополнительно сообщаем, что согласно пункту 2.20 порядка заполнения Расчета в случае отсутствия какого-либо показателя количественные и суммовые показатели заполняются значением «0» («ноль»), в остальных случаях во всех знакоместах соответствующего поля проставляется прочерк.
Пунктом 22.2 порядка заполнения Расчета определено, что в персонифицированных сведениях о застрахованных лицах, в которых отсутствуют данные о сумме выплат и иных вознаграждений, начисленных в пользу физического лица за последние три месяца отчетного (расчетного) периода, подраздел 3.2 раздела 3 Расчета не заполняется.
Обращаем внимание, что Кодексом не предусмотрено освобождение от исполнения обязанности плательщика страховых взносов – организации по представлению Расчетов в случае неосуществления финансово-хозяйственной деятельности и отсутствия выплат физическим лицам.
Представляя расчеты с нулевыми показателями, плательщик заявляет в налоговый орган об отсутствии в конкретном отчетном периоде выплат и вознаграждений в пользу физических лиц, являющихся объектом обложения страховыми взносами, и, соответственно, об отсутствии сумм страховых взносов, подлежащих уплате за этот же отчетный период.
Кроме того, представляемые Расчеты с нулевыми показателями позволяют налоговым органам отделить недобросовестных плательщиков, которые нарушают установленный Налоговым кодексом срок для представления Расчетов, от плательщиков, не производящих в конкретном отчетном периоде выплат и иных вознаграждений физическим лицам, и, следовательно, не применять к данным плательщикам способы обеспечения исполнения обязанностей по уплате страховых взносов, установленные статьей 76 Налогового кодекса (в частности, в виде приостановления операций плательщика по его счетам в банке и переводов его электронных денежных средств), а также не привлекать к ответственности, предусмотренной статьей 119 Налогового кодекса.
Заместитель директора Департамента Р.А.СААКЯН
Нулевая отчетность ООО | Сколько стоит сдать нулевую отчетность ООО в “Балиот”
По составу документов нулевая отчетность ООО, как бухгалтерская, так и налоговая, практически не отличается от комплекта, обязательного для действующих предприятий. Она сдается в те же сроки, в случае их пропуска организацию ожидают штрафные санкции.
Необходимость отчитаться «по нулям» возникает у вновь созданных компаний, которые не начали хозяйственную деятельность либо приостановили ее по определенным причинам. При продаже бизнеса период может оказаться длительным, и все это время подача нулевой отчетности ООО должна производиться в установленном порядке.
Состав бухгалтерской отчетности
Юридические лица по окончании года обязаны сдать бухгалтерскую (финансовую) отчетность, которая включает в себя баланс и отчет о финансовых результатах (о прибылях и убытках). Баланс не может быть «пустым». Как минимум, у компании на пассиве обозначается стоимость уставного капитала, которая указана в Уставе организации.
Баланс не может быть «пустым». Как минимум, у компании на пассиве обозначается стоимость уставного капитала, которая указана в Уставе организации.
Состав активов бывает разным. Если учредители не полностью внесли свои доли, указывается дебиторская задолженность. Оплата уставного капитала основными средствами, материалами, товаром отражается в соответствующей строке. Имеется особенность для обществ, зарегистрированных в последнем квартале года. Они могут подавать баланс за период со дня внесения в ЕГРЮЛ по 31 декабря следующего года включительно. Например, с 10.11.2018 по 31.12. 2019 года. Самое важное правило бухгалтерской (финансовой) отчетности: актив баланса равняется пассиву баланса, без данного равенства контролирующий орган не примет отчетность и наложат штрафные санкции.
Нулевая налоговая отчетность ООО
Содержание и количество отчетов определяет система налогообложения, которую использует общество с ограниченной ответственностью. На общем режиме их больше, на специальных — меньше. Предприятия, имеющие транспорт, земельные участки, недвижимость сдают декларацию по налогу на имущество, а также декларацию по транспортному налогу. При отсутствии таких объектов, обязанность не возникает. Если они подпадают под налоговые льготы, нужно обязательно подавать «нулевку».
Предприятия, имеющие транспорт, земельные участки, недвижимость сдают декларацию по налогу на имущество, а также декларацию по транспортному налогу. При отсутствии таких объектов, обязанность не возникает. Если они подпадают под налоговые льготы, нужно обязательно подавать «нулевку».
Организации на ОСНО
Компании на общем режиме должны подавать декларации по основной деятельности за год и за каждый квартал:
- по НДС — принимается только в электронном виде;
- по прибыли — заполняются титул, раздел 1 (1.1, 1.2), лист 02.
Если у компании не было движений на расчетном счете в течении отчетного периода, то сдается единая (упрощенная) налоговая декларация на бумажном носителе до 20 числа месяца следующего отчетного периода.
Прибыль будет равна нулю, когда операции отсутствуют в течение года. Если в одном из кварталов работа велась (возможно, с убытком), цифры будут переходить по отчету – налог формируется нарастающим итогом. Может иметь место переходящий остаток прошлых периодов. Таким образом, в «нулевке» не всегда стоят только нули и прочерки.
Таким образом, в «нулевке» не всегда стоят только нули и прочерки.
Организации на УСН и ЕНВД
Фирмы, работающие на «упрощенке», сдают декларацию в ИФНС один раз в год. Она заполняется по общей стандартной форме (Пр. ФНС № ММВ-7-3/352@, 04.07.2014) на основании данных по году.
Плательщик по ЕНВД обязан сняться с учета в течение 5 дней после прекращения деятельности. Если фактически она не осуществляется, но в собственности (аренде) находятся объекты, физические показатели которых использовались для расчета налога (помещение, транспорт), нужно отчитываться по установленным правилам.
Расчеты 2-НДФЛ и 6-НДФЛ
Обязанность представить расчеты по подоходному налогу возникает при наличии работников по трудовому договору, гражданско-правовому договору и т. д. и начислении зарплаты, дивидендов. В ином случае их подавать не надо (Письмо ФНС № БС-4-11/7928@, 04.05.2016). Если все работники уволены, сдача нулевой отчетности ООО, стоимость которой прямо зависит от количества заполняемых форм, обойдется заказчику дешевле.
Расчеты по страховым взносам
Формы РСВ-1 (в ИФНС), отчет 4-ФСС обязаны сдавать все юридические лица ежеквартально и по итогам года, даже если работа не осуществляется и выплаты по заработной плате не производятся. Такая ситуация является редкой, генеральный директор и главный бухгалтер обычно остаются в числе действующих работников. Они могут не получать зарплаты, но при этом форма СЗВ-М подается в Пенсионный фонд ежемесячно (период засчитывается в стаж), а также ежегодно сдавать СЗВ-стаж для подтверждения его.
Стоимость нулевой отчетности для ООО
Подготовка документов для ИФНС, ПФР и ФСС включающие составление пояснительных записок, писем, которые желательно прикладывать, чтобы избежать лишних уточнений и проверок. Срок их оформления определяется объемом работы и способом отправки.
Компания «БАЛИОТ» оказывает услуги по сопровождению бизнеса в Москве больше 12 лет, и на практике изучила все требования контролирующих органов. В приведенном прайсе указаны тарифы для организаций на общем и упрощенных режимах налогообложения.
Заполните форму обратной связи или позвоните в офис «БАЛИОТ» по телефону +7(495)127-7398, чтобы уточнить, сколько стоит сдать нулевую отчетность ООО для вашей конкретной ситуации, и получить ответы специалиста на все интересующие вопросы.
1С:БизнесСтарт онлайн-бухгалтерия для малого бизнеса.
Илья Кузнецов
Меня, как начинающего предпринимателя, все более чем устраивает. Бухгалтер был приятно удивлён такой возможности работы – что не надо устанавливать программу и можно работать с любого устройства и в любом месте, главное доступ в интернет. Спасибо вам большое
Альбина
Я бы рекомендовала компанию своим друзьям, если бы получала деньги на агитацию – шутка)) На самом деле, впервые работаю именно в облачной системе и мне все нравится, особенно что нет привязки к рабочему месту. Думаю за вашей системой Будущее! Желаю вашей команде процветания и успехов во всех начинаниях!!!
Синдяшкин Денис Владимирович,
ООО “Продос”, Красноярск
Программа идеальна! (хочу приз)))) А если серьезно, то будет здорово, если добавите информативности. 1СБизнесСтарт рассчитана на начинающих “бизнесменов и безнесвумен”, а у них не всегда такой же багаж знаний как у проф бухгалтеров и если добавить информативности – будет проще понимать, в чем именно допустил ошибку, и почему тот или иной отчет выдает не совсем желаемые результаты. Ну и некоторые пункты меню не являются интуитивно-понятными.
1СБизнесСтарт рассчитана на начинающих “бизнесменов и безнесвумен”, а у них не всегда такой же багаж знаний как у проф бухгалтеров и если добавить информативности – будет проще понимать, в чем именно допустил ошибку, и почему тот или иной отчет выдает не совсем желаемые результаты. Ну и некоторые пункты меню не являются интуитивно-понятными.
Кристина Нодь,
ИП Нодь Кристина Андреевна, Алтайский край
Пользуемся программой второй год. Довольны работой, по звонку оказывается профессиональная помощь. Хорошие акции и скидки по оплате. Пользовались, пользуемся и будем пользоваться))) Рекомендуем коллегам по сфере деятельности вашу платформу! Удачи и процветания! РА Креатика.
Николаева Ирина,
ИП, Гостевой дом «Солнечная гавань», г.Новороссийск
Для ИП здесь всё просто. Ведение учета занимает всего один день в месяц. На все вопросы отвечает служба поддержки.
На все вопросы отвечает служба поддержки.
Лазарев Алексей,
ООО “КОМВИД СП”
Хороший интерфейс для начинающих работать в 1С. Своего бухгалтера нет. До этого пользовался другой онлайн системой, но при сдаче годовой отчетности обнаружилось достаточно много недостатков. Стал искать срочную замену, выбрал эту – не жалею. Учет веду сам, почти во всем разбираюсь, но при сдаче отчетных периодов, все равно, советуюсь со знакомым бухгалтером.
Мелехина Оксана,
ООО «Профбух-консалтинг»
Отличная программа для ведения бухгалтерии ИП или небольшой компании. Простой и интуитивно понятный интерфейс. Нет ничего лишнего, разобраться сможет даже новичок. Но в тоже время, в программе присутствует весь необходимый функционал для ведения полноценного учета и сдачи отчетности. Также есть возможность ведения складского учета и учета заработной платы.
Борисов Максим Леонидович,
Услуги полиграфии, г.Ярославль
Все подошло для ИП на УСН, счет на оплату подготовил сам.
Сидоренков Игорь,
Председатель ТСН
Отчетность очень хорошо реализована, вопросов никаких нет. Взаимодействие отлично налажено, всё отправляется. При взносах в ПФР, ФСС и прочие фонды, в платежном поручении сразу подтягиваются расчетные счета, куда платить. Огромный плюс! У конкурентов такого нет.
Сигаев Д.,
Предприниматель
Никогда не думал, что стану работать в облачных сервисах. До недавнего времени относился к ним с недоверием. Однако доступность цены привлекла меня к этому продукту. Еще как плюс постоянно актуальные документы и тех поддержка. В целом продукт получился отличный!
Дина Абитова,
Сеть мебельных салонов ООО “Реноме”, г. Екатеринбург
Екатеринбург
Рекомендуем БизнесСтарт знакомым ИП, программа удобная.
Респираторно-синцитиальный вирус и исчезновение эпидемий гриппа в Корее в сезоне COVID-19 2020–2021 гг.
https://doi.org/10.1016/j.ijid.2021.07.005Получить права и контент НПИ воздействуют не только на COVID-19, но и на ряд других инфекционных заболеванийМы исследовали, являются ли РСВ и БИФ эпидемиями зимой 2020-21 гг. в Корее.
При анализе, основанном на эпиднадзоре, зимних эпидемий RSV и IFV не наблюдалось.
Позитивность IFV была почти нулевой, но были отдельные случаи RSV.
В данных эпиднадзора из 13 других стран эпидемии инфекционного вируса гриппа не наблюдались.
Резюме
Цели
Мы исследовали, снижают ли немедикаментозные вмешательства (НФВ) распространенность зимних респираторных вирусных инфекций, представленных респираторно-синцитиальным вирусом (РСВ) и вирусом гриппа (ИФВ), зимой в Корее.
Методы
Использовалась база данных системы мониторинга корейского гриппа и респираторных вирусов. С января 2016 г. по январь 2021 г. собирались еженедельные положительные результаты респираторных вирусов и еженедельное количество госпитализаций с острыми респираторными инфекциями. Период NPI был определен как период с февраля 2020 г. по январь 2021 г. Мы проанализировали, изменились ли госпитализация и положительный результат образцов на респираторные вирусы после NPI. Были использованы байесовские модели структурных временных рядов и анализ Пуассона.Также были изучены данные из других стран/регионов, сообщающих о положительных показателях RSV и IFV.
Результаты
По сравнению с периодом до NPI положительные показатели RSV и IFV значительно снизились до 19% и 6%, а также 23% и 6% от прогнозируемого значения. Также значительно снизилась госпитализация до 9% и 8%, а также 10% и 5% от прогнозируемого значения. Положительные показатели IFV в 14 странах в период NPI были почти нулевыми, тогда как спорадические вспышки RSV имели место в некоторых странах.
Выводы
В сезоне 2020–2021 гг. в Корее не наблюдалось зимних эпидемий РСВ и БИФ.
Ключевые слова
Респираторно-синцитиальный вирус
Грипп
немедикаментозное вмешательство
COVID-19
Южная Корея
Рекомендуемые статьиСсылки на статьи (0)
Опубликовано Elsevier Ltd от имени Международного общества инфекционных заболеваний.
Рекомендованные статьи
Ссылки на статьи
Вспышка РСВ-инфекции в неонатологической клинике в сезон РСВ-сезона | BMC Pediatrics
Здесь мы описываем первую вспышку внутрибольничной эпидемии РСВ в неонатологической клинике с момента введения в Болгарии рутинной диагностики РСВ с помощью ПЦР (2013/2014).В годы, предшествовавшие этой вспышке, в отделениях интенсивной терапии новорожденных наблюдались лишь единичные случаи инфицирования РСВ в течение сезонов РСВ.
РСВ является наиболее частым вирусным возбудителем инфекций ИДНД у детей в возрасте до 5 лет. По данным разных авторов, РСВ вызывает 50–90% госпитализаций по поводу бронхиолита, 5–40% госпитализаций по поводу пневмонии и 10–30% госпитализаций по поводу трахеобронхита [19,20,21]. В Болгарии за сезоны 2015/16, 2016/17 и 2017/18 РСВ выявлен у 44 человек.5% новорожденных с бронхиолитом и 25,1% с пневмонией [16]. В течение сезона 2014–2015 гг. доминировал серотип А, а в течение следующих трех сезонов доминировал РСВ-В [15, 16]. В наших образцах отделений интенсивной терапии, где было возможно типирование, был доказан RSV-B. В Болгарии наблюдается ярко выраженная сезонность РСВ-инфекций в течение декабря-марта с пиком заболеваний в феврале [15, 16], т. е. описанная здесь эпидемическая вспышка приходится на вторую половину сезона РСВ.
По данным разных авторов, РСВ вызывает 50–90% госпитализаций по поводу бронхиолита, 5–40% госпитализаций по поводу пневмонии и 10–30% госпитализаций по поводу трахеобронхита [19,20,21]. В Болгарии за сезоны 2015/16, 2016/17 и 2017/18 РСВ выявлен у 44 человек.5% новорожденных с бронхиолитом и 25,1% с пневмонией [16]. В течение сезона 2014–2015 гг. доминировал серотип А, а в течение следующих трех сезонов доминировал РСВ-В [15, 16]. В наших образцах отделений интенсивной терапии, где было возможно типирование, был доказан RSV-B. В Болгарии наблюдается ярко выраженная сезонность РСВ-инфекций в течение декабря-марта с пиком заболеваний в феврале [15, 16], т. е. описанная здесь эпидемическая вспышка приходится на вторую половину сезона РСВ.
У пораженных доношенных детей (группа 1) симптомы ИНДП проявляются через несколько дней после выписки из родильного дома.Таким образом, они должны были заразиться во время пребывания в больнице от RSV-позитивных посетителей или медицинского персонала с респираторными симптомами или без них.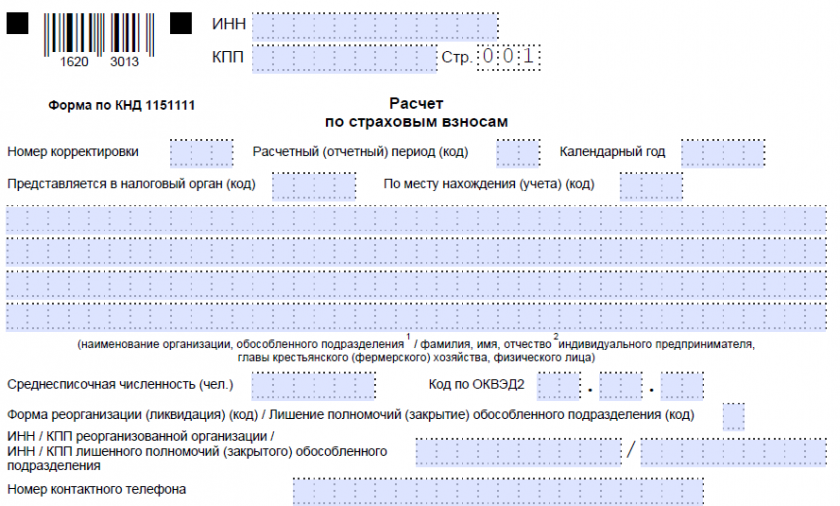 Хотя путь передачи РСВ способствует его распространению среди детей раннего возраста [9], следует обсудить роль медицинского персонала и пробелы в противоэпидемическом режиме. К сожалению, в описываемой здесь вспышке источник заражения (медицинский персонал или посетители) не был выявлен. Важно отметить, что не было ни одного случая РСВ-инфекции среди детей, находившихся на попечении в приюте.Вероятно, это связано с ограниченным контактом с медицинским персоналом, другими матерями или посетителями и демонстрирует преимущества системы совместного проживания в профилактике внутрибольничных инфекций дыхательных путей в неонатальных отделениях для здоровых детей. Кроме того, в таких палатах матери активно участвуют в уходе за своими младенцами.
Хотя путь передачи РСВ способствует его распространению среди детей раннего возраста [9], следует обсудить роль медицинского персонала и пробелы в противоэпидемическом режиме. К сожалению, в описываемой здесь вспышке источник заражения (медицинский персонал или посетители) не был выявлен. Важно отметить, что не было ни одного случая РСВ-инфекции среди детей, находившихся на попечении в приюте.Вероятно, это связано с ограниченным контактом с медицинским персоналом, другими матерями или посетителями и демонстрирует преимущества системы совместного проживания в профилактике внутрибольничных инфекций дыхательных путей в неонатальных отделениях для здоровых детей. Кроме того, в таких палатах матери активно участвуют в уходе за своими младенцами.
Недоношенные дети с пограничным расстройством личности или без него подвергаются повышенному риску тяжелого течения RSV-LRTI в течение первых 2 лет жизни. Паливизумаб, моноклональное антитело к F-белку РСВ, было разработано для иммунопрофилактики РСВ-заболевания. После получения лицензии в 1998 г. паливизумаб применяется во все большем числе стран с различными критериями возмещения расходов, которые меняются с годами [9, 11, 12, 22, 23]. Согласно рекомендациям Американской академии педиатрии (ААП) до 2014 г. иммунопрофилактику РСВ проводили недоношенным детям гестационного возраста (ГВ) < 35 ГВт [22, 24]. Проспективные клинические испытания продемонстрировали эффективность паливизумаба на уровне 45–82% в отношении госпитализаций, связанных с РСВ [9, 13, 14]. Из-за его высокой цены были проведены исследования «затраты-эффективность» для разных подгрупп новорожденных высокого риска, но они не дали единых рекомендаций по профилактике в зависимости от гестационного возраста [25, 26].Так, в последующие годы в США и некоторых странах ЕС критерии возмещения были ограничены наиболее уязвимыми группами: новорожденные, рожденные недоношенными на сроке ≤29 недель гестации, дети с БЛД или гемодинамически значимыми ИБС [23, 24, 27]. После внедрения РСВ-иммунопрофилактики в Болгарии в 2010 г.
После получения лицензии в 1998 г. паливизумаб применяется во все большем числе стран с различными критериями возмещения расходов, которые меняются с годами [9, 11, 12, 22, 23]. Согласно рекомендациям Американской академии педиатрии (ААП) до 2014 г. иммунопрофилактику РСВ проводили недоношенным детям гестационного возраста (ГВ) < 35 ГВт [22, 24]. Проспективные клинические испытания продемонстрировали эффективность паливизумаба на уровне 45–82% в отношении госпитализаций, связанных с РСВ [9, 13, 14]. Из-за его высокой цены были проведены исследования «затраты-эффективность» для разных подгрупп новорожденных высокого риска, но они не дали единых рекомендаций по профилактике в зависимости от гестационного возраста [25, 26].Так, в последующие годы в США и некоторых странах ЕС критерии возмещения были ограничены наиболее уязвимыми группами: новорожденные, рожденные недоношенными на сроке ≤29 недель гестации, дети с БЛД или гемодинамически значимыми ИБС [23, 24, 27]. После внедрения РСВ-иммунопрофилактики в Болгарии в 2010 г. , первоначально охватывающей только детей с тяжелой формой БЛД, критерии возмещения расходов постепенно были распространены на всех детей с ГВ < 30 GW в возрасте до 1 года; лица в возрасте до 2 лет, нуждающиеся в лечении по поводу ПРЛ в течение предшествующих 6 месяцев, или с гемодинамически значимым ИБС.Начиная с сезона 2019/2020 гг., расходы на паливизумаб также возмещаются для недоношенных детей с гестационным возрастом от 30 до < 32 GW и < 6 месяцев в начале сезона РСВ.
, первоначально охватывающей только детей с тяжелой формой БЛД, критерии возмещения расходов постепенно были распространены на всех детей с ГВ < 30 GW в возрасте до 1 года; лица в возрасте до 2 лет, нуждающиеся в лечении по поводу ПРЛ в течение предшествующих 6 месяцев, или с гемодинамически значимым ИБС.Начиная с сезона 2019/2020 гг., расходы на паливизумаб также возмещаются для недоношенных детей с гестационным возрастом от 30 до < 32 GW и < 6 месяцев в начале сезона РСВ.
У недоношенных детей, особенно с БЛД, РСВ-заболевание протекает значительно тяжелее, с поражением нижних дыхательных путей или пневмонией. Часто накладывается бактериальная инфекция [21, 27, 28, 29]. У наших двух наиболее тяжело пораженных младенцев тяжелая форма RSV осложнилась респираторно-ассоциированной инфекцией (P1 и P2).
Если РСВ-заболевание у таких новорожденных высокого риска возникает в отделении интенсивной терапии, выписка домой откладывается. В нашей популяции недоношенных детей этот период составлял от 1 недели для более легких случаев и более 2 месяцев для младенцев с тяжелым фоновым БЛД и критическим ухудшением состояния. На сегодняшний день нет единых рекомендаций по началу приема паливизумаба во время пребывания новорожденных из группы высокого риска в отделении интенсивной терапии [10]. Таким образом, крайне недоношенные пациенты отделения интенсивной терапии интенсивной терапии, родившиеся непосредственно перед или во время сезона РСВ в Болгарии (декабрь-март), как правило, не получают паливизумаб перед выпиской домой.Так как затраты на госпитализацию значительно возрастут, практика в нашем отделении интенсивной терапии состоит в том, чтобы вводить паливизумаб вне рекомендаций только крайне недоношенным детям с самым высоким риском тяжелой БЛД (потребность в ИВЛ и/или высокая потребность в кислороде в течение всего первого месяца жизни). Таким образом, профилактику РСВ у таких детей начинают примерно через месяц после рождения с ежемесячной дозы 15 мг/кг паливизумаба. Из наших 7 RSV-положительных пациентов отделения интенсивной терапии паливизумаб ранее назначался только для P1, крайне недоношенного ребенка с тяжелой формой БЛД.
На сегодняшний день нет единых рекомендаций по началу приема паливизумаба во время пребывания новорожденных из группы высокого риска в отделении интенсивной терапии [10]. Таким образом, крайне недоношенные пациенты отделения интенсивной терапии интенсивной терапии, родившиеся непосредственно перед или во время сезона РСВ в Болгарии (декабрь-март), как правило, не получают паливизумаб перед выпиской домой.Так как затраты на госпитализацию значительно возрастут, практика в нашем отделении интенсивной терапии состоит в том, чтобы вводить паливизумаб вне рекомендаций только крайне недоношенным детям с самым высоким риском тяжелой БЛД (потребность в ИВЛ и/или высокая потребность в кислороде в течение всего первого месяца жизни). Таким образом, профилактику РСВ у таких детей начинают примерно через месяц после рождения с ежемесячной дозы 15 мг/кг паливизумаба. Из наших 7 RSV-положительных пациентов отделения интенсивной терапии паливизумаб ранее назначался только для P1, крайне недоношенного ребенка с тяжелой формой БЛД. У остальных 6 пациентов потребность в кислороде отсутствовала или была снижена на 1-м месяце жизни. Таким образом, они получили свою первую инъекцию паливизумаба после выявления индексного случая.
У остальных 6 пациентов потребность в кислороде отсутствовала или была снижена на 1-м месяце жизни. Таким образом, они получили свою первую инъекцию паливизумаба после выявления индексного случая.
Среди наших пациентов отделения интенсивной терапии, РСВ-инфекция была наиболее критической у младенца с тяжелой формой БЛД, несмотря на продолжающуюся профилактику паливизумабом. Морфологическая незрелость легкого и изменения, связанные с БЛД, могли способствовать тяжелому течению заболевания. К счастью, несмотря на низкий гестационный возраст и сопутствующие заболевания, ни один из младенцев в нашей когорте RSV не умер.Следует отметить, что трое крайне недоношенных пациентов отделения интенсивной терапии с тяжелой формой БЛД уже получили одну или две инъекции паливизумаба до начала вспышки РСВ и не заразились. Таким образом, паливизумаб может предотвратить заболевание RSV или помочь таким младенцам выжить и уменьшить количество тяжелых случаев.
За последние два десятилетия в литературе было опубликовано несколько исследований вспышек РСВ в отделениях интенсивной терапии новорожденных/детских отделениях специального ухода с участием 7–15 недоношенных детей [30,31,32,33,34]. После выявления первого случая РСВ необходимо провести скрининг всех младенцев в ОИТН, изолировать симптоматических и инфицированных младенцев, а также провести строгие процедуры инфекционного контроля, чтобы остановить распространение. Диздар и др. В 2004 г. сообщалось о вспышке РСВ у 15 РСВ-положительных симптоматических недоношенных детей, 5 из них (~ 30%) умерли [30]. Во время вспышки, описанной Kilani RA (2002), у 8 новорожденных с очень низким гестационным возрастом была диагностирована RSV-заболевание, 4 из них нуждались в искусственной вентиляции легких, и один умер. В то же время 12 доношенных и поздненедоношенных детей оставались РСВ-негативными и бессимптомными, вероятно, за счет анти-РСВ IgG-антител, проникающих через плаценту в основном в последние месяцы беременности [35].В своем исследовании Halasa и соавт. обобщили значительные негативные последствия вспышки RSV в отделении интенсивной терапии интенсивной терапии для оказания медицинской помощи, больничных расходов и результатов лечения пациентов [36].
После выявления первого случая РСВ необходимо провести скрининг всех младенцев в ОИТН, изолировать симптоматических и инфицированных младенцев, а также провести строгие процедуры инфекционного контроля, чтобы остановить распространение. Диздар и др. В 2004 г. сообщалось о вспышке РСВ у 15 РСВ-положительных симптоматических недоношенных детей, 5 из них (~ 30%) умерли [30]. Во время вспышки, описанной Kilani RA (2002), у 8 новорожденных с очень низким гестационным возрастом была диагностирована RSV-заболевание, 4 из них нуждались в искусственной вентиляции легких, и один умер. В то же время 12 доношенных и поздненедоношенных детей оставались РСВ-негативными и бессимптомными, вероятно, за счет анти-РСВ IgG-антител, проникающих через плаценту в основном в последние месяцы беременности [35].В своем исследовании Halasa и соавт. обобщили значительные негативные последствия вспышки RSV в отделении интенсивной терапии интенсивной терапии для оказания медицинской помощи, больничных расходов и результатов лечения пациентов [36]. Анализируя вспышки РСВ в отделениях интенсивной терапии, большинство авторов приходят к выводу, что стандартные меры инфекционного контроля, такие как изоляция и группирование, строгое мытье рук, халаты и перчатки, являются основными средствами предотвращения или преодоления распространения РСВ. Паливизумаб может помочь ограничить вспышки РСВ в отделениях интенсивной терапии [30, 31, 32, 34, 37, 38, 39], но его использование в таких ситуациях остается спорным и продолжает обсуждаться.Однако применение паливизумаба в практике отделений интенсивной терапии интенсивной терапии в качестве дополнительного инструмента к рутинным мерам инфекционного контроля не редкость [10, 37, 38, 39]. Таким образом, необходимо дополнительно изучить необходимость и эффективность профилактики паливизумабом во время вспышек РСВ в отделениях интенсивной терапии.
Анализируя вспышки РСВ в отделениях интенсивной терапии, большинство авторов приходят к выводу, что стандартные меры инфекционного контроля, такие как изоляция и группирование, строгое мытье рук, халаты и перчатки, являются основными средствами предотвращения или преодоления распространения РСВ. Паливизумаб может помочь ограничить вспышки РСВ в отделениях интенсивной терапии [30, 31, 32, 34, 37, 38, 39], но его использование в таких ситуациях остается спорным и продолжает обсуждаться.Однако применение паливизумаба в практике отделений интенсивной терапии интенсивной терапии в качестве дополнительного инструмента к рутинным мерам инфекционного контроля не редкость [10, 37, 38, 39]. Таким образом, необходимо дополнительно изучить необходимость и эффективность профилактики паливизумабом во время вспышек РСВ в отделениях интенсивной терапии.
Другим аспектом, который следует упомянуть при обсуждении сообщения о вспышке, является длительное выделение РСВ недоношенными пациентами: у большинства из них вторая ПЦР показала положительный результат на РСВ через 1-3 недели после первой пробы, независимо от клиническое выздоровление. Такое длительное выделение РСВ у новорожденных из группы высокого риска может длиться до 4 недель [10, 30, 32]. Это еще больше усложняет контроль вспышек в отделениях интенсивной терапии и требует изоляции пораженных младенцев до выписки или до получения отрицательных результатов ПЦР.
Такое длительное выделение РСВ у новорожденных из группы высокого риска может длиться до 4 недель [10, 30, 32]. Это еще больше усложняет контроль вспышек в отделениях интенсивной терапии и требует изоляции пораженных младенцев до выписки или до получения отрицательных результатов ПЦР.
Хотя доношенные дети также могут быть поражены внутрибольничной РСВ-инфекцией, заболевание обычно протекает в легкой форме. Нашим доношенным симптомным больным требовалась кратковременная госпитализация или лечение на дому с последующим выздоровлением без осложнений.У здоровых доношенных или почти доношенных (34–37 GW) новорожденных пассивный иммунитет, обеспечиваемый трансплацентарными анти-RSV антителами, может помочь снизить количество госпитализаций, связанных с RSV, в первые месяцы жизни. Активная иммунизация женщин во время беременности для профилактики тяжелого течения РСВ в неонатальном периоде и раннем грудном возрасте остается сложной задачей. Также обсуждается подходящее время вакцинации – во втором или третьем триместре. Этого должно быть достаточно для выработки иммунитета у матерей, передачи трансплацентарных антител и защиты новорожденных, в том числе родившихся недоношенными [40].В последние годы деятельность по исследованиям и разработкам вакцин против RSV значительно возросла [21, 41, 42]. Несколько клинических испытаний вакцины против RSV от фазы I до фазы III с различными стратегиями вакцинации, кратко изложенные Rezaee et al., В настоящее время проводятся или были недавно завершены, но на сегодняшний день нет лицензированной вакцины против RSV для беременных женщин [43].
Этого должно быть достаточно для выработки иммунитета у матерей, передачи трансплацентарных антител и защиты новорожденных, в том числе родившихся недоношенными [40].В последние годы деятельность по исследованиям и разработкам вакцин против RSV значительно возросла [21, 41, 42]. Несколько клинических испытаний вакцины против RSV от фазы I до фазы III с различными стратегиями вакцинации, кратко изложенные Rezaee et al., В настоящее время проводятся или были недавно завершены, но на сегодняшний день нет лицензированной вакцины против RSV для беременных женщин [43].
Эпидемическая динамика респираторно-синцитиального вируса в текущем и будущем климате
Данные
Набор данных РСВ на уровне округов США основан на данных о госпитализациях, первоначально полученных из баз данных государственных стационаров (SID) в рамках проекта Healthcare Cost and Utilization Project (HCUP), который поддерживается Агентством исследований и качества в области здравоохранения (AHRQ).Данные HCUP SID представляют в среднем 96% выписанных из стационара местных больниц для сообщающих штатов, хотя не все штаты участвуют в сборе данных. Есть некоторые колебания в количестве общественных больниц, сообщающих с течением времени, в зависимости от штата. Стандартное отклонение в процентной отчетности в среднем составляет 2%. Были включены записи о госпитализации, которые включали код Международной классификации болезней 9-го пересмотра, клиническая модификация (ICD-9-CM) для RSV (079.6, 466.11, 480.1) в рамках 15 диагнозов при выписке.Данные о госпитализации были доступны на еженедельном уровне. Данные о госпитализации доступны с 1989 г., однако изменение кодов отчетности в 1996 г. привело к значительному увеличению числа случаев в настоящее время. Чтобы избежать возможной систематической ошибки из-за переключения в отчетах, мы берем все наблюдения на уровне округов, начиная с 1997 года. Самый длинный временной ряд охватывает 1997–2011 годы. Мы удаляем округа с очень редкими наблюдениями (максимальная заболеваемость <10 случаев), а также удаляем серии нулевых наблюдений с начала временного ряда.Мы удаляем все округа, которые имеют менее 5 лет последовательных наблюдений из-за возможной ошибочной подгонки модели к этому более короткому временному ряду, хотя эти округа сохраняются при построении пространственных средних значений.
Есть некоторые колебания в количестве общественных больниц, сообщающих с течением времени, в зависимости от штата. Стандартное отклонение в процентной отчетности в среднем составляет 2%. Были включены записи о госпитализации, которые включали код Международной классификации болезней 9-го пересмотра, клиническая модификация (ICD-9-CM) для RSV (079.6, 466.11, 480.1) в рамках 15 диагнозов при выписке.Данные о госпитализации были доступны на еженедельном уровне. Данные о госпитализации доступны с 1989 г., однако изменение кодов отчетности в 1996 г. привело к значительному увеличению числа случаев в настоящее время. Чтобы избежать возможной систематической ошибки из-за переключения в отчетах, мы берем все наблюдения на уровне округов, начиная с 1997 года. Самый длинный временной ряд охватывает 1997–2011 годы. Мы удаляем округа с очень редкими наблюдениями (максимальная заболеваемость <10 случаев), а также удаляем серии нулевых наблюдений с начала временного ряда.Мы удаляем все округа, которые имеют менее 5 лет последовательных наблюдений из-за возможной ошибочной подгонки модели к этому более короткому временному ряду, хотя эти округа сохраняются при построении пространственных средних значений.
Данные о госпитализации в Мексике на уровне штата поступают из Subsistema Automatizado de Egresos Hospitalarios (SAEH), собираемой Sistema Nacional de Información en Salud (SINAIS) и контролируемой Secretaría de Salud. Мы берем данные обо всех случаях бронхиолита (коды по МКБ-10 J21.0, J21.1, J21.8, J21.9), серьезная инфекция дыхательных путей, в первую очередь вызванная RSV 38 (дополнительная таблица 8). Данные суммировались за неделю, чтобы соответствовать данным США и отражать время образования РСВ. Данные по Мексике охватывают все годы с 2000 по 2014 год.
Данные о температуре и удельной влажности взяты из набора данных 39 с координатной сеткой Североамериканского регионального повторного анализа (NARR), подготовленного Национальными центрами экологического прогнозирования (NCEP). Этот набор данных с высоким разрешением (32 км, ежедневные наблюдения) охватывает географические и временные масштабы наших данных о здоровье.Данные об осадках поступают от Группы климатических опасностей Инфракрасные осадки со станционными данными (CHIRPS) 40 . Пространственные средние значения строятся с использованием шейп-файлов для округов США из Бюро переписи населения США и для штатов Мексики.
Пространственные средние значения строятся с использованием шейп-файлов для округов США из Бюро переписи населения США и для штатов Мексики.
Данные климатических проекций поступают из проекта взаимного сравнения совмещенных моделей, фаза 5 (CMIP5). Прогнозы осадков исходят из всех моделей CMIP5, работающих по сценарию Репрезентативной траектории концентрации 8.5. Удельная влажность рассчитывается на основе прогнозов температуры и относительной влажности на основе мультимодельного среднего значения, доступ к которому осуществляется через KNMI Climate Explorer (https://climexp.knmi.nl/start.cgi).
Данные о населении США были получены из общедоступных комбинированных файлов данных Бюро переписи населения США, доступных через Национальное бюро экономических исследований. Данные о рождении в США были загружены из Центров по контролю за заболеваниями. Демографические данные по Мексике были получены из Instituto Nacional de Estadística y Geografía. Годовые оценки численности населения округа (США) и штата (Мексика) из этих источников интерполировались на еженедельном уровне с использованием кубического сплайна, чтобы избежать ступенчатых скачков при переходе от одного года к другому.
Данные на уровне округов в Соединенных Штатах более зашумлены, чем средние значения на уровне штатов, использованные в исх. 27 , однако они дают некоторые преимущества. Например, временные ряды на уровне штатов для Калифорнии показывают динамический переход от двухлетних вспышек к ежегодным вспышкам в 1999 г. На уровне округов мы наблюдаем двухгодичные циклы, сохраняющиеся с 1999 г. в Калифорнии и далее, но с северными и южными округами, не совпадающими по фазе ( Дополнительный рис. 4). Это говорит о том, что использование данных на уровне округов может дать более точную картину динамики в конкретном месте.
Определения
Мы определяем три типа динамического паттерна, наблюдаемого во временных рядах для конкретного местоположения в наборе данных. Динамика мелкой впадины определяется, когда среднегодовая минимальная заболеваемость в конкретном месте превышает 5% от средней максимальной заболеваемости. Двухгодичные местоположения определяются с использованием значимости двухгодичного сигнала с использованием периодограммы Ломба-Скаргла. Мы используем значение значимости 1% (все p -значения ниже 5% показаны на дополнительном рис.3а, а также отношение двухлетних и годовых амплитуд Фурье на дополнительном рисунке 3b 27 ). При выполнении моделирования для рис. 3 мы определяем хаотические области как места, где постоянная Ляпунова положительна.
Мы используем значение значимости 1% (все p -значения ниже 5% показаны на дополнительном рис.3а, а также отношение двухлетних и годовых амплитуд Фурье на дополнительном рисунке 3b 27 ). При выполнении моделирования для рис. 3 мы определяем хаотические области как места, где постоянная Ляпунова положительна.
Для расчета средней недели начала мы сначала вычисляем среднюю заболеваемость в неделю (т. е. каждую неделю, усредненную за все годы для данных местностей), а затем нормализуем эти значения между 0 и 1. Мы определяем начало эпидемического периода как 26-е число. неделя года, примерно первая неделя июля.Этот период выбран, поскольку он охватывает все эпидемии в наших данных (дополнительный рисунок 6). Мы определяем начало как когда нормированная заболеваемость превышает 0,2, предполагая, что это значение достаточно низкое, чтобы представлять собой начало, но достаточно высокое, чтобы превысить случайные колебания данных. Использование нормализованной заболеваемости, в отличие от пороговых значений заболеваемости/населения, позволяет создать единую меру для наборов данных как по США, так и по Мексике, несмотря на различия в выборке между двумя местами.
Подход к моделированию
Наш подход к моделированию состоит из двух этапов 29 .Сначала мы используем модель TSIR временных рядов, дискретную временную адаптацию модели SIR 14,41 , чтобы оценить ненаблюдаемую восприимчивую популяцию для каждого местоположения с течением времени. Затем мы используем оценочные восприимчивые временные ряды для построения эмпирической скорости передачи. Скорость передачи используется в качестве зависимой переменной в панельной регрессии, где оценивается влияние климата.
Модель TSIR
Модель TSIR описывает количество инфицированных и восприимчивых лиц в виде набора разностных уравнений.Количество восприимчивых лиц определяется по формуле:
$${S}_{t+1}={S}_{t}+{B}_{t}-{I}_{t}+{u} _{т}$$
(1)
где \({S}_{t}\) и \({I}_{t}\) – количество восприимчивых лиц и количество инфицированных лиц соответственно, а также период времени, \(t\ ), время генерации RSV приблизительно равно 1 неделе. \({B}_{t}\) — рождения, а \({u}_{t}\) — аддитивный шум, при этом \(E[{u}_{t}]=0\). Восприимчивая популяция на каждом временном шаге может быть записана как \({S}_{t}=\bar{S}+{Z}_{t}\), где \(\bar{S}\) – среднее число восприимчивых особей в популяции, а \({Z}_{t}\) – неизвестное отклонение от среднего числа восприимчивых особей на каждом временном шаге.{t-1}I{r}_{k}+{Z}_{t}+{u}_{t}$$
\({B}_{t}\) — рождения, а \({u}_{t}\) — аддитивный шум, при этом \(E[{u}_{t}]=0\). Восприимчивая популяция на каждом временном шаге может быть записана как \({S}_{t}=\bar{S}+{Z}_{t}\), где \(\bar{S}\) – среднее число восприимчивых особей в популяции, а \({Z}_{t}\) – неизвестное отклонение от среднего числа восприимчивых особей на каждом временном шаге.{t-1}I{r}_{k}+{Z}_{t}+{u}_{t}$$
(2)
, где \(\rho\) — частота сообщений, учитывающая как занижение сведений о госпитализациях, вызванных РСВ, так и случаи инфекций, которые не привели к госпитализации, а \(I{r}_{k}\) — зарегистрированная заболеваемость . Используя это уравнение, \({Z}_{t}\) оценивается как остатки от линейной регрессии совокупных рождений по совокупным случаям, предполагая, что \({u}_{t}\) мало. Инверсия наклона линии регрессии дает оценку уровня отчетности \(\rho\).{\альфа}}{S}_{t}}{{N}_{t}}$$
(3)
, которое логарифмически линеаризовано как:
}) + \ альфа {\ mathrm {ln}} ({I} _ {t}) + {\ mathrm {ln}} (\ bar {S} + {Z} _ {t}) – {\ mathrm {ln }}({N}_{t})$$
(4)
, где \({\beta }_{t}\) – двухнедельные коэффициенты, отражающие сезонную тенденцию скорости передачи, а \(\alpha\) – константа, отражающая неоднородности в смешивании и дискретизации непрерывного временного процесса. Мы фиксируем \(\альфа\) на уровне 0,97, чтобы соответствовать предыдущим исследованиям 42 . Предполагается, что двухнедельные сезонные бета-версии, в отличие от еженедельных бета-версий, позволяют избежать переобучения параметров из-за высокой корреляции скоростей передачи в течение последовательных недель. Уравнение (4) аппроксимируется с использованием регрессии Пуассона с логарифмической связью. Окончательные результаты устойчивы к использованию отрицательного бинома на данном этапе (дополнительная таблица 7). Затем можно оценить среднее количество восприимчивых лиц, \(\bar{S}\), используя предельные вероятности профиля из оценки уравнения.{\alpha}{S}_{t}}$$
Мы фиксируем \(\альфа\) на уровне 0,97, чтобы соответствовать предыдущим исследованиям 42 . Предполагается, что двухнедельные сезонные бета-версии, в отличие от еженедельных бета-версий, позволяют избежать переобучения параметров из-за высокой корреляции скоростей передачи в течение последовательных недель. Уравнение (4) аппроксимируется с использованием регрессии Пуассона с логарифмической связью. Окончательные результаты устойчивы к использованию отрицательного бинома на данном этапе (дополнительная таблица 7). Затем можно оценить среднее количество восприимчивых лиц, \(\bar{S}\), используя предельные вероятности профиля из оценки уравнения.{\alpha}{S}_{t}}$$
(5)
Во избежание раздувания \({\rm{Em}}{\beta }_{t}\) мы добавляем один к нулю наблюдения во временном ряду инфицированных, что представляет собой непрерывную низкоуровневую фоновую передачу, приводящую к отсутствию эпидемии. вымирание мы наблюдаем в данных. Результаты модели также устойчивы к удалению нулевых наблюдений из зараженных временных рядов (дополнительная таблица 3). Для установки TSIR используется пакет TSIR 43 .{2}\) подгонки TSIR <0,5 (101 округ). Эти места, как правило, находятся в округах с очень низкой численностью населения, где стохастическая изменчивость низкого уровня в случаях становится пропорциональной величине сезонных колебаний. Наши результаты устойчивы к использованию полного набора данных и порогового значения на основе популяции (дополнительные таблицы 5 и 6). Временные ряды в мексиканском наборе данных более зашумлены, чем в Соединенных Штатах, даже для штатов с большим населением, что, как мы предполагаем, связано со стохастическим характером факторов, определяющих количество осадков, которые преобладают в этом регионе, а также из-за проблем с выборкой, таких как более высокий порог для госпитализации. .В Мексике мы удаляем данные из двух штатов, где модель TSIR не обеспечивает хорошего соответствия из-за очень разреженных данных (максимум менее 10 случаев во временном ряду): Колима и Керетаро. Наш окончательный набор данных, к которому мы подгоняем основную модель регрессии, включает 214 местоположений и в общей сложности 119 802 наблюдения за положением за неделю.
Для установки TSIR используется пакет TSIR 43 .{2}\) подгонки TSIR <0,5 (101 округ). Эти места, как правило, находятся в округах с очень низкой численностью населения, где стохастическая изменчивость низкого уровня в случаях становится пропорциональной величине сезонных колебаний. Наши результаты устойчивы к использованию полного набора данных и порогового значения на основе популяции (дополнительные таблицы 5 и 6). Временные ряды в мексиканском наборе данных более зашумлены, чем в Соединенных Штатах, даже для штатов с большим населением, что, как мы предполагаем, связано со стохастическим характером факторов, определяющих количество осадков, которые преобладают в этом регионе, а также из-за проблем с выборкой, таких как более высокий порог для госпитализации. .В Мексике мы удаляем данные из двух штатов, где модель TSIR не обеспечивает хорошего соответствия из-за очень разреженных данных (максимум менее 10 случаев во временном ряду): Колима и Керетаро. Наш окончательный набор данных, к которому мы подгоняем основную модель регрессии, включает 214 местоположений и в общей сложности 119 802 наблюдения за положением за неделю. Результаты модели устойчивы к включению данных из всех округов США и Мексики (дополнительная таблица 5).
Результаты модели устойчивы к включению данных из всех округов США и Мексики (дополнительная таблица 5).
Панельная регрессия
Мы подгоняем модель линейной регрессии, используя эмпирическую скорость передачи в качестве зависимой переменной:
$${\mathrm{ln}}({\rm{Em}}{\beta }_{t,l })={b}_{1}(1/{H}_{t,l})+{b}_{2}{P}_{t,l}+{\gamma}_{l,m }+{\delta}_{l,y}+{\epsilon}_{t,l}$$
(6)
где \({\rm{Em}}{\beta }_{t,l}\) – эмпирическая передача во время \(t\) и в месте \(l\), \({H}_{ {t}_{l}}\) — влажность, а \({P}_{t,l}\) — осадки.Мы включаем фиктивные переменные местоположения по месяцам \({\gamma }_{l,m}\), которые устраняют сезонные колебания передачи в зависимости от местоположения, которые могут быть смешаны с другими сезонно меняющимися факторами, такими как школьные семестры. Мы также включаем фиктивные данные по годам \({\delta}_{l,y}\), которые удаляют характерные для конкретного местоположения тенденции передачи или эпизодические случаи передачи, которые могут быть ложно коррелированы с климатом. Стандартные ошибки сгруппированы на уровне местоположения, хотя стандартные ошибки Уайта дают аналогичные результаты (дополнительная таблица 4).
Стандартные ошибки сгруппированы на уровне местоположения, хотя стандартные ошибки Уайта дают аналогичные результаты (дополнительная таблица 4).
Непараметрические бинарные модели и общие аддитивные модели также подходят для проверки точности подобранной функциональной формы зависимости удельной влажности и осадков (дополнительные рис. 8 и 9). Запаздывающие осадки и влажность за неделю до передачи проверяются, но не оказываются значительными (дополнительная таблица 9).
Моделирование
Мы запускаем несколько различных симуляций, чтобы проверить влияние климата на динамику эпидемии РСВ.Чтобы позволить климату полностью охарактеризовать сезонные изменения в передаче и средней передаче, мы переоцениваем уравнение. (6) удаление фиктивных переменных управления как:
$${\mathrm{ln}}({\rm{Em}}{\beta}_{t,l})={b}_{1}(1/ {H}_{t,l})+{b}_{2}{P}_{t,l}+{\epsilon}_{t,l}$$
(7)
На эту модель могут повлиять другие сезонно меняющиеся или зависящие от местоположения тренды, и поэтому она представляет собой верхнюю границу климатического воздействия. Результаты этой модели показаны на дополнительном рис.11 и являются значимыми (\(p\ll 0,001\)).
Результаты этой модели показаны на дополнительном рис.11 и являются значимыми (\(p\ll 0,001\)).
Мы запускаем моделирование в пространстве параметров средней передачи и сезонных изменений значений передачи с целью оценки (1) местоположения бифуркаций (рис. 3а, левый график) и (2) разницы между текущей и 2100 прогнозируемой динамикой в будущем. (Рис. 3а, правый график). Чтобы плавно варьировать сезонные изменения пропускания в пространстве параметров, мы используем функцию косинуса для представления сезонности влажности. Моделирование выполняется в течение 50 лет, чтобы исключить влияние переходных процессов, и анализируются только последние 10 лет.Чтобы другие факторы оставались постоянными, демографические данные в этих симуляциях основаны на округе Кингс, штат Нью-Йорк. На рис. 3a (справа) мы начертили стрелку для каждого местоположения в нашем наборе данных, где основание стрелки представляет предполагаемые текущие значения параметров, а точка стрелки представляет прогнозируемые будущие значения параметров.
Чтобы создать рис. 3b, на этот раз мы запускаем моделирование, позволяющее сезонным изменениям климата полностью указать сезонную и среднюю скорость передачи, удаляя косинусную структуру.Мы берем выходные данные всех 23 климатических моделей, включенных в среднее значение CMIP5. Для каждой модели мы рассчитываем отношение среднего количества осадков за неделю в конце века к началу века (используя в каждом случае 5-летнюю среднюю аномалию). Затем мы применяем это отношение к наблюдаемым осадкам в нашем наборе данных, также усредненным за 5-летний период, чтобы свести к минимуму погрешность при сравнении выходных данных модели с данными наблюдений. Мы применяем тот же метод к модельно-средней удельной влажности. Прогнозируемые осадки и влажность вводятся в уравнение.(7) для расчета сезонно меняющейся скорости передачи. Моделирование вперед выполняется на 50 лет, чтобы удалить переходные процессы, и только последние 5 лет показаны на рис. 3b.
Сводка отчета
Дополнительная информация о дизайне исследования доступна в Кратком отчете об исследовании природы, связанном с этой статьей.
Значение всеобщего ношения масок в больницах
Инфекционный контроль Hosp Epidemiol. 2020, 17 августа: 1–4.
, Mnurs, 1 , Mnurs, 1 , Mnurs, 1 , Mnurs, 1 , Mnurs, 1 , Mnurs, 1 , MMEDSC, 2 , PHD, 2 , MD, 3 , MD, 4 , MD, 4 и , MD 1, 2Shuk-Ching Wong
1 Гонконг, Специальная кластерная больница, Королева Мэри, Группа по борьбе с инфекцией, Западный округ Регион, Китай
Жермен Кит-Минг Лам
1 Группа инфекционного контроля, Больница Королевы Марии, Западный кластер Гонконга, Специальный административный район Гонконг, Китай
Кристин Хо-Ян АуЙеунг
1 Группа инфекционного контроля , Больница Королевы Марии, Западный кластер Гонконга, Специальный административный район Гонконг, Китай
Вероника Винг-Мэн Чан
1 Группа инфекционного контроля, Больница Королевы Марии, Западный кластер Гонконга, Специальный административный район Гонконг, Китай
Newton Lau-Dan Wong
1 Группа инфекционного контроля, Больница Королевы Марии, Западный кластер Гонконга, Специальный административный район Гонконг, Китай
Саймон Юнг-Чун Со
2 Отделение микробиологии, Больница Королевы Марии, Специальный административный район Гонконг, Китай
Джонатан Хон-Кван Чен
2 Отделение микробиологии больницы Королевы Марии, Специальный административный район Гонконг, Китай
Иван Фан-Нгай Хунг
3 Департамент медицины, Ли Ка Шинг Медицинский факультет Гонконгского университета, Покфулам, Специальный административный район Гонконг, Китай
Джаспер Фук-Ву Чан
4 Кафедра микробиологии, Ли Ка Шинг Медицинский факультет Гонконгского университета , Специальный административный район Гонконг, Китай
Квок-Юнг Юэн
4 Кафедра микробиологии, Медицинский факультет Ли Ка Шинг, Th e Университет Гонконга, Специальный административный район Гонконг, Китай
Винсент Чи-Чунг Ченг
1 Группа инфекционного контроля, Больница Королевы Марии, Западный кластер Гонконга, Специальный административный район Гонконг, Китай
2 Отделение микробиологии, Больница Королевы Марии, Специальный административный район Гонконг, Китай
1 Группа инфекционного контроля, Больница Королевы Марии, Западный кластер Гонконга, Специальный административный район Гонконг, Китай
2 Отделение микробиологии, Королева Больница Мэри, Специальный административный район Гонконг, Китай
3 Медицинский факультет, Медицинский факультет Ли Ка Шинг, Университет Гонконга, Покфулам, Специальный административный район Гонконг, Китай
4 Кафедра микробиологии, Ли Ка Шинг Медицинский факультет Университета Гонконга, Специальный административный район Гонконг, Китай
Auth или для корреспонденции: Винсент Чи-Чунг Ченг, E-mail: kh. ukh@gnehcccv
ukh@gnehcccvПоступила в редакцию 13 июня 2020 г .; Пересмотрено 3 августа 2020 г .; Принято 5 августа 2020 г.
Авторские права © Общество эпидемиологии здравоохранения Америки, 2020 г. разрешает неограниченное повторное использование, распространение и воспроизведение на любом носителе при условии правильного цитирования оригинальной работы. Эта статья цитировалась другими статьями в PMC.- Дополнительные материалы
Для получения дополнительных материалов, сопровождающих этот документ, посетите http://dx.doi.org/10.1017/ice.2020.425.
GUID: 0B9C9432-C8CC-4BDA-A0A2-FB7864D61331
Abstract
Универсальное ношение масок для медицинских работников и пациентов в больницах было принято для борьбы с коронавирусной болезнью 2019 (COVID-19) с уровнем соблюдения 7,09%. %, соответственно. С февраля по апрель 2020 г. были достигнуты нулевые показатели нозокомиального гриппа А, гриппа В и респираторно-синцитиальной вирусной инфекции, что значительно ниже соответствующих месяцев 2017–2019 гг.
Беспрецедентная вспышка коронавирусной болезни 2019 года (COVID-19) из-за тяжелого острого респираторного синдрома коронавируса 2 (SARS-CoV-2) продолжает распространяться по всему миру. Наличие предсимптомной передачи SARS-CoV-2 побудило нас внедрить всеобщее маскирование в больницах. 1,2 В Гонконге в рамках проактивных мер инфекционного контроля по борьбе с COVID-19 было принято всеобщее ношение масок для медицинских работников (HCW) и пациентов. 3 Поскольку опубликованные данные об эффективности универсальной политики маскирования для предотвращения внутрибольничной передачи респираторных вирусов ограничены, мы проанализировали заболеваемость внутрибольничным гриппом A, гриппом B и респираторно-синцитиальным вирусом (RSV) в сети здравоохранения в Гонконге во время эпохи COVID-19 по сравнению с историческим периодом до введения всеобщего маскирования (т. е. периодом до вмешательства).
Методы
Меры инфекционного контроля при COVID-19
Исследование проводилось в сети медицинских учреждений, включающей отделение неотложной помощи при университете, учебную больницу и 4 больницы расширенного ухода на 3100 коек в Гонконге. В связи со вспышкой пневмонии, вызванной COVID-19, в Ухане, Китай, наш план реагирования изменился с уровня тревоги на уровень серьезного реагирования 4 января 2020 г., а 25 января 2020 г. в Гонконге он был дополнительно повышен до уровня чрезвычайной ситуации. 3 Универсальное ношение масок было введено для всех медработников 4 января 2020 г., а введение в действие началось 25 января 2020 г. Всем пациентам были предоставлены хирургические маски. В дополнение к активному эпиднадзору и ранней изоляции подозрительных случаев для быстрой молекулярной диагностики группа инфекционного контроля больницы также провела интенсивное обучение медработников посредством форумов, посещений отделений и личного обучения надеванию и снятию средств индивидуальной защиты. 3,4 Соблюдалась гигиена рук.
В связи со вспышкой пневмонии, вызванной COVID-19, в Ухане, Китай, наш план реагирования изменился с уровня тревоги на уровень серьезного реагирования 4 января 2020 г., а 25 января 2020 г. в Гонконге он был дополнительно повышен до уровня чрезвычайной ситуации. 3 Универсальное ношение масок было введено для всех медработников 4 января 2020 г., а введение в действие началось 25 января 2020 г. Всем пациентам были предоставлены хирургические маски. В дополнение к активному эпиднадзору и ранней изоляции подозрительных случаев для быстрой молекулярной диагностики группа инфекционного контроля больницы также провела интенсивное обучение медработников посредством форумов, посещений отделений и личного обучения надеванию и снятию средств индивидуальной защиты. 3,4 Соблюдалась гигиена рук.
Соблюдение мер инфекционного контроля
Соблюдение гигиены рук проводилось в соответствии с протоколом Всемирной организации здравоохранения (ВОЗ). Соблюдение всеобщего ношения масок медицинскими работниками и пациентами контролировалось медицинскими сестрами инфекционного контроля (ICN) у постели больного в палатах с открытой кабиной.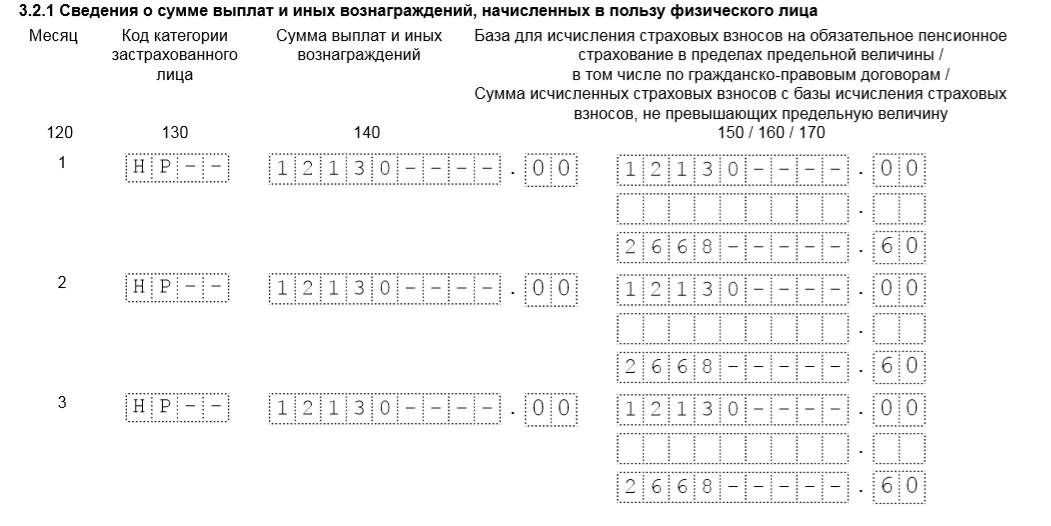 Дизайн палат не менялся в 2020 году. При каждом 20-минутном посещении палаты ИКН также регистрировали эпизоды, когда медработники и пациенты носили хирургические маски ненадлежащим образом (определялось как маска, не полностью закрывающая нос или рот) или не выполняли ручные операции. гигиены сразу после прикосновения к внешней поверхности масок.
Дизайн палат не менялся в 2020 году. При каждом 20-минутном посещении палаты ИКН также регистрировали эпизоды, когда медработники и пациенты носили хирургические маски ненадлежащим образом (определялось как маска, не полностью закрывающая нос или рот) или не выполняли ручные операции. гигиены сразу после прикосновения к внешней поверхности масок.
Клиническая и лабораторная диагностика гриппа и респираторно-синцитиального вируса
В дополнение к диагностике COVID-19 у пациентов с лихорадкой или респираторными симптомами брали носоглоточные аспираты или мазки из носоглотки для исключения других респираторных вирусных инфекций, включая грипп А, грипп B и респираторно-синцитиальный вирус (RSV) с использованием Xpert Xpress Flu/RSV (Cepheid, Sunnyvale, CA) (дополнительный файл 1 онлайн). ICN оценили лабораторные результаты для выявления нозокомиальной респираторной вирусной инфекции, которая была определена как пациенты с началом лихорадки или респираторных симптомов >48 часов после госпитализации, и рекомендовали соответствующие меры инфекционного контроля для предотвращения вспышки в больнице.
Мы отслеживали заболеваемость внутрибольничным заражением гриппом А, гриппом В и РСВ с февраля 2020 г. по апрель 2020 г., после того как 25 января 2020 г. началось введение всеобщего ношения масок. Этот период представляет собой обычный всплеск сезонного гриппа в Гонконге, который происходит с января по апрель и с июля по август (заражение RSV происходит в течение всего года в Гонконге). В качестве доинтервенционного периода для сравнения были выбраны соответствующие месяцы (февраль–апрель) 2017, 2018 и 2019 гг.
Статистический анализ
Тест χ 2 использовался для сравнения независимых категориальных переменных между группами. P < 0,05 считалось статистически значимым.
Результаты
Внутрибольничное заражение гриппом А, гриппом В и РСВ
Количество пациентов, протестированных на грипп А, грипп В и РСВ во время госпитализации, было сопоставимо между двумя периодами (таблица). Отсутствие внутрибольничной инфекции гриппа А, гриппа В и РСВ было достигнуто с февраля по апрель 2020 года в нашей сети здравоохранения. Количество внутрибольничных случаев гриппа А, гриппа В и РСВ в месяц и на 1000 пациенто-дней в месяц было значительно ниже, чем в период до вмешательства (таблица).
Количество внутрибольничных случаев гриппа А, гриппа В и РСВ в месяц и на 1000 пациенто-дней в месяц было значительно ниже, чем в период до вмешательства (таблица).
Таблица 1.
Nosocomial грипп Вирус, вирус гриппа B и дыхательный синцитиальный вирус до и во время COVID-19 ERA
| Переменная | 2017-2019 (FEB-APR) | 2020 апрель) и | P Значение |
|---|---|---|---|
| Лабораторный запрос на выявление респираторных вирусов b | |||
| Общее количествопациентов, обследованных в месяц, среднее ± SD | 1357 ± 188 | 1342 ± 355 | 0,923 |
| 110 ± 13 | 68 ± 16 | . 001 001 | |
| Вирус гриппа А c , d | |||
| Внутрибольничный (NPA или NPS собран >48 часов после поступления)положительных результатов в месяц, среднее значение ± SD | 5 ± 2,7 | 0 ± 0 | ,012 |
| Число положительных результатов на 1000 пациенто-дней в месяц, среднее значение ± SD | 40 4 10 7 0 4 1 0 7 0 4 1 0 7 0 9 0, 07 ± 0, 0,07 | .023 | |
| Вирус гриппа В c , d | |||
| Внутрибольничный (NPA или NPS собран >48 часов после поступления)положительных результатов в месяц, среднее ± SD | 2 ± 3 | 0 ± 0 | 0,386 |
| Число положительных результатов на 1000 пациенто-дней в месяц, среднее ± SD | 10 4 0 7 0,03 9 ± 0,04 | . 403 403 | |
| Респираторно-синцитиальный вирус c , d | |||
| Внутрибольничный (NPA или NPS собран >48 часов после поступления)положительных результатов в месяц, среднее ± SD | 3 ± 2 | 0 ± 0 | .014 |
| Число положительных результатов на 1000 пациенто-дней в месяц, среднее ± SD | 10 4 0 7 0,04 4 ± 0,04 | .023 | |
Соблюдение мер инфекционного контроля
Общее ежемесячное соблюдение гигиены рук (среднее ± SD) с февраля по апрель 2020 г. составило 73,3 ± 2,1%, что сопоставимо с соответствующим показателем в доинтервенционный период ( 76. 9 ± 3,6%) ( P = 0,14). В ходе трехнедельного аудита с 18 мая 2020 г. по 5 июня 2020 г. ICN совершили 74 посещения отделений. Показатели соблюдения режима ношения хирургических масок среди медработников составили 100% (889 из 889), а среди взрослых пациентов — 75,9% (1155 из 1522). Неправильное ношение хирургической маски значительно чаще наблюдалось среди пациентов (132 из 1155, 11,4%), чем среди медработников (11 из 889, 1,2%) ( P < 0,001). Напротив, значительно больше медработников (29 из 889, 3,3%) касались внешней поверхности своей хирургической маски, чем пациенты (18 из 1155, 1,3%).6%) ( P = 0,01) (таблица), но никто из них не выполнял гигиену рук сразу после прикосновения к маске.
9 ± 3,6%) ( P = 0,14). В ходе трехнедельного аудита с 18 мая 2020 г. по 5 июня 2020 г. ICN совершили 74 посещения отделений. Показатели соблюдения режима ношения хирургических масок среди медработников составили 100% (889 из 889), а среди взрослых пациентов — 75,9% (1155 из 1522). Неправильное ношение хирургической маски значительно чаще наблюдалось среди пациентов (132 из 1155, 11,4%), чем среди медработников (11 из 889, 1,2%) ( P < 0,001). Напротив, значительно больше медработников (29 из 889, 3,3%) касались внешней поверхности своей хирургической маски, чем пациенты (18 из 1155, 1,3%).6%) ( P = 0,01) (таблица), но никто из них не выполнял гигиену рук сразу после прикосновения к маске.
Таблица 2.
Соблюдение ношения хирургических масок среди работников здравоохранения и пациентов
| Unit | Эпизоды HCWS наблюдали | Эпизоды HCWS в хирургических масках, № (%) | Эпизоды HCWS в хирургии Маски неправильно, № (%) a | Случаи прикосновения медицинских работников к внешней поверхности хирургических масок, №(%) b | Случаи наблюдения пациентов | Случаи ношения хирургических масок пациентами, количество (%) | Случаи неправильного ношения хирургических масок пациентами, количество (%) Эпизоды больных коснулись наружной поверхности хирургических масок, № (%) B | 14 | Медицина | 394 | 394 | 394 (100) | 3/394 (0,8) | 10/394 2. 5) 5) | 753 | 568 (75,4) | 67/568 (11.8) | 2/568 (0,4) | 9/568 (0,4) 9/568 (0,4) 9/568|||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Операция | 251 | 251 (100) | 5/251 (2.0) | 12/251 (4.8) | 45414 | 482 | 365 (75.7) | 60/365 (16.4) | 16/365 (4.4) | ||||||||||||||||
| Pediatrics | 128 | 128 (100) | 2 / 128 (1. 6) 6) | 5/128 (3.9) | Na | Na | Na | Na | Na | Na | 40 | 40 | 40 (100) | 0 (0) | 1/40 ( 2.5) | 136 | 136 | 105 (77.2) | 105 (77.2) | 1/105 (1. 0) 0) | 0 (0) | 0 (0) | |||
| Obgyn | 23 | 23 (100) | 1/23 (4.3) | 1 / 23 (4.3) | 40 | 40 | 26 (65,0) | 1/26 (3.8) | 0 (0) | ||||||||||||||||
| 53 | 53 (100) | 0 (0) | 0 (0) | 111 | 91 (82,0) | 91 (82,0) | 3/91 (3. 3) 3) | 0 (0) | 0 (0) | ||||||||||||||||
| Всего | 889 | 889 (100) | 11 889 (1.2) D | 29/889 (3.3) 99/889 (3.3) E | 1522 | 1122 | 1,155 (75,9) | 132/1155 (11.4) | 18/1155 (1.6) |
Обсуждение
Для мер инфекционного контроля против респираторных вирусов, отличных от SARS-CoV-2, наши медработники обычно принимают меры предосторожности при воздушно-капельных инфекциях, надев хирургические маски в пределах 1 м от контакта с пациентом и соблюдая гигиену рук.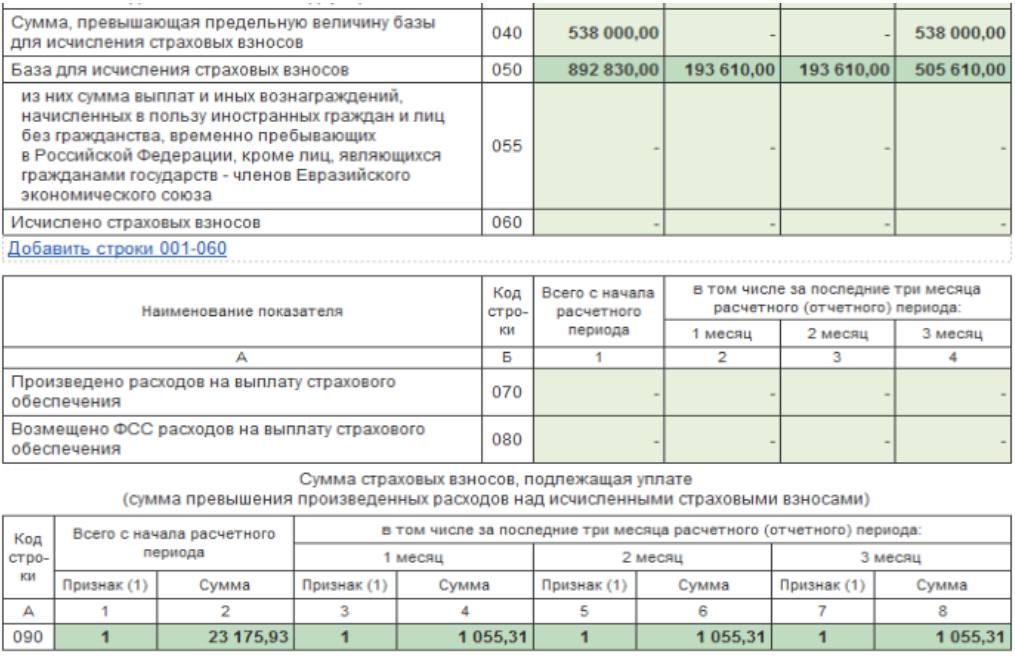 Однако в доинтервенционный период наблюдалось меньшее количество спорадических случаев нозокомиального гриппа А, гриппа В и РСВ, несмотря на нашу практику инфекционного контроля.В эпоху COVID-19 медицинские работники и пациенты дополнительно должны были постоянно носить хирургические маски в больницах. Хотя соблюдение гигиены рук медработниками было сопоставимо до и во время эпохи COVID-19, политика всеобщего ношения масок может быть важным фактором, способствующим достижению нулевого внутрибольничного заражения гриппом А, гриппом В и РСВ.
Однако в доинтервенционный период наблюдалось меньшее количество спорадических случаев нозокомиального гриппа А, гриппа В и РСВ, несмотря на нашу практику инфекционного контроля.В эпоху COVID-19 медицинские работники и пациенты дополнительно должны были постоянно носить хирургические маски в больницах. Хотя соблюдение гигиены рук медработниками было сопоставимо до и во время эпохи COVID-19, политика всеобщего ношения масок может быть важным фактором, способствующим достижению нулевого внутрибольничного заражения гриппом А, гриппом В и РСВ.
Всеобщее ношение масок может уменьшить выделение SARS-CoV-2 или других респираторных вирусов от лиц с симптомами и без симптомов и, таким образом, уменьшить загрязнение окружающей среды, как показано в нашем недавнем исследовании. 5 Кроме того, ношение хирургических масок может также препятствовать ковырянию в носу и прикосновению к глазам, т. е. подсознательному поведению 6 , которое создает риск самозаражения патогенов из окружающей среды через загрязненные руки. Этот фактор является причиной того, что мы так активно продвигаем наш шестой принцип, разработанный учреждением, «гигиена рук перед прикосновением к слизистой оболочке» вместе с практикой ВОЗ «Пять моментов для гигиены рук». 7,8
Этот фактор является причиной того, что мы так активно продвигаем наш шестой принцип, разработанный учреждением, «гигиена рук перед прикосновением к слизистой оболочке» вместе с практикой ВОЗ «Пять моментов для гигиены рук». 7,8
Соблюдение всеобщего маскирования контролировалось в период с мая по июнь 2020 г., через 4 месяца после активации уровня экстренного реагирования, когда в наших больницах было введено всеобщее ношение масок.Соблюдение всеобщего ношения масок среди медработников остается на 100%, что позволяет предположить, что практика всеобщего ношения масок среди медработников устойчива в эпоху COVID-19. Однако несколько медработников неправильно носили хирургические маски и не соблюдали гигиену рук сразу после прикосновения к внешней поверхности масок, что указывает на необходимость дальнейшего обучения. Понятно, что не все проверенные пациенты носили хирургические маски из-за их бессознательного состояния или нестабильного клинического состояния. Однако ношение хирургических масок медработниками или пациентами в больнице успешно предотвратило вспышку нозокомиального гриппа А во время пандемии 2009 года. 9 В нашей модели хомяков для COVID-19 перегородка хирургической маски, размещенная между клетками, в которых содержатся хомяки, инфицированные SARS-CoV-2, и клетками, в которых содержатся незащищенные хомячки, значительно снизила скорость бесконтактной передачи. 10
9 В нашей модели хомяков для COVID-19 перегородка хирургической маски, размещенная между клетками, в которых содержатся хомяки, инфицированные SARS-CoV-2, и клетками, в которых содержатся незащищенные хомячки, значительно снизила скорость бесконтактной передачи. 10
Универсальное ношение масок в больницах в эпоху COVID-19 заслуживает дальнейшего изучения. Учитывая другие усиленные меры инфекционного контроля при пандемии COVID-19 в 2020 году в качестве потенциальных сопутствующих переменных, всеобщее ношение масок представляется ключевой мерой для контроля передачи респираторных вирусов, а также для достижения нулевой внутрибольничной передачи COVID-19, гриппа А, гриппа B и RSV в нашей сети здравоохранения.
Благодарность
Мы благодарим наших медицинских работников за борьбу с пандемией COVID-19.
Дополнительный материал
Для получения дополнительных материалов, сопровождающих этот документ, посетите http://dx.doi.org/10. 1017/ice.2020.425.
1017/ice.2020.425.
Финансовая поддержка
Финансовая поддержка по данной статье не предоставлялась.
Конфликт интересов
Все авторы сообщают об отсутствии конфликта интересов, относящегося к этой статье.
Ссылки
1.Адвани С.Д., Смит Б.А., Льюис С.С., Андерсон Д.Дж., Секстон Д.Дж. Всеобщее маскирование в больницах в эпоху COVID-19: пора ли задуматься об экранировании? Инфекционный контроль Hosp Epidemiol 2020. 29 апреля [Epub перед печатью]. doi: 10.1017/ice.2020.179. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]2. Кломпас М., Моррис К.А., Синклер Дж., Пирсон М., Шеной Э.С. Всеобщее маскирование в больницах в эпоху COVID-19. N Engl J Med 2020;382(21):e63. дои: 10.1056/NEJMp2006372. [PubMed] [CrossRef] [Google Scholar]3. Cheng VCC, Wong SC, Chen JHK и др.Эскалация мер инфекционного контроля в связи с быстро развивающейся эпидемиологией коронавирусной болезни 2019 года (COVID-19), вызванной SARS-CoV-2 в Гонконге. Инфекционный контроль Hosp Epidemiol 2020; 41: 493–498. [Бесплатная статья PMC] [PubMed] [Google Scholar]4.
Cheng VCC, Wong SC, Chuang VWM и др.
Отсутствие нозокомиальной передачи коронавирусной болезни 2019 (COVID-19) из-за SARS-CoV-2 на предпандемической фазе в Гонконге. Am J Infect Control
2020; 48: 890–896. [Бесплатная статья PMC] [PubMed] [Google Scholar]5.
Ченг В.К., Вонг С.К., Чан В.В. и др.Взятие проб воздуха и окружающей среды на SARS-CoV-2 вокруг госпитализированных пациентов с коронавирусной болезнью 2019 (COVID-19). Инфекционный контроль Hosp Epidemiol
2020. 8 июня [Epub перед печатью]. doi: 10.1017/ice.2020.282. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]6.
Квок Ю.Л.А., Гралтон Дж., Маклоус М.Л. Прикосновение к лицу: частая привычка, которая влияет на гигиену рук. Am J Infect Control
2015;43:112–114. [Бесплатная статья PMC] [PubMed] [Google Scholar]7.
Wong SC, AuYeung CHY, Lam GKM и др.
Возможно ли добиться 100% соблюдения гигиены рук во время пандемии коронавирусной болезни 2019 (COVID-19)?
Джей Хосп заражает
2020.
[Бесплатная статья PMC] [PubMed] [Google Scholar]4.
Cheng VCC, Wong SC, Chuang VWM и др.
Отсутствие нозокомиальной передачи коронавирусной болезни 2019 (COVID-19) из-за SARS-CoV-2 на предпандемической фазе в Гонконге. Am J Infect Control
2020; 48: 890–896. [Бесплатная статья PMC] [PubMed] [Google Scholar]5.
Ченг В.К., Вонг С.К., Чан В.В. и др.Взятие проб воздуха и окружающей среды на SARS-CoV-2 вокруг госпитализированных пациентов с коронавирусной болезнью 2019 (COVID-19). Инфекционный контроль Hosp Epidemiol
2020. 8 июня [Epub перед печатью]. doi: 10.1017/ice.2020.282. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]6.
Квок Ю.Л.А., Гралтон Дж., Маклоус М.Л. Прикосновение к лицу: частая привычка, которая влияет на гигиену рук. Am J Infect Control
2015;43:112–114. [Бесплатная статья PMC] [PubMed] [Google Scholar]7.
Wong SC, AuYeung CHY, Lam GKM и др.
Возможно ли добиться 100% соблюдения гигиены рук во время пандемии коронавирусной болезни 2019 (COVID-19)?
Джей Хосп заражает
2020. 15 мая: S0195-6701(20)30247-4. [Google Академия]8.
Cheng VCC, Wong SC, Wong SCY, Yuen KY. Гигиена рук под непосредственным наблюдением — от медицинских работников до пациентов. Джей Хосп заражает
2019;101:380–382. [PubMed] [Google Scholar]9.
Ченг В.К., Тай Дж.В., Вонг Л.М. и др.
Профилактика внутрибольничной передачи вируса пандемического гриппа свиного происхождения A/h2N1 с помощью пакета инфекционного контроля. Джей Хосп заражает
2010; 74: 271–277. [Бесплатная статья PMC] [PubMed] [Google Scholar]10.
Чан Дж.Ф., Юань С., Чжан А.Дж. и др.
Хирургическая перегородка в маске снижает риск бесконтактной передачи коронавируса в модели золотого сирийского хомяка 2019 (COVID-19).Клин заразить Dis
2020. [Epub перед печатью]. doi: 10.1093/cid/ciaa644. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
15 мая: S0195-6701(20)30247-4. [Google Академия]8.
Cheng VCC, Wong SC, Wong SCY, Yuen KY. Гигиена рук под непосредственным наблюдением — от медицинских работников до пациентов. Джей Хосп заражает
2019;101:380–382. [PubMed] [Google Scholar]9.
Ченг В.К., Тай Дж.В., Вонг Л.М. и др.
Профилактика внутрибольничной передачи вируса пандемического гриппа свиного происхождения A/h2N1 с помощью пакета инфекционного контроля. Джей Хосп заражает
2010; 74: 271–277. [Бесплатная статья PMC] [PubMed] [Google Scholar]10.
Чан Дж.Ф., Юань С., Чжан А.Дж. и др.
Хирургическая перегородка в маске снижает риск бесконтактной передачи коронавируса в модели золотого сирийского хомяка 2019 (COVID-19).Клин заразить Dis
2020. [Epub перед печатью]. doi: 10.1093/cid/ciaa644. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]Frontiers | Реакция антигенных сайт-специфических конкурентных антител на гибридный белок респираторно-синцитиального вируса была связана с элиминацией вируса при трансплантации гемопоэтических клеток у взрослых
Введение
Респираторно-синцитиальный вирус (RSV) представляет собой одноцепочечный РНК-вирус с отрицательным смыслом семейства Pneumoviridae . РСВ передается через фомиты и крупнокапельные аэрозоли. РСВ, традиционно считающийся наиболее частым респираторным возбудителем у детей в возрасте до 5 лет, недавно было обнаружено, что он широко распространен среди лиц с ослабленным иммунитетом (1, 2). РСВ также является основной причиной тяжелых респираторных инфекций у детей и взрослых с ослабленной иммунной системой, при этом уровень смертности достигает 80% (3). Реципиенты трансплантации гемопоэтических клеток (HCT) очень уязвимы к тяжелым последствиям инфекции RSV с самым высоким риском смертности в течение 100 дней после трансплантации (4).Лицензированная вакцина против RSV еще не доступна из-за проблем со стабильностью, чистотой, воспроизводимостью, переносимостью и активностью вакцин-кандидатов (5–8). Более того, пациенты с ослабленным иммунитетом могут не реагировать адекватно на вакцинацию из-за относительной иммунологической супрессии. Текущие стратегии лечения с доказанной эффективностью у пациентов с ослабленным иммунитетом включают противовирусную терапию, такую как рибавирин, паливизумаб, и иммуномодуляцию с тотальным ВВИГ (9–11).
РСВ передается через фомиты и крупнокапельные аэрозоли. РСВ, традиционно считающийся наиболее частым респираторным возбудителем у детей в возрасте до 5 лет, недавно было обнаружено, что он широко распространен среди лиц с ослабленным иммунитетом (1, 2). РСВ также является основной причиной тяжелых респираторных инфекций у детей и взрослых с ослабленной иммунной системой, при этом уровень смертности достигает 80% (3). Реципиенты трансплантации гемопоэтических клеток (HCT) очень уязвимы к тяжелым последствиям инфекции RSV с самым высоким риском смертности в течение 100 дней после трансплантации (4).Лицензированная вакцина против RSV еще не доступна из-за проблем со стабильностью, чистотой, воспроизводимостью, переносимостью и активностью вакцин-кандидатов (5–8). Более того, пациенты с ослабленным иммунитетом могут не реагировать адекватно на вакцинацию из-за относительной иммунологической супрессии. Текущие стратегии лечения с доказанной эффективностью у пациентов с ослабленным иммунитетом включают противовирусную терапию, такую как рибавирин, паливизумаб, и иммуномодуляцию с тотальным ВВИГ (9–11).
RSV представляет собой белок класса I, который опосредует проникновение вируса в клетки-хозяева путем трансформации из метастабильной тримерной конформации до слияния (pre-F) в высокостабильную конформацию после слияния (post-F).Антигенная топология RSV F существенно изменяется во время этого перехода. Молекулы, которые предотвращают эти структурные изменения, могут предотвратить слияние вирусов и потенциально могут использоваться в качестве терапевтических средств для лечения инфекции RSV. Некоторые группы эпитопов, называемые антигенными сайтами, обычно сохраняются как в пре-F, так и в пост-F конформациях, тогда как другие обнаруживаются либо в пре-F, либо в пост-F конформациях (12). Описано шесть антигенных участков на белке F: Ø-V. Антигенный сайт Ø («нулевой») находится на вершине пре-F-тримера.Пре-F-специфические антитела (MEDI8897 и D25) распознают антигенный сайт Ø (13). Антигенный сайт I находится в конформации post-F. mAb 131-2A связывается с антигенным сайтом I при пост-F-подтверждении (14, 15). Антигенные сайты II и IV находятся как в пре-F, так и в пост-F конформациях. Паливизумаб (Синагис) является первым охарактеризованным моноклональным антителом (мАт) и в настоящее время единственным лицензированным моноклональным антителом для профилактики тяжелой РСВ-инфекции у детей из группы высокого риска. Он распознает антигенный сайт II. mAb 101F распознает антигенный сайт IV.Хотя элементы вторичной структуры, формирующие сайт III, присутствуют как в пре-F, так и в пост-F, они принимают различное пространственное расположение в пост-F, что приводит к более высокому сродству к связыванию с пре-F (16). Показано, что сильно нейтрализующее mAb MPE8 распознает антигенный сайт III (16). Антигенный сайт V находится в конформации pre-F и расположен между сайтами Ø и III. mAb AM14 нацеливается на антигенный сайт V и является сильно нейтрализующим mAb (17, 18).
Антигенные сайты II и IV находятся как в пре-F, так и в пост-F конформациях. Паливизумаб (Синагис) является первым охарактеризованным моноклональным антителом (мАт) и в настоящее время единственным лицензированным моноклональным антителом для профилактики тяжелой РСВ-инфекции у детей из группы высокого риска. Он распознает антигенный сайт II. mAb 101F распознает антигенный сайт IV.Хотя элементы вторичной структуры, формирующие сайт III, присутствуют как в пре-F, так и в пост-F, они принимают различное пространственное расположение в пост-F, что приводит к более высокому сродству к связыванию с пре-F (16). Показано, что сильно нейтрализующее mAb MPE8 распознает антигенный сайт III (16). Антигенный сайт V находится в конформации pre-F и расположен между сайтами Ø и III. mAb AM14 нацеливается на антигенный сайт V и является сильно нейтрализующим mAb (17, 18).
RSV представляет собой в первую очередь вирус, ограниченный слизистой оболочкой, вызывающий повреждение верхних и нижних дыхательных путей во время многочисленных раундов репликации. Он может вызывать клеточные и гуморальные иммунные реакции на разных уровнях у реципиентов HCT, в зависимости от степени иммунодефицита людей после трансплантации. Нейтрализующие антитела, специфичные для RSV, играют важную роль в предотвращении тяжелой инфекции, в то время как считается, что клеточные иммунные ответы играют критическую роль в разрушении инфицированных RSV клеток и, таким образом, в устранении инфекции. Ранее не инфицированные РСВ, но иммунокомпетентные младенцы могут выделять РСВ из верхних дыхательных путей (ВДП) до 21 дня; напротив, дети с ослабленным иммунитетом могут выделять РСВ в течение нескольких месяцев (19, 20).В мышиной модели инфекции RSV CD8+ Т-клетки способны устранять инфекцию RSV (14, 21–23). Ограниченные данные исследований младенцев с первичной инфекцией RSV позволяют предположить, что клеточный иммунный ответ со специфическими цитотоксическими Т-лимфоцитами инициируется в течение 10 дней после заражения (24, 25). Сообщалось об исследованиях гуморального иммунного ответа после первичной инфекции RSV у детей и повторной инфекции у детей и взрослых (26–28).
Он может вызывать клеточные и гуморальные иммунные реакции на разных уровнях у реципиентов HCT, в зависимости от степени иммунодефицита людей после трансплантации. Нейтрализующие антитела, специфичные для RSV, играют важную роль в предотвращении тяжелой инфекции, в то время как считается, что клеточные иммунные ответы играют критическую роль в разрушении инфицированных RSV клеток и, таким образом, в устранении инфекции. Ранее не инфицированные РСВ, но иммунокомпетентные младенцы могут выделять РСВ из верхних дыхательных путей (ВДП) до 21 дня; напротив, дети с ослабленным иммунитетом могут выделять РСВ в течение нескольких месяцев (19, 20).В мышиной модели инфекции RSV CD8+ Т-клетки способны устранять инфекцию RSV (14, 21–23). Ограниченные данные исследований младенцев с первичной инфекцией RSV позволяют предположить, что клеточный иммунный ответ со специфическими цитотоксическими Т-лимфоцитами инициируется в течение 10 дней после заражения (24, 25). Сообщалось об исследованиях гуморального иммунного ответа после первичной инфекции RSV у детей и повторной инфекции у детей и взрослых (26–28). Хотя введение внутривенного иммуноглобулина (ВВИГ) с высокой активностью нейтрализующих антител против РСВ и паливизумаба обеспечивает защиту от тяжелой РСВ-инфекции у детей из группы высокого риска, роль нейтрализующих антител в выздоровлении от развившейся инфекции не ясна.Ранее мы продемонстрировали, что значительно более высокие уровни гуморальных антител, конкурирующих с паливизумабом, и титры нейтрализующих антител связаны с более быстрым клиренсом RSV у реципиентов HCT. Эта когорта из сорока инфицированных RSV взрослых HCT предоставила нам возможность для дальнейшего изучения других уровней конкурентных антител, специфичных к эпитопу RSV, и выявления дополнительных иммунных коррелятов вирусного клиренса. Были разработаны и стандартизированы еще три анализа конкурентных антител, специфичных к эпитопу RSV, для обнаружения конкурентных антител к антигенным сайтам Ø, I и IV.Кроме того, понимание взаимосвязи между нейтрализующими антителами и эпитопной специфичностью конкурентных антител, вырабатываемых в ответ на естественную инфекцию РСВ, будет иметь решающее значение при выборе и разработке новых моноклональных антител и вакцин для профилактики РСВ.
Хотя введение внутривенного иммуноглобулина (ВВИГ) с высокой активностью нейтрализующих антител против РСВ и паливизумаба обеспечивает защиту от тяжелой РСВ-инфекции у детей из группы высокого риска, роль нейтрализующих антител в выздоровлении от развившейся инфекции не ясна.Ранее мы продемонстрировали, что значительно более высокие уровни гуморальных антител, конкурирующих с паливизумабом, и титры нейтрализующих антител связаны с более быстрым клиренсом RSV у реципиентов HCT. Эта когорта из сорока инфицированных RSV взрослых HCT предоставила нам возможность для дальнейшего изучения других уровней конкурентных антител, специфичных к эпитопу RSV, и выявления дополнительных иммунных коррелятов вирусного клиренса. Были разработаны и стандартизированы еще три анализа конкурентных антител, специфичных к эпитопу RSV, для обнаружения конкурентных антител к антигенным сайтам Ø, I и IV.Кроме того, понимание взаимосвязи между нейтрализующими антителами и эпитопной специфичностью конкурентных антител, вырабатываемых в ответ на естественную инфекцию РСВ, будет иметь решающее значение при выборе и разработке новых моноклональных антител и вакцин для профилактики РСВ.
Методы
Объекты исследования
реципиентов HCT с лабораторно подтвержденной инфекцией верхних дыхательных путей RSV при включении и отрицательными результатами рентгенографии грудной клетки были зарегистрированы в течение 72 часов после постановки диагноза RSV и стратифицированы по уровню риска прогрессирования в нижние дыхательные пути, как описано ранее (29).С января 2012 г. по апрель 2015 г. у всех пациентов собирали сыворотку при поступлении (острый период) и через 14–60 дней после госпитализации (выздоравливающий) для оценки гуморального иммунного ответа. Образцы назального смыва собирали при включении в исследование, на 7-й день (±1), 14-й день (±1) и между 21-м и 28-м днем (±1) для обнаружения вирусов подтипов RSV/A и RSV/B с помощью реальных тестов. время, полимеразная цепная реакция с обратной транскрипцией (RT-PCR). При зачислении было проведено интервью для получения исторической информации, а медицинские записи были просмотрены для извлечения демографических и клинических данных. Институциональные наблюдательные советы Онкологического центра им. М. Д. Андерсона Техасского университета и Медицинского колледжа Бэйлора одобрили протокол исследования, и от всех участников было получено письменное информированное согласие.
Институциональные наблюдательные советы Онкологического центра им. М. Д. Андерсона Техасского университета и Медицинского колледжа Бэйлора одобрили протокол исследования, и от всех участников было получено письменное информированное согласие.
Полимеразная цепная реакция с обратной транскрипцией в реальном времени (RT-PCR)
Экстракцию вирусной РНК и обнаружение RSV/A и RSV/B в образцах смыва из носа с помощью RT-PCR в сертифицированной CLIA лаборатории диагностики респираторных вирусов (CLIA ID# 45D0919666) проводили, как описано ранее (30).
Анализ конкурентных антител антигенного сайта
Для измерения концентрации антител, конкурирующих с D25 (участок Ø), антитела, конкурирующего с 131-2A (участок I), антитела, конкурирующего с паливизумабом (участок II), и антитела, конкурирующего с 101F (участок IV) в сыворотке, которые конкурируют с биотинилированными моноклональными антителами за связывание с соответствующим антигенным участком слитого белка RSV. D25 и 101F были приобретены у Cambridge Biologics, LLC, Бруклин, Массачусетс, США.Паливизумаб был получен от MedImmune, LLC, Gaithersburg, MD, USA. 131-2A был получен от EMD Millipore Corporation, Темекула, Калифорния, США. mAb биотинилировали с помощью набора для биотинилирования антител Pierce TM (Pierce, Rockford, IL, USA) в соответствии с инструкциями производителя. Источником слитого белка был очищенный от сахарозы RSV/A/Bernett (spRSV, GA1) для сайтов I, II и IV. Сто мкл spRSV (общий белок 7 мкг/мл) наносили на 96-луночный планшет Immulon 2HB (Thermo Scientific, Waltham, MA, USA) на 18 ч при 4°C.Для анализа конкурентных антител сайта Ø 100 мкл клеточной суспензии HEp-2 (24 x 10 4 клеток/мл) в 10% FBS/MEM высевали на 96-луночные планшеты для тканевых культур Falcon от Corning (Питтстон, Пенсильвания, США). ). Планшеты инкубировали при 37°C с 5% CO 2 и влажностью 85% в течение 24 часов для образования монослоев. Клетки инокулировали spRSV (MOI = 0,002) и инкубировали в тех же условиях в течение 2 дней.
D25 и 101F были приобретены у Cambridge Biologics, LLC, Бруклин, Массачусетс, США.Паливизумаб был получен от MedImmune, LLC, Gaithersburg, MD, USA. 131-2A был получен от EMD Millipore Corporation, Темекула, Калифорния, США. mAb биотинилировали с помощью набора для биотинилирования антител Pierce TM (Pierce, Rockford, IL, USA) в соответствии с инструкциями производителя. Источником слитого белка был очищенный от сахарозы RSV/A/Bernett (spRSV, GA1) для сайтов I, II и IV. Сто мкл spRSV (общий белок 7 мкг/мл) наносили на 96-луночный планшет Immulon 2HB (Thermo Scientific, Waltham, MA, USA) на 18 ч при 4°C.Для анализа конкурентных антител сайта Ø 100 мкл клеточной суспензии HEp-2 (24 x 10 4 клеток/мл) в 10% FBS/MEM высевали на 96-луночные планшеты для тканевых культур Falcon от Corning (Питтстон, Пенсильвания, США). ). Планшеты инкубировали при 37°C с 5% CO 2 и влажностью 85% в течение 24 часов для образования монослоев. Клетки инокулировали spRSV (MOI = 0,002) и инкубировали в тех же условиях в течение 2 дней. Планшеты всех четырех анализов блокировали на 1 ч 5% молоком (сухое быстрорастворимое обезжиренное молоко с гвоздикой) в 1X фосфатно-солевом буфере.Минимум 100 мкл D25, 131-2A, паливизумаба и 101F в концентрации 1,25 мкг/мл в 5% молоке (для 131-2A, паливизумаба и 101F) и 5% молока в 10% определенной эмбриональной телячьей сыворотке Среду Essential Medium (для D25) добавляли в двух повторностях с последующим двукратным серийным разведением (от 12 500 до 24,41 нг/мл) для получения стандартной кривой на каждом планшете. Затем в планшеты с покрытием добавляли 50 мкл 2-кратных серийных разведений образцов сыворотки (от 1:5 до 1:2,560) в двух повторностях, а затем сразу 50 мкл 100 нг/мл биотинилированных мАТ (D25, 131-2A, добавляли паливизумаб и 101F), полученные с помощью набора для биотинилирования антител Pierce TM (Pierce, Rockford, IL) в соответствии с инструкциями производителя, с последующей инкубацией в течение 1 часа.После промывания добавляли HRP-конъюгированный стрептавидин (SeraCare Life Sciences, Gaithersburg, MD) еще на час.
Планшеты всех четырех анализов блокировали на 1 ч 5% молоком (сухое быстрорастворимое обезжиренное молоко с гвоздикой) в 1X фосфатно-солевом буфере.Минимум 100 мкл D25, 131-2A, паливизумаба и 101F в концентрации 1,25 мкг/мл в 5% молоке (для 131-2A, паливизумаба и 101F) и 5% молока в 10% определенной эмбриональной телячьей сыворотке Среду Essential Medium (для D25) добавляли в двух повторностях с последующим двукратным серийным разведением (от 12 500 до 24,41 нг/мл) для получения стандартной кривой на каждом планшете. Затем в планшеты с покрытием добавляли 50 мкл 2-кратных серийных разведений образцов сыворотки (от 1:5 до 1:2,560) в двух повторностях, а затем сразу 50 мкл 100 нг/мл биотинилированных мАТ (D25, 131-2A, добавляли паливизумаб и 101F), полученные с помощью набора для биотинилирования антител Pierce TM (Pierce, Rockford, IL) в соответствии с инструкциями производителя, с последующей инкубацией в течение 1 часа.После промывания добавляли HRP-конъюгированный стрептавидин (SeraCare Life Sciences, Gaithersburg, MD) еще на час.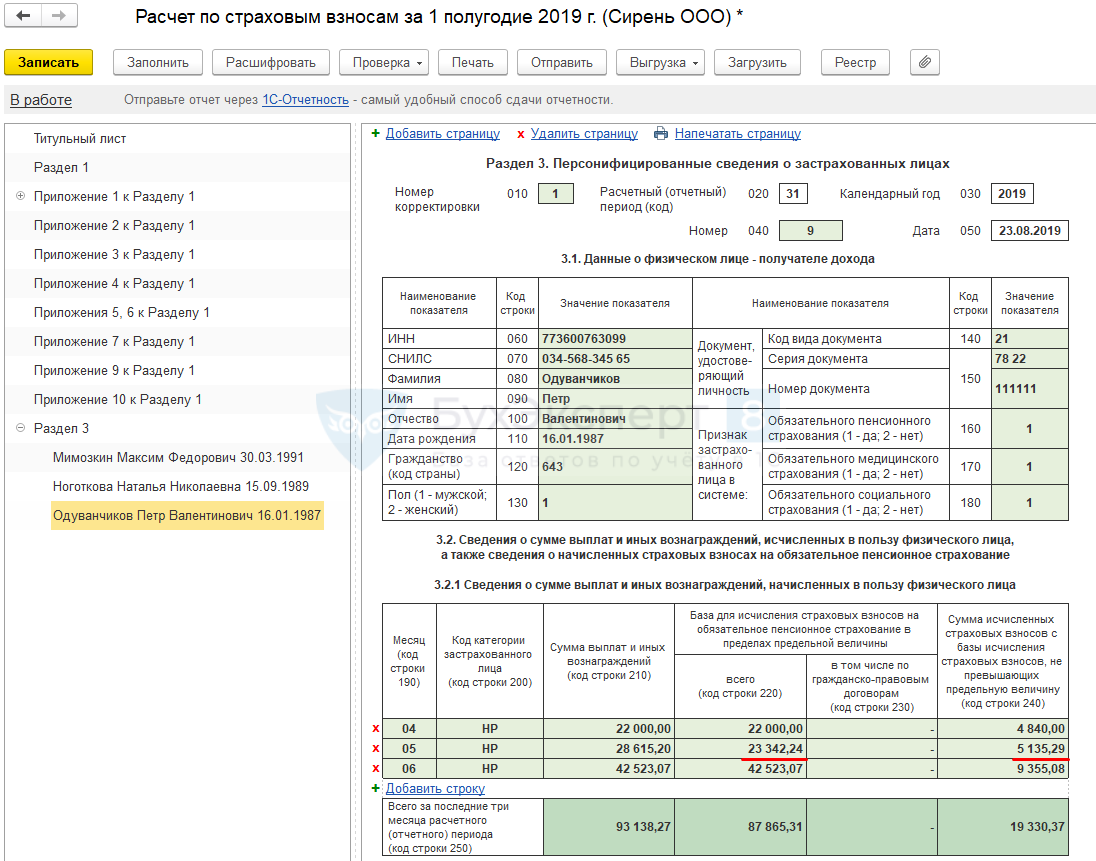 Лунки, содержащие биотинилированные mAb без сыворотки, служили в качестве положительных контролей, представляющих максимальное связывание. Отрицательным контролем служили лунки без биотинилированных mAb, содержащие либо 5% молока вместо сыворотки, либо лунки, содержащие сыворотку. Модель четырехпараметрической логистической регрессии (4PL) использовалась для расчета концентраций конкурентных антител (мкг/мл) на основе динамического диапазона стандартной кривой путем интерполяции концентрации стандартов, соответствующей значению поглощения, при котором тестируемая сыворотка образец приводил к 50% ингибированию.Нижний предел обнаружения (LLoD) составлял 1,0 мкг/мл для анализа конкурентных антител на сайте I, II и IV и 7,8 мкг/мл для анализа конкурентного антитела на сайте Ø. Образцам с концентрацией ниже LLoD было присвоено значение 0,5 и 3,9 мкг/мл соответственно.
Лунки, содержащие биотинилированные mAb без сыворотки, служили в качестве положительных контролей, представляющих максимальное связывание. Отрицательным контролем служили лунки без биотинилированных mAb, содержащие либо 5% молока вместо сыворотки, либо лунки, содержащие сыворотку. Модель четырехпараметрической логистической регрессии (4PL) использовалась для расчета концентраций конкурентных антител (мкг/мл) на основе динамического диапазона стандартной кривой путем интерполяции концентрации стандартов, соответствующей значению поглощения, при котором тестируемая сыворотка образец приводил к 50% ингибированию.Нижний предел обнаружения (LLoD) составлял 1,0 мкг/мл для анализа конкурентных антител на сайте I, II и IV и 7,8 мкг/мл для анализа конкурентного антитела на сайте Ø. Образцам с концентрацией ниже LLoD было присвоено значение 0,5 и 3,9 мкг/мл соответственно.
Анализ специфической микронейтрализации белка RSV F (MN)
Образцы сыворотки и четыре mAb (D25, 131-2A, паливизумаб и 101F) были проанализированы на наличие нейтрализующих антител (Nt Ab) против RSV/A/Tracy и RSV/B/18537 в клетках HEp-2 с использованием квалифицированного анализа микронейтрализации. как описано ранее (31–33).Образцы сыворотки и моноклональные антитела (конечная концентрация 40 мкг/мл) сначала разбавляли 1:8, а затем последовательно разбавляли в 2 раза. К каждому разведению добавляли равный объем RSV/A Tracy или RSV/B 18537 и инкубировали при 36°C с 5% CO 2 в течение 90 минут. В каждую лунку 96-луночного планшета добавляли по сто мкл клеток HEp 2 и инкубировали в течение 6–7 или 7–8 дней для анализов микронейтрализации RSV/A и RSV/B соответственно. Затем 96-луночные планшеты фиксировали и окрашивали раствором 10% формалина/0,01% кристаллического фиолетового в течение ~24 ч.После того, как 96-луночные планшеты были высушены на воздухе, их считывали. Титры нейтрализующих антител определяли как конечное разведение, при котором наблюдалось 50% снижение вирусного цитопатического эффекта (ЦПЭ). Любому образцу сыворотки с титром < LLoD (2,5 log2) присваивали значение 2 log2. Любые mAb, дающие титр < LLoD, тестировали повторно с использованием маточного раствора (1,0 мг/мл) и присваивали значение 0,2 log2, если титр снова был отрицательным.
как описано ранее (31–33).Образцы сыворотки и моноклональные антитела (конечная концентрация 40 мкг/мл) сначала разбавляли 1:8, а затем последовательно разбавляли в 2 раза. К каждому разведению добавляли равный объем RSV/A Tracy или RSV/B 18537 и инкубировали при 36°C с 5% CO 2 в течение 90 минут. В каждую лунку 96-луночного планшета добавляли по сто мкл клеток HEp 2 и инкубировали в течение 6–7 или 7–8 дней для анализов микронейтрализации RSV/A и RSV/B соответственно. Затем 96-луночные планшеты фиксировали и окрашивали раствором 10% формалина/0,01% кристаллического фиолетового в течение ~24 ч.После того, как 96-луночные планшеты были высушены на воздухе, их считывали. Титры нейтрализующих антител определяли как конечное разведение, при котором наблюдалось 50% снижение вирусного цитопатического эффекта (ЦПЭ). Любому образцу сыворотки с титром < LLoD (2,5 log2) присваивали значение 2 log2. Любые mAb, дающие титр < LLoD, тестировали повторно с использованием маточного раствора (1,0 мг/мл) и присваивали значение 0,2 log2, если титр снова был отрицательным.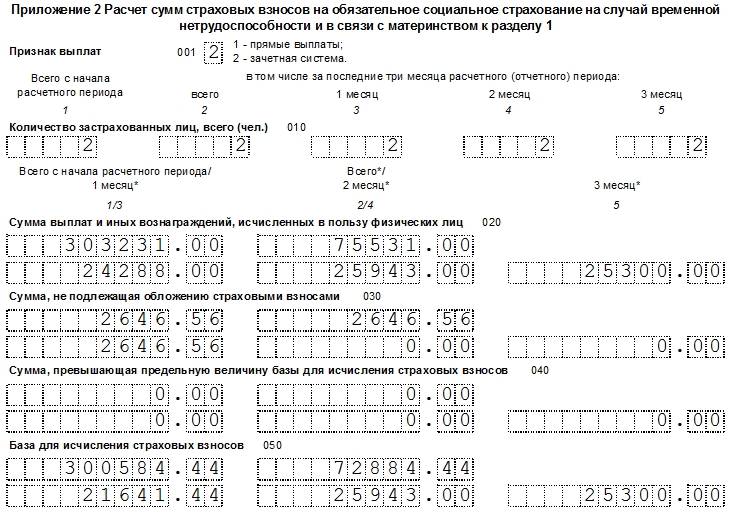
Статистический анализ
Для демографических характеристик и клинических исходов были проанализированы непрерывные переменные и категориальные переменные.Парный тест t использовали для определения того, существенно ли различаются среднее геометрическое титра нейтрализующих антител (GMT) (log2) или среднее геометрическое логарифмических трансформированных концентраций конкурентных антител (GMC) между образцами, полученными в остром периоде, и образцами, выздоравливающими. Тест с двумя образцами t был использован для определения того, значительно ли различаются концентрации нейтрализующих антител (log2) или GMC логарифмически трансформированных конкурентных антител у пациентов, инфицированных RSV/A и RSV/B, а также между реципиентами HCT, которые выделяют вирус. для < 14 и ≥ 14 дней.Статистическая значимость была указана для p значений <0,05. Коэффициенты корреляции Пирсона рассчитывали между титрами нейтрализующих антител и концентрациями сайт-специфических конкурентных антител. Статистический анализ проводили с использованием SPSS Statistic 22 (IBM, Armonk, NY).
Статистический анализ проводили с использованием SPSS Statistic 22 (IBM, Armonk, NY).
Результаты
Демографические и клинические показатели взрослых HCT, инфицированных RSV, были сопоставимы между исследовательскими группами
Клинические характеристики при включении суммированы для всех 40 взрослых HCT в таблице 1 из предыдущей публикации (29), стратифицированной по продолжительности выделения RSV (<14 или ≥14 дней) или по подтипу инфекции RSV (RSV/A или RSV/B). .Вкратце, все перечисленные переменные были сопоставимы между группами. Единственная наблюдаемая существенная разница заключалась в том, что реципиенты, которые выделяли РСВ в течение ≥14 дней, с большей вероятностью получали трансплантацию аллогенных стволовых клеток по сравнению с реципиентами с более короткой продолжительностью выделения вируса (18/20 против 11/20, p <0,025). ). Абсолютное количество нейтрофилов и абсолютное количество лимфоцитов находится в пределах нормы для этих когорт. Среднее время от трансплантации до заражения РСВ составляет 169 и 100 дней для взрослых, выделяющих РСВ из ВДП в течение <14 и ≥14 дней соответственно.
Среднее время от трансплантации до заражения РСВ составляет 169 и 100 дней для взрослых, выделяющих РСВ из ВДП в течение <14 и ≥14 дней соответственно.
Таблица 1 . Уровни антител к RSV в сыворотке пациентов с острым заболеванием и выздоравливающих от инфицированных RSV HCT взрослых.
Сайт-специфические анализы конкурентных антител были специфичны для соответствующих конкурентных антител
Специфичность четырех анализов конкурентных антител была подтверждена с использованием панели моноклональных антител (12,5 мкг/мл) для конкуренции с биотинилированными моноклональными антителами, специфичными к их соответствующим антигенным сайтам (рис. 1). Используя 125-кратно более высокую концентрацию, панель моноклональных антител, которые связывают антигенные сайты на белке F, отличные от сайта-мишени для биотинилированного моноклонального антитела, не были способны ингибировать связывание биотинилированного моноклонального антитела с его антигенным сайтом. Например, D25 ингибировал или конкурировал с биотинилированным D25 в анализе конкурентного антитела сайта Ø, в то время как остальные моноклональные антитела в панели не ингибировали связывание биотинилированного D25 с сайтом Ø.
Например, D25 ингибировал или конкурировал с биотинилированным D25 в анализе конкурентного антитела сайта Ø, в то время как остальные моноклональные антитела в панели не ингибировали связывание биотинилированного D25 с сайтом Ø.
Рисунок 1 . Специфичность анализов антигенных сайт-специфических конкурентных антител RSV. Синий цвет указывает на то, что mAb не ингибируют биотинилированные mAb, специфичные к антигенному участку RSV. Красный цвет указывает на сильное ингибирование антигенного сайта RSV.Шкала 0,0–1,5 представляет уровень ингибирования mAb от самого сильного до самого слабого. ПВЗ, паливизумаб; МВА, мотавизумаб. Представленные данные получены из 3 независимых параллельных конкурентных анализов антител.
Моноклональные антитела показали разные уровни нейтрализующей активности
Нейтрализующую активность моноклональных антител в концентрации 40 мкг/мл оценивали в тестах микронейтрализации RSV/A и RSV/B (рис. 2). МкАТ D25, которое связывается с антигенным сайтом Ø, является наиболее активным из МкАТ, используемых в конкурентных анализах антител. Паливизумаб и mAb 101F, которые связываются с сайтом II и сайтом IV, соответственно, обладают умеренной нейтрализующей активностью антител, а mAb 131-2A, сайт I, не обладает измеримой нейтрализующей активностью, что согласуется с ранее опубликованными результатами (34).
Паливизумаб и mAb 101F, которые связываются с сайтом II и сайтом IV, соответственно, обладают умеренной нейтрализующей активностью антител, а mAb 131-2A, сайт I, не обладает измеримой нейтрализующей активностью, что согласуется с ранее опубликованными результатами (34).
Рисунок 2 . Нейтрализующая активность антигенного сайт-специфического моноклонального антитела RSV. В экспериментах использовали RSV/A Tracy и RSV/B 18537. Концентрация mAb составляла 40 мкг/мл для D25, паливизумаба, 131-2A и 101F в анализах микронейтрализации как RSV/A, так и RSV/B, за исключением того, что mAb 131-2A использовали при 1.0 мг/мл в анализе микронейтрализации RSV/B. По оси Y отложены титры нейтрализующих антител RSV/A Tracy или RSV/B 18537 (log2) для различных mAb, используемых в анализе микронейтрализации. Представленные данные взяты из 3 независимых повторных анализов микронейтрализации ± стандартное отклонение.
Реконвалесцентная сыворотка содержала более высокую концентрацию сайт-специфического конкурирующего или нейтрализующего антитела, чем острая сыворотка
Значительное повышение уровней антител к РСВ (конкурентных и нейтрализующих антител) в сыворотке выздоравливающих по сравнению с сывороткой больных в остром периоде было измерено с помощью всех четырех анализов конкурентных антител и обоих анализов микронейтрализации (таблица 1).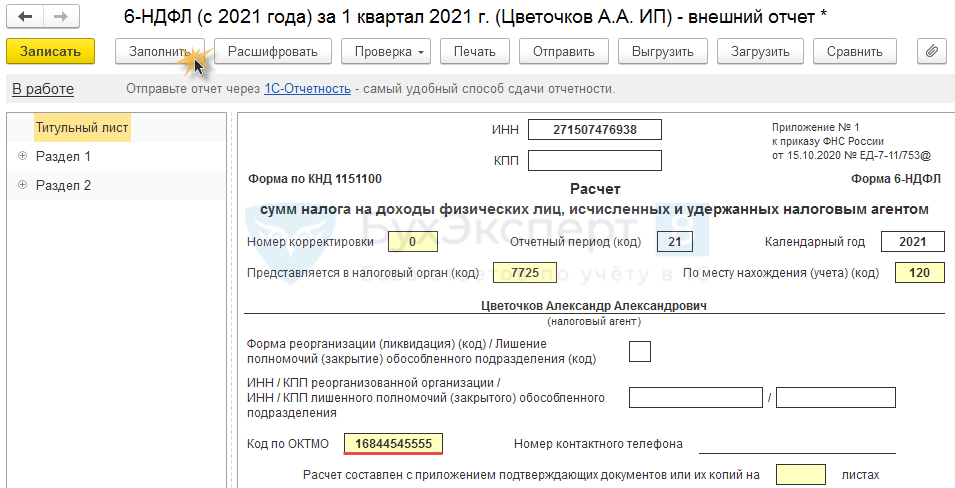 GMC антитела, конкурирующего с D25 (таблица 1), была самой высокой в сыворотке как в остром периоде, так и в сыворотке реконвалесцентов, за ним следуют антитело, конкурирующее с 101F (участок IV), антитело, конкурирующее с паливизумабом (участок II), и конкурирующее с 131-2A антитело (участок И) антитела. GMT нейтрализующих антител RSV/A и RSV/B были сопоставимы. Однако кратность увеличения концентрации конкурентных антител была наибольшей для конкурирующих с паливизумабом антител (5.6) и наименьшей для конкурирующих с D25 антител (2.6). Кратность увеличения была сопоставима между титрами нейтрализующих антител против RSV/A и RSV/B (6.5).
GMC антитела, конкурирующего с D25 (таблица 1), была самой высокой в сыворотке как в остром периоде, так и в сыворотке реконвалесцентов, за ним следуют антитело, конкурирующее с 101F (участок IV), антитело, конкурирующее с паливизумабом (участок II), и конкурирующее с 131-2A антитело (участок И) антитела. GMT нейтрализующих антител RSV/A и RSV/B были сопоставимы. Однако кратность увеличения концентрации конкурентных антител была наибольшей для конкурирующих с паливизумабом антител (5.6) и наименьшей для конкурирующих с D25 антител (2.6). Кратность увеличения была сопоставима между титрами нейтрализующих антител против RSV/A и RSV/B (6.5).
Более высокие уровни антител были обнаружены у взрослых HCT, выделяющих RSV
<14 дней Конкурентное антитело в GMC (мкг/мл) и нейтрализующее антитело в GMT (log2) сравнивали между взрослыми HCT, выделяющими вирус из их ВДП в течение <14 и ≥14 дней (таблица 2). Что касается острой сыворотки, не было существенной разницы между двумя группами ни для сайт-специфических конкурентных антител, ни для RSV-специфических нейтрализующих антител. Однако для выздоравливающих сывороток значительно более высокие уровни (<0.01) были обнаружены как сайт-специфические конкурентные антитела, так и РСВ-специфические нейтрализующие антитела у взрослых HCT, выделяющих РСВ <14 дней, за исключением сайта Ø конкурентного антитела. Кроме того, все сыворотки выздоравливающих имели более высокие уровни антител, чем сыворотки острых состояний, как для сайт-специфических конкурентных антител, так и для RSV-специфических нейтрализующих антител. Общая GMC для четырех конкурирующих антител в сыворотке выздоравливающих увеличилась примерно в 5 раз для взрослых HCT с выделением вируса <14 дней и примерно в 2 раза.5 раз для тех, кто выделяет вирус ≥14 дней. Для взрослых HCT, выделяющих вирус менее 14 дней, общая GMC четырех сайт-специфических антител увеличилась с 47,4 мкг/мл в сыворотке острого состояния до 228,6 мкг/мл в сыворотке выздоравливающих. Для взрослых HCT, выделяющих вирус ≥14 дней, общая GMC увеличилась с 34,1 мкг/мл в сыворотке острого периода до 91,8 мкг/мл в сыворотке выздоравливающих.
Однако для выздоравливающих сывороток значительно более высокие уровни (<0.01) были обнаружены как сайт-специфические конкурентные антитела, так и РСВ-специфические нейтрализующие антитела у взрослых HCT, выделяющих РСВ <14 дней, за исключением сайта Ø конкурентного антитела. Кроме того, все сыворотки выздоравливающих имели более высокие уровни антител, чем сыворотки острых состояний, как для сайт-специфических конкурентных антител, так и для RSV-специфических нейтрализующих антител. Общая GMC для четырех конкурирующих антител в сыворотке выздоравливающих увеличилась примерно в 5 раз для взрослых HCT с выделением вируса <14 дней и примерно в 2 раза.5 раз для тех, кто выделяет вирус ≥14 дней. Для взрослых HCT, выделяющих вирус менее 14 дней, общая GMC четырех сайт-специфических антител увеличилась с 47,4 мкг/мл в сыворотке острого состояния до 228,6 мкг/мл в сыворотке выздоравливающих. Для взрослых HCT, выделяющих вирус ≥14 дней, общая GMC увеличилась с 34,1 мкг/мл в сыворотке острого периода до 91,8 мкг/мл в сыворотке выздоравливающих.
Таблица 2 . Уровни антител к RSV между инфицированными RSV HCT взрослыми, которые выделяют RSV <14 дней и ≥14 дней.
Доля вклада GMC каждого сайт-специфического конкурентного антитела в общую GMC для сыворотки острой и реконвалесцентной сыворотки взрослых HCT, выделяющих вирус <14 дней и ≥14 дней, показана на рисунке 3.Для взрослых HCT, выделяющих вирус менее 14 дней, ~ 60% от общего GMC состоит из антител, конкурирующих с D25, и снижается до ~ 30% в сыворотке реконвалесцентов; в то время как процентное содержание 131-2A, антител, конкурирующих с паливизумабом, и антител, конкурирующих с 101F, увеличилось. Для взрослых HCT, выделяющих вирус ≥14 дней, ~ 70% от общего GMC также составляли D25-конкурирующие антитела в острой сыворотке, и процентный вклад четырех конкурирующих антител не увеличивался, даже несмотря на то, что общий GMC увеличился с 34.1 мкг/мл в острой сыворотке до 91,8 мкг/мл в выздоравливающей сыворотке.
Рисунок 3 . Процентное отношение GMC каждого антигенного сайт-специфического конкурентного антитела RSV (мкг/мл) к общему GMC (мкг/мл) для острых и выздоравливающих сывороток от взрослых HCT, выделяющих вирус <14 дней и ≥14 дней. Ось Y представляет собой процент GMC каждого конкурентного антитела от общего GMC. По оси X указаны типы сыворотки: острая или выздоравливающая сыворотка от взрослых HCT, выделяющих вирус <14 дней или ≥14 дней.Общая GMC представляла собой сумму 4 конкурентных GMC антител. Процентное содержание каждого конкурентного антитела было отношением GMC конкурентного антитела к общему GMC. GMC, средняя геометрическая концентрация. N = 40 в каждом конкурентном анализе антител.
Процентное отношение GMC каждого антигенного сайт-специфического конкурентного антитела RSV (мкг/мл) к общему GMC (мкг/мл) для острых и выздоравливающих сывороток от взрослых HCT, выделяющих вирус <14 дней и ≥14 дней. Ось Y представляет собой процент GMC каждого конкурентного антитела от общего GMC. По оси X указаны типы сыворотки: острая или выздоравливающая сыворотка от взрослых HCT, выделяющих вирус <14 дней или ≥14 дней.Общая GMC представляла собой сумму 4 конкурентных GMC антител. Процентное содержание каждого конкурентного антитела было отношением GMC конкурентного антитела к общему GMC. GMC, средняя геометрическая концентрация. N = 40 в каждом конкурентном анализе антител.
Значимых различий в уровнях антител в сыворотке больных и выздоравливающих между взрослыми HCT, инфицированными RSV/A, и RSV/B не наблюдалось
Сайт-специфические конкурентные антитела GMC и нейтрализующие антитела GMT сравнивали между взрослыми HCT, инфицированными RSV/A и RSV/B (таблица 3). Не наблюдалось существенных различий как в уровне нейтрализующих антител, так и в концентрациях сайт-специфических конкурентных антител в острой сыворотке и сыворотке выздоравливающих между взрослыми HCT, инфицированными RSV/A, по сравнению с RSV/B. Повышение активности антител было обнаружено в сыворотке выздоравливающих RSV/A и RSV/B инфицированных HCT взрослых с помощью всех 6 анализов. Кроме того, общая GMC 4 конкурирующих антител была сопоставима (133,6 против 159,9 мкг/мл) в сыворотке реконвалесцентов между RSV/A и RSV/B инфицированными HCT взрослыми.Это наблюдение согласуется с тем, что антигенные сайты II и IV хорошо сохраняются среди изолятов RSV в подгруппах RSV/A и RSV/B.
Не наблюдалось существенных различий как в уровне нейтрализующих антител, так и в концентрациях сайт-специфических конкурентных антител в острой сыворотке и сыворотке выздоравливающих между взрослыми HCT, инфицированными RSV/A, по сравнению с RSV/B. Повышение активности антител было обнаружено в сыворотке выздоравливающих RSV/A и RSV/B инфицированных HCT взрослых с помощью всех 6 анализов. Кроме того, общая GMC 4 конкурирующих антител была сопоставима (133,6 против 159,9 мкг/мл) в сыворотке реконвалесцентов между RSV/A и RSV/B инфицированными HCT взрослыми.Это наблюдение согласуется с тем, что антигенные сайты II и IV хорошо сохраняются среди изолятов RSV в подгруппах RSV/A и RSV/B.
Таблица 3 . Уровни антител к RSV между RSV/A и RSV/B инфицированными HCT взрослыми.
Доля вклада каждого сайт-специфического конкурентного антитела GMC в общий GMC для инфицированных RSV/A и B HCT взрослых показана на рисунке 4. D25-конкурирующие антитела составляют ~60% от общего GMC в острой сыворотке для как RSVA, так и B инфицировали взрослых HCT, и их количество снизилось до ~ 50% в сыворотке выздоравливающих; в то время как процентное содержание 131-2A, антител, конкурирующих с паливизумабом, и антител, конкурирующих с 101F, увеличилось в сыворотке выздоравливающих как у A, так и у B инфицированных HCT взрослых.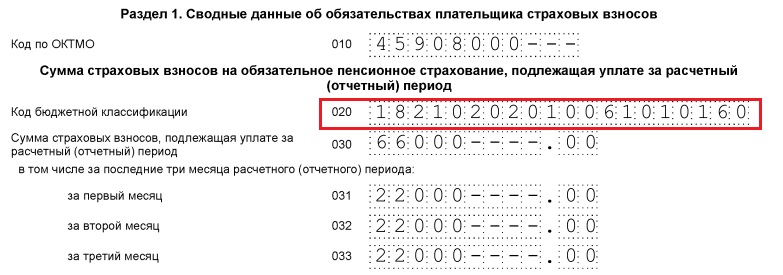
Рисунок 4 . Отношение GMC каждого сайт-специфического конкурентного антитела RSV (мкг/мл) к общему GMC (мкг/мл) для взрослых HCT, инфицированных RSV/A и B. GMC, средняя геометрическая концентрация. n = 40 в каждом конкурентном анализе антител.
Сайт-специфические конкурирующие антитела коррелируют с RSV-специфическими нейтрализующими антителами
Коэффициент корреляции Пирсона был рассчитан для измерения силы линейной связи между сайт-специфическими конкурентными антителами и специфичными нейтрализующими антителами к РСВ.Мы наблюдали значительную положительную корреляцию между сайт-специфическими конкурентными антителами, измеренными с помощью четырех анализов сайт-специфических конкурентных антител, и нейтрализующими антителами, измеренными с помощью анализов микронейтрализации RSV/A и RSV/B. Коэффициенты корреляции колебались от 0,33 до 0,83 для сывороток при острых состояниях и от 0,50 до 0,88 для сывороток выздоравливающих, при этом все корреляции были значимыми ( p <0,05) (рис.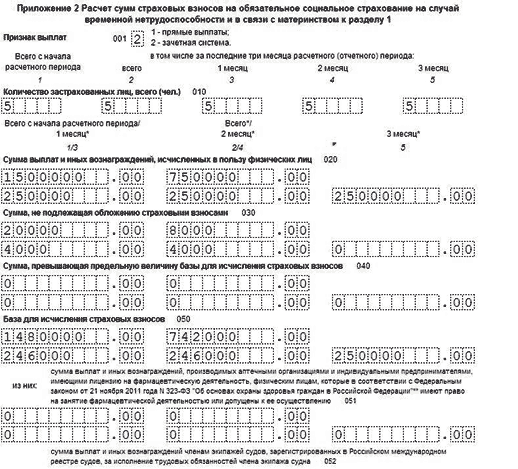 5). Самая высокая корреляция наблюдалась между концентрацией антител, конкурирующих с 101F, в сайте IV и титрами нейтрализующих антител к RSV, а самая низкая корреляция наблюдалась между концентрацией антител, конкурирующих с сайтом Ø D25, и титрами нейтрализующих антител к RSV у взрослых HCT, инфицированных RSV.
5). Самая высокая корреляция наблюдалась между концентрацией антител, конкурирующих с 101F, в сайте IV и титрами нейтрализующих антител к RSV, а самая низкая корреляция наблюдалась между концентрацией антител, конкурирующих с сайтом Ø D25, и титрами нейтрализующих антител к RSV у взрослых HCT, инфицированных RSV.
Рисунок 5 . Корреляция антигенного сайт-специфического конкурентного антитела РСВ и специфичного нейтрализующего антитела РСВ. Коэффициент корреляции Пирсона был рассчитан для измерения силы линейной связи. Коэффициенты корреляции колебались от 0,33 до 0,83 для острых сывороток и 0,50–0,88 для реконвалесцентных сывороток. *Корреляция значима на уровне 0,05 (двусторонняя). **Корреляция значима на уровне 0,01 (двусторонняя). n = 40 в каждом анализе конкурентных антител и анализе микронейтрализации.
Обсуждение
Глубокое понимание реакции антител человека на инфекцию RSV поможет в разработке и оценке вакцин и терапевтических средств против болезни RSV. В предыдущих исследованиях сообщалось об эпитопах, на которые нацелены специфичные к RSV нейтрализующие антитела в сыворотке человека (35, 36), а также сообщалось о специфичности и функциональных свойствах антител, вызванных естественной инфекцией RSV (17). Насколько нам известно, настоящее исследование является первым, в котором описаны сайт-специфические конкурентные ответы антител на пре-F и пост-F конформации и сопоставлены эти сайт-специфические конкурентные ответы антител с вирусным клиренсом и ответами нейтрализующих антител в естественно инфицированных RSV HCT. Взрослые.
В предыдущих исследованиях сообщалось об эпитопах, на которые нацелены специфичные к RSV нейтрализующие антитела в сыворотке человека (35, 36), а также сообщалось о специфичности и функциональных свойствах антител, вызванных естественной инфекцией RSV (17). Насколько нам известно, настоящее исследование является первым, в котором описаны сайт-специфические конкурентные ответы антител на пре-F и пост-F конформации и сопоставлены эти сайт-специфические конкурентные ответы антител с вирусным клиренсом и ответами нейтрализующих антител в естественно инфицированных RSV HCT. Взрослые.
В этом проспективном когортном исследовании конкурентные антитела пре-F и пост-F были выявлены после инфицирования RSV у взрослых HCT. Самая высокая концентрация сайт-специфических конкурентных антител в острой сыворотке была против сайта 0 в пре-F конформации, что согласуется с ранее опубликованными результатами, показывающими, что префузные F-специфические антитела преобладают в поликлональных нейтрализующих антисыворотках (36).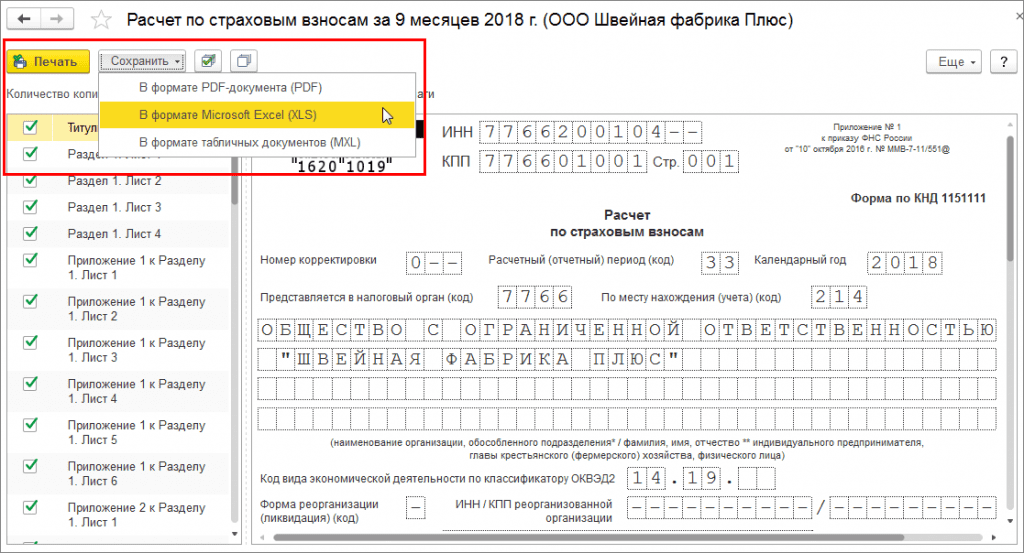 Однако высокие уровни специфичных к сайту Ø конкурентных антител, присутствующих в группе ≥14 дней, были неэффективны для элиминации вируса после установления вирусной инфекции.Нгвута и др. (36) использовали методы, основанные на абсорбции, для определения нейтрализующей активности, связанной с конформациями пре-F и пост-F, а также сайтом Ø и сайтом II. Наши анализы сайт-специфических конкурентных антител измеряли концентрации сайт-специфических конкурентных антител, но напрямую не демонстрировали нейтрализующую активность антигенных сайт-специфических конкурирующих антител. В целом, РСВ-специфические антитела играют важную роль в предотвращении инфекции и меньшую роль в элиминации вируса.В группе, которая избавилась от вируса менее чем за 14 дней, наблюдалась более сильная гуморальная реакция, вероятно, отражающая большее иммунологическое восстановление после трансплантации стволовых клеток. Хотя мы не измеряли клеточно-опосредованный иммунитет, весьма вероятно, что у этой группы также был более сильный клеточный иммунный ответ, который способствовал улучшению элиминации вируса.
Однако высокие уровни специфичных к сайту Ø конкурентных антител, присутствующих в группе ≥14 дней, были неэффективны для элиминации вируса после установления вирусной инфекции.Нгвута и др. (36) использовали методы, основанные на абсорбции, для определения нейтрализующей активности, связанной с конформациями пре-F и пост-F, а также сайтом Ø и сайтом II. Наши анализы сайт-специфических конкурентных антител измеряли концентрации сайт-специфических конкурентных антител, но напрямую не демонстрировали нейтрализующую активность антигенных сайт-специфических конкурирующих антител. В целом, РСВ-специфические антитела играют важную роль в предотвращении инфекции и меньшую роль в элиминации вируса.В группе, которая избавилась от вируса менее чем за 14 дней, наблюдалась более сильная гуморальная реакция, вероятно, отражающая большее иммунологическое восстановление после трансплантации стволовых клеток. Хотя мы не измеряли клеточно-опосредованный иммунитет, весьма вероятно, что у этой группы также был более сильный клеточный иммунный ответ, который способствовал улучшению элиминации вируса.
Сайт I имел самую низкую концентрацию конкурентных антител, что также согласуется с результатами, опубликованными Гилманом и другими (17, 37).Наибольшее кратное увеличение было обнаружено в отношении сайта II, что свидетельствует о том, что после инфицирования RSV иммунный ответ распознает другие антигенные сайты, которые не являются уникальными для пре-F формы. Это было продемонстрировано увеличением доли GMC конкурентных антител сайта II, сайта IV и сайта I, но не сайта Ø, к общему GMC в сыворотке реконвалесцентов взрослых HCT, которые быстро излечились от вирусной инфекции. Неясно, почему антитела, нацеленные на сайты, уникальные для пре-F формы, сохраняются дольше по сравнению с сайтами, общими для пре-F и пост-F форм.Важно отметить, что большинство конкурентных антител были направлены на сайт Ø в образцах острой сыворотки. Если бы аналогичное увеличение концентрации произошло в четырех антигенных участках в образцах сыворотки выздоравливающих, это привело бы к более высокому увеличению пропорции сайт-специфических конкурентных антител, которые имели более низкую концентрацию в образцах сыворотки при острых состояниях, таких как участки II и IV. Изменение доли сайт-специфических конкурентных антител усугублялось более высоким значением LLoD (7.8 мкг/мл) для анализа конкурентного антитела на клеточном сайте Ø, что было заметно выше по сравнению с LLoD (1,0 мкг/мл) для трех других конкурентных анализов антител.
Изменение доли сайт-специфических конкурентных антител усугублялось более высоким значением LLoD (7.8 мкг/мл) для анализа конкурентного антитела на клеточном сайте Ø, что было заметно выше по сравнению с LLoD (1,0 мкг/мл) для трех других конкурентных анализов антител.
Мы использовали корреляцию Пирсона для определения связи между четырьмя сайт-специфическими конкурентными антителами и между концентрациями сайт-специфических антител и титрами нейтрализующих антител. Самые высокие корреляции с уровнями нейтрализующих антител, специфичных для РСВ, наблюдались с конкурентными антителами сайтов II и IV.Эти результаты позволяют предположить, что антитела против паливизумаба и эпитопов 101F ответственны за значительную часть вируснейтрализующей способности сыворотки. Это также предполагает, что сайт-специфические анализы конкурентных антител измеряют изменения, которые непосредственно связаны с изменениями уровней нейтрализующих антител. Более низкая корреляция, обнаруженная между концентрациями конкурентных антител в антигенном сайте Ø и титрами нейтрализующих антител, может быть связана с тем, что антигенный сайт Ø является наименее консервативной областью по сравнению с другими антигенными сайтами в белке F (13, 38, 39), хотя это не анализировалось. в данном исследовании.Низкая корреляция также может быть связана с относительно высоким LLoD конкурентного анализа антител сайта Ø по сравнению с более низким LLoD для трех других анализов сайт-специфических конкурентных антител. Кроме того, небольшие изменения в концентрации конкурентного антитела к антигенному сайту Ø могут быть связаны с более значительными изменениями в активности нейтрализующих антител, что затрудняет обнаружение сильной корреляции из-за вариабельности анализа. Из четырех mAb, которые мы тестировали на активность нейтрализующих антител, mAb D25, нацеленное на сайт Ø, было наиболее эффективным из mAb, за ним следовали 101F и паливизумаб; 131-2A не проявляет нейтрализующей активности, что согласуется с тем, что сообщали Phung и другие (40).Эти различные активности нейтрализующих антител позволяют предположить, что сайты 0, II и IV являются основными мишенями ответа нейтрализующих антител человека, а антигенный сайт I не является основной мишенью. Интересно, что, хотя существовала сильная корреляция между концентрацией конкурентного антитела в сайте I и титрами специфичных к RSV нейтрализующих антител, mAb сайта I (131-2A) не обладало обнаруживаемой активностью нейтрализующего антитела.
в данном исследовании.Низкая корреляция также может быть связана с относительно высоким LLoD конкурентного анализа антител сайта Ø по сравнению с более низким LLoD для трех других анализов сайт-специфических конкурентных антител. Кроме того, небольшие изменения в концентрации конкурентного антитела к антигенному сайту Ø могут быть связаны с более значительными изменениями в активности нейтрализующих антител, что затрудняет обнаружение сильной корреляции из-за вариабельности анализа. Из четырех mAb, которые мы тестировали на активность нейтрализующих антител, mAb D25, нацеленное на сайт Ø, было наиболее эффективным из mAb, за ним следовали 101F и паливизумаб; 131-2A не проявляет нейтрализующей активности, что согласуется с тем, что сообщали Phung и другие (40).Эти различные активности нейтрализующих антител позволяют предположить, что сайты 0, II и IV являются основными мишенями ответа нейтрализующих антител человека, а антигенный сайт I не является основной мишенью. Интересно, что, хотя существовала сильная корреляция между концентрацией конкурентного антитела в сайте I и титрами специфичных к RSV нейтрализующих антител, mAb сайта I (131-2A) не обладало обнаруживаемой активностью нейтрализующего антитела. Наблюдаемая прямая корреляция, вероятно, отражает способность взрослых HCT вызывать эффективный гуморальный ответ на антигенные сайты на белке F, а не механистическую корреляцию между концентрацией конкурентных антител в сайте I и активностью нейтрализующих антител.
Наблюдаемая прямая корреляция, вероятно, отражает способность взрослых HCT вызывать эффективный гуморальный ответ на антигенные сайты на белке F, а не механистическую корреляцию между концентрацией конкурентных антител в сайте I и активностью нейтрализующих антител.
В этом проспективном когортном исследовании оценивалось влияние инфекции РСВ вирусными подгруппами (РСВ/А и РСВ/В) на гуморальный иммунный ответ на четыре антигенных сайта. Не наблюдалось существенных различий как в уровне нейтрализующих антител, так и в концентрациях сайт-специфических конкурентных антител, измеренных между реципиентами HCT, инфицированными RSV/A, по сравнению с RSV/B. Кроме того, пропорция и общая GMC четырех конкурирующих антител были сопоставимы в сыворотке выздоравливающих между взрослыми HCT, инфицированными RSV/A и RSV/B.Это наблюдение согласуется с тем, что антигенный сайт II и сайт IV хорошо консервативен между подгруппами RSV/A и RSV/B, и предполагает, что моновалентная вакцина RSV-F против инфекции RSV/A и RSV/B, вероятно, достаточна для защиты от тяжелой формы RSV. болезнь.
болезнь.
Наше исследование имеет некоторые ограничения. Небольшое число инфицированных РСВ взрослых с НСТ ( n = 40) не является репрезентативным для взрослых в общей популяции. Более высокий рост концентрации конкурентных антител и титра нейтрализующих антител после инфицирования RSV может наблюдаться у здоровых взрослых по сравнению со взрослыми HCT.Кроме того, мы не измеряли концентрацию конкурентных антител к сайту III и сайту V, оставшимся антигенным сайтам пре-F. Таким образом, их вклад в активность нейтрализующих антител после инфекции RSV не был определен в этой когорте взрослых HCT, инфицированных RSV.
Таким образом, исследование выявило значительно более высокие концентрации сайт-специфических конкурентных антител в F RSV (за исключением сайта Ø) у взрослых HCT, которые выделили RSV <14 дней, по сравнению с ≥14 дней, сопоставимые концентрации конкурентных антител в сыворотке выздоравливающих между RSV /A и RSV/B инфицированных HCT взрослых, а также значительную положительную корреляцию между сайт-специфическими конкурентными антителами и активностью RSV-специфических нейтрализующих антител. В заключение, у взрослых HCT, инфицированных RSV естественным путем, сайт-специфические конкурентные гуморальные ответы возникали на антигенные сайты, обнаруженные как в конформациях F до слияния, так и после слияния, и были связаны с клиренсом вируса. Данные могут предполагать, но не демонстрируют, что эти реакции антител способствуют наблюдаемому более быстрому клиренсу вируса. Более быстрый клиренс у людей с более высоким ответом антител может просто отражать уровень иммунной компетентности этих людей.Следовательно, наблюдаемая связь между более высоким ответом антител и более быстрым клиренсом не обязательно является причиной и следствием. Кроме того, необходима дальнейшая оценка того, как ответы, опосредованные Т-клетками, способствуют элиминации вируса РСВ. Наконец, реципиенты HCT, вероятно, выиграют от иммунопрофилактики моноклональными антителами или вакцины RSV-F, если они лицензированы для предотвращения тяжелой инфекции RSV в период их уязвимости после трансплантации.
В заключение, у взрослых HCT, инфицированных RSV естественным путем, сайт-специфические конкурентные гуморальные ответы возникали на антигенные сайты, обнаруженные как в конформациях F до слияния, так и после слияния, и были связаны с клиренсом вируса. Данные могут предполагать, но не демонстрируют, что эти реакции антител способствуют наблюдаемому более быстрому клиренсу вируса. Более быстрый клиренс у людей с более высоким ответом антител может просто отражать уровень иммунной компетентности этих людей.Следовательно, наблюдаемая связь между более высоким ответом антител и более быстрым клиренсом не обязательно является причиной и следствием. Кроме того, необходима дальнейшая оценка того, как ответы, опосредованные Т-клетками, способствуют элиминации вируса РСВ. Наконец, реципиенты HCT, вероятно, выиграют от иммунопрофилактики моноклональными антителами или вакцины RSV-F, если они лицензированы для предотвращения тяжелой инфекции RSV в период их уязвимости после трансплантации.
Доступность данных
Наборы данных, созданные для этого исследования, доступны по запросу соответствующему автору.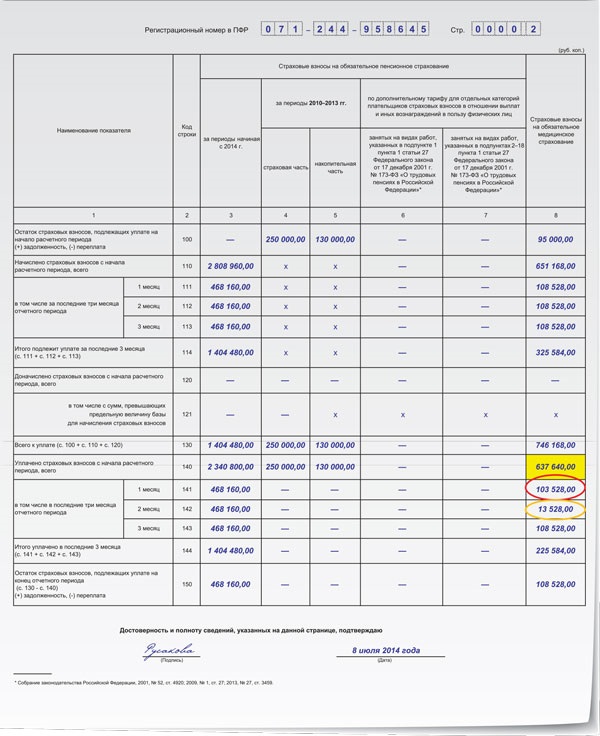
Заявление об этике
Это исследование было проведено в соответствии с рекомендациями институциональных наблюдательных советов Онкологического центра им. М. Д. Андерсона Техасского университета и Медицинского колледжа Бейлора с письменного информированного согласия всех субъектов. Все субъекты дали письменное информированное согласие в соответствии с Хельсинкской декларацией. Протокол был одобрен Онкологическим центром им. М.Д. Андерсона Техасского университета и Медицинским колледжем Бэйлора.
Вклад авторов
XY, RC и PP разработали исследование.XY, OI, VA, LA, TM и PP провели исследование. XY, LF-S и PP проанализировали данные. DS и RC предоставили образцы. КП обрабатывал образцы. F-AP, VA, LA, TM, LF-S, KP, DS, RC и PP редактировали текст. XY написал первый черновик рукописи.
Заявление о конфликте интересов
Авторы заявляют, что исследование проводилось при отсутствии каких-либо коммерческих или финансовых отношений, которые могли бы быть истолкованы как потенциальный конфликт интересов.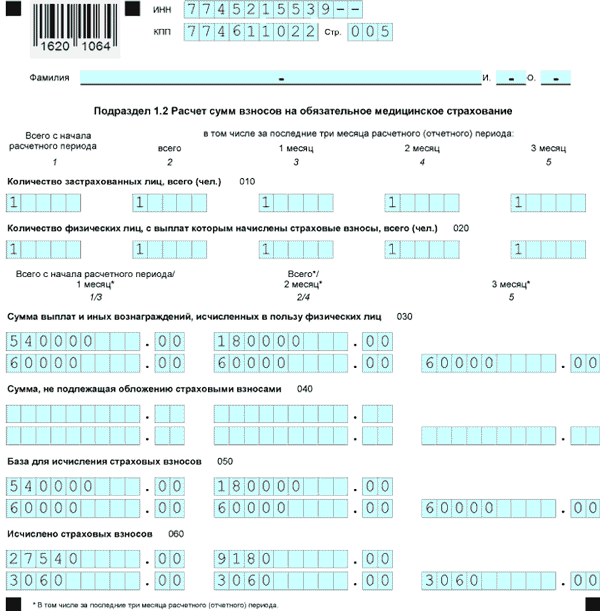
Благодарности
Авторы выражают признательность Dr.Barney S Graham, MD Ph.D (Лаборатория вирусного патогенеза, NIAID/VRC, NIH Bethesda, MD) за предоставление этих mAb D25 и AM14 против антигенных сайтов во время разработки анализа. Авторы признают вклад рецензентов в улучшение качества оформления рукописи. Авторы признают возможность устно представить данные на 11-м Международном симпозиуме по респираторно-синцитиальным вирусам в 2018 году в Эшвилле, Северная Каролина, США.
Ссылки
1. Choi JH, Choi EH, Kang HJ, Park KD, Park SS, Shin HY и др.Респираторные вирусные инфекции после трансплантации гемопоэтических стволовых клеток у детей. J Korean Med Sci. (2013) 28:36–41. doi: 10.3346/jkms.2013.28.1.36
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
2. Lo MS, Lee GM, Gunawardane N, Burchett SK, Lachenauer CS, Lehmann LE. Воздействие RSV, аденовируса, гриппа и парагриппозной инфекции на педиатрических пациентов, получающих трансплантацию стволовых клеток, солидных органов или химиотерапию рака. Детская трансплантация .(2013) 17:133–43. doi: 10.1111/petr.12022
Детская трансплантация .(2013) 17:133–43. doi: 10.1111/petr.12022
Полнотекстовая перекрестная ссылка | Академия Google
3. Анак С., Атай Д., Унувар А., Гарипардич М., Агаоглу Л., Озтюрк Г. и соавт. Вспышка респираторно-синцитиальной вирусной инфекции среди детей с онкологическими заболеваниями и/или ТКМ. Детский пульмонол. (2010) 45:307–11. doi: 10.1002/стр.21184
Полнотекстовая перекрестная ссылка | Академия Google
4. Asner S, Stephens D, Pedulla P, Richardson SE, Robinson J, Allen U. Факторы риска и исходы инфекций, связанных с респираторно-синцитиальным вирусом, у детей с ослабленным иммунитетом. Pediatr Infect Dis J . (2013) 32:1073–6. дои: 10.1097/INF.0b013e31829dff4d
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
6. Kim HW, Canchola JG, Brandt CD, Pyles G, Chanock RM, Jensen K, et al. Респираторно-синцитиальное вирусное заболевание у детей раннего возраста, несмотря на предшествующее введение антигенной инактивированной вакцины.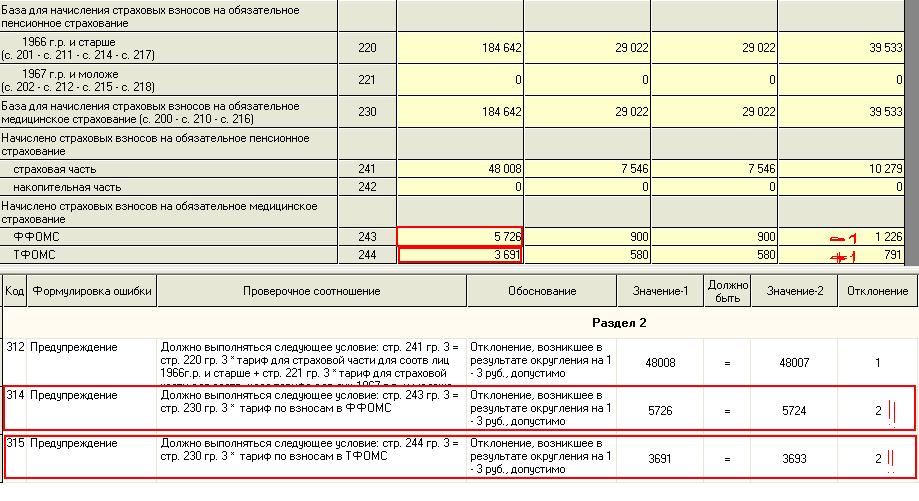 Am J Эпидемиол. (1969) 89:422–34.
Am J Эпидемиол. (1969) 89:422–34.
Реферат PubMed | Академия Google
7. Муньос Ф.М., Пьедра П.А., Глезен В.П.Безопасность и иммуногенность очищенной вакцины слитого белка-2 респираторно-синцитиального вируса у беременных женщин. Вакцина . (2003) 21:3465–7. doi: 10.1016/S0264-410X(03)00352-9
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
8. Wright PF, Karron RA, Belshe RB, Shi JR, Randolph VB, Collins PL, et al. Отсутствие обострения заболевания респираторно-синцитиальной вирусной инфекцией дикого типа, возникающего после введения живых, аттенуированных, респираторно-синцитиальных вирусных вакцин. Вакцина . (2007) 25:7372–8. doi: 10.1016/j.vaccine.2007.08.014
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
9. Ложно А.Р., Уолш Э.Е. Респираторно-синцитиальная вирусная инфекция у взрослых. Clin Microbiol Rev. (2000) 13:371–84. doi: 10.1128/CMR.13.3.371
Полнотекстовая перекрестная ссылка | Академия Google
10. Шиффер И.Т., Кирби К., Санмайер Б., Сторб Р., Кори Л., Бекх М. Сроки и тяжесть внебольничных респираторных вирусных инфекций при миелоаблативной и немиелоаблативной трансплантации гемопоэтических стволовых клеток. Гематологические. (2009) 94:1101–8. doi: 10.3324/гематол.2008.003186
Шиффер И.Т., Кирби К., Санмайер Б., Сторб Р., Кори Л., Бекх М. Сроки и тяжесть внебольничных респираторных вирусных инфекций при миелоаблативной и немиелоаблативной трансплантации гемопоэтических стволовых клеток. Гематологические. (2009) 94:1101–8. doi: 10.3324/гематол.2008.003186
Полнотекстовая перекрестная ссылка | Академия Google
11. Ljungman P, Ward KN, Crooks BN, Parker A, Martino R, Shaw PJ, et al. Респираторные вирусные инфекции после трансплантации стволовых клеток: проспективное исследование рабочей группы по инфекционным заболеваниям европейской группы по трансплантации крови и костного мозга. Пересадка костного мозга. (2001) 28:479–84. doi: 10.1038/sj.bmt.1703139
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
13.McLellan JS, Chen M, Leung S, Graepel KW, Du X, Yang Y и др. Структура тримера слитого гликопротеина RSV, связанного со специфичным для слияния нейтрализующим антителом. Наука. (2013) 340:1113–7. doi: 10.1126/наука.1234914
doi: 10.1126/наука.1234914
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
14. Андерсон Дж.Дж., Норден Дж., Сондерс Д., Томс Г.Л., Скотт Р. Анализ местных и системных иммунных ответов, индуцированных у мышей BALB/c экспериментальной респираторно-синцитиальной вирусной инфекцией. Дж Ген Вирол. (1990) 71 (часть 7): 1561–70.
Реферат PubMed | Академия Google
15. Sastre P, Melero JA, García-Barreno B, Palomo C. Сравнение аффинной хроматографии и адсорбции на рекомбинантных инфицированных клетках вируса коровьей оспы для истощения антител, направленных против гликопротеинов респираторно-синцитиального вируса, присутствующих в препарате иммуноглобулина человека. J Med Virol. (2005) 76: 248–55. doi: 10.1002/jmv.20349
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
16.Корти Д., Бьянки С., Ванцетта Ф., Минола А., Перес Л., Агатик Г. и др. Перекрестная нейтрализация четырех парамиксовирусов человеческим моноклональным антителом. Природа. (2013) 501:439–43. doi: 10.1038/nature12442
Природа. (2013) 501:439–43. doi: 10.1038/nature12442
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
17. Gilman MS, Castellanos CA, Chen M, Ngwuta JO, Goodwin E, Moin SM, et al. Быстрое профилирование репертуара антител RSV из В-клеток памяти естественно инфицированных взрослых доноров. Научная иммунол. (2016) 1:eaaj1879.doi: 10.1126/sciimmunol.aaj1879
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
18. Mousa JJ, Kose N, Matta P, Gilchuk P, Crowe JE Jr. Новый конформационно-специфический нейтрализующий эпитоп перед слиянием на слитом белке респираторно-синцитиального вируса. Нат. микробиол. (2017) 2:16271. doi: 10.1038/nmicrobiol.2016.271
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
19. Фишаут М., Туберген Д., Макинтош К. Клеточный ответ на респираторные вирусы с особым упором на детей с нарушениями клеточно-опосредованного иммунитета. J Педиатр. (1980) 96:179–86. doi: 10.1016/S0022-3476(80)80799-2
J Педиатр. (1980) 96:179–86. doi: 10.1016/S0022-3476(80)80799-2
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
20. Hall CB, Powell KR, MacDonald NE, Gala CL, Menegus ME, Suffin SC, et al. Респираторно-синцитиальная вирусная инфекция у детей с ослабленной иммунной функцией. N Engl J Med. (1986) 315:77–81. дои: 10.1056/NEJM198607103150201
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
21. Bangham CR, Cannon MJ, Karzon DT, Askonas BA.Цитотоксический Т-клеточный ответ на респираторно-синцитиальный вирус у мышей. Дж Вирол. (1985) 56:55–9.
Реферат PubMed | Академия Google
22. Кэннон М.Дж., Опеншоу П.Дж., Асконас Б.А. Цитотоксические Т-клетки элиминируют вирус, но усиливают патологию легких у мышей, инфицированных респираторно-синцитиальным вирусом. J Exp Med. (1988) 168:1163–8. doi: 10.1084/jem.168.3.1163
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
23. Тейлор Г., Стотт Э.Дж., Хейл А.Дж.Цитотоксические лимфоциты в легких мышей, инфицированных респираторно-синцитиальным вирусом. Дж Ген Вирол. (1985) 66 (часть 12): 2533–8. дои: 10.1099/0022-1317-66-12-2533
Тейлор Г., Стотт Э.Дж., Хейл А.Дж.Цитотоксические лимфоциты в легких мышей, инфицированных респираторно-синцитиальным вирусом. Дж Ген Вирол. (1985) 66 (часть 12): 2533–8. дои: 10.1099/0022-1317-66-12-2533
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
24. Чиба Ю., Хигашидате Ю., Суга К., Хондзё К., Цуцуми Х., Огра П.Л. Развитие клеточно-опосредованного цитотоксического иммунитета к респираторно-синцитиальному вирусу у младенцев после естественной инфекции. J Med Virol. (1989) 28:133–9.doi: 10.1002/jmv.18
304
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
25. Исаакс Д., Бэнгэм К.Р., МакМайкл А.Дж. Клеточно-опосредованный цитотоксический ответ на респираторно-синцитиальный вирус у детей раннего возраста с бронхиолитом. Ланцет . (1987) 2:769–71. doi: 10.1016/S0140-6736(87)92502-5
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
26. Russell CD, Unger SA, Walton M, Schwarze J. Иммунный ответ человека на инфекцию респираторно-синцитиального вируса. Clin Microbiol Rev. (2017) 30:481–502. doi: 10.1128/CMR.00090-16
Иммунный ответ человека на инфекцию респираторно-синцитиального вируса. Clin Microbiol Rev. (2017) 30:481–502. doi: 10.1128/CMR.00090-16
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
27. Кутсая А., Терос-Яаккола Т., Каккола Л., Тойвонен Л., Пелтола В., Варис М. и соавт. Проспективное клинико-серологическое наблюдение в раннем детстве выявляет высокую частоту субклинической РСВ-инфекции и относительно высокую частоту реинфекции в течение первых 3 лет жизни. Эпидемиол Инфекция. (2016) 144:1622–33. дои: 10.1017/S0950268815003143
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
28.Холл CB, Уолш EE, Лонг CE, Шнабель KC. Иммунитет к и частота реинфекции респираторно-синцитиальным вирусом. J Инфиц. дис. (1991) 163:693–8. doi: 10.1093/infdis/163.4.693
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
29. Ye X, Iwuchukwu OP, Avadhanula V, Aideyan LO, McBride TJ, Ferlic-Stark LL, Piedra PA. Сравнение связывания паливизумаб-подобных антител с различными конформациями белка F RSV у инфицированных RSV взрослых реципиентов гемопоэтических клеток. J Инфиц. дис. (2018) 217:1247–56. doi: 10.1093/infdis/jiy026
Сравнение связывания паливизумаб-подобных антител с различными конформациями белка F RSV у инфицированных RSV взрослых реципиентов гемопоэтических клеток. J Инфиц. дис. (2018) 217:1247–56. doi: 10.1093/infdis/jiy026
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
30. Авадханула В., Чемали Р.Ф., Шах Д.П., Гантоджи С.С., Аззи Дж.М., Айдеян Л.О. и соавт. Инфекция новым респираторно-синцитиальным вирусом генотипа Онтарио (ON1) у взрослых реципиентов трансплантата гемопоэтических клеток, Техас, 2011–2013 гг. J Инфиц. дис. (2015) 211:582–9. дои: 10.1093/infdis/jiu473
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
31.Пьедра П.А., Уайд П.Р., Каслман В.Л., Амброуз М.В., Джуэлл А.М., Спилман Д.Дж. и др. Усиление легочной патологии, связанное с применением инактивированной формалином респираторно-синцитиальной вирусной вакцины у хлопчатобумажных крыс, не является уникальным вирусным феноменом. Вакцина. (1993) 11:1415–23. дои: 10.1016/0264-410X(93)
(1993) 11:1415–23. дои: 10.1016/0264-410X(93)
-3
Полнотекстовая перекрестная ссылка | Академия Google
32. Пьедра П.А., Грейс С., Джуэлл А., Спинелли С., Бантинг Д., Хогерман Д.А. и соавт. Вакцина на основе очищенного слитого белка защищает от заболеваний нижних дыхательных путей во время сезона респираторно-синцитиального вируса у детей с муковисцидозом. Pediatr Infect Dis J . (1996) 15:23–31. дои: 10.1097/00006454-199601000-00006
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
33. Piedra PA, Hause AM, Aideyan L. Респираторно-синцитиальный вирус (RSV): нейтрализующие антитела, коррелят иммунной защиты. Методы Мол Биол. (2016) 1442:77–91. дои: 10.1007/978-1-4939-3687-8_7
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
34. Goodwin E, Gilman MSA, Wrapp D, Chen M, Ngwuta JO, Moin SM, et al.Младенцы, инфицированные респираторно-синцитиальным вирусом, продуцируют мощные нейтрализующие антитела, в которых отсутствует соматическая гипермутация. Иммунитет. (2018) 48:339–349.e5. doi: 10.1016/j.immuni.2018.01.005
Иммунитет. (2018) 48:339–349.e5. doi: 10.1016/j.immuni.2018.01.005
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
35. Магро М., Мас В., Чаппелл К., Васкес М., Кано О., Луке Д. и соавт. Нейтрализующие антитела против преактивной формы слитого белка респираторно-синцитиального вируса открывают уникальные возможности для клинического вмешательства. Proc Natl Acad Sci USA. (2012) 109:3089–94. doi: 10.1073/pnas.1115941109
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
36. Ngwuta JO, Chen M, Modjarrad K, Joyce MG, Kanekiyo M, Kumar A, et al. F-специфические антитела перед слиянием определяют величину нейтрализующей активности РСВ в сыворотке крови человека. Sci Transl Med. (2015) 7:309ra162. doi: 10.1126/scitranslmed.aac4241
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
37.Widjaja I, Wicht O, Luytjes W, Leenhouts K, Rottier PJM, van Kuppeveld FJM и др. Характеристика ответов антител против эпитоп-специфического антиреспираторно-синцитиального вируса (анти-RSV) после естественной инфекции и после вакцинации инактивированным формалином RSV. Дж Вирол. (2016) 90:5965–77. doi: 10.1128/ОВИ.00235-16
Характеристика ответов антител против эпитоп-специфического антиреспираторно-синцитиального вируса (анти-RSV) после естественной инфекции и после вакцинации инактивированным формалином RSV. Дж Вирол. (2016) 90:5965–77. doi: 10.1128/ОВИ.00235-16
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
38. Nichols WG, Gooley T, Boeckh M. Внебольничные инфекции респираторно-синцитиального вируса и вируса парагриппа после трансплантации гемопоэтических стволовых клеток: опыт Исследовательского центра рака Фреда Хатчинсона. Трансплантация костного мозга Биол . (2001) 7 (Прил.): 11S−15S. doi: 10.1053/bbmt.2001.v7.pm11777098
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
39. Коннор А.Л., Бевитт Д.Дж., Томс Г.Л. Сравнение последовательностей генов респираторно-синцитиального вируса А2 человека и слитого гликопротеина 8/60 и картирование эпитопов антител, специфичных для подгруппы. Дж Мед Вирол .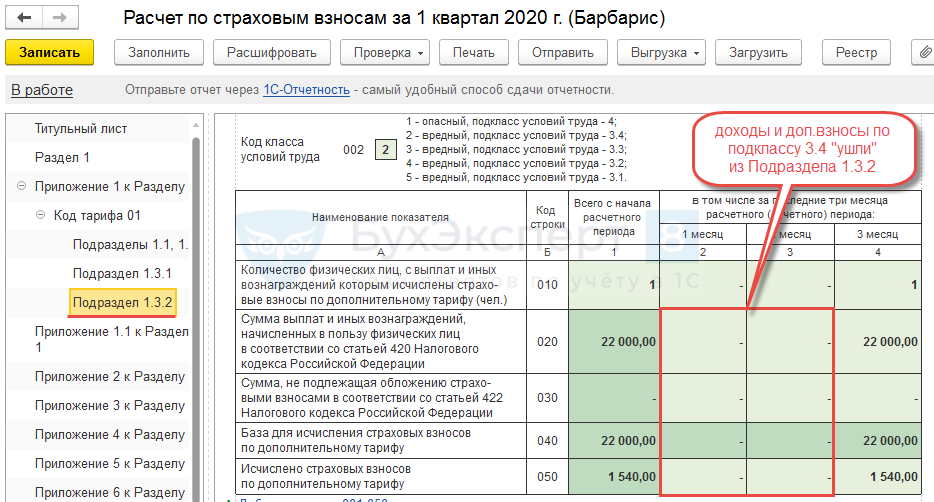 (2001) 63:168–77. doi: 10.1002/1096-9071(20000201)63:2<168::AID-JMV1012>3.0.CO;2-U
(2001) 63:168–77. doi: 10.1002/1096-9071(20000201)63:2<168::AID-JMV1012>3.0.CO;2-U
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
40.Phung E, Chang LA, Morabito KM, Kanekiyo M, Chen M, Nair D, et al. Эпитоп-специфические серологические анализы RSV: вопросы конформации. Вакцины . (2019) 7:E23. doi: 10.3390/vaccines7010023
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
Смертность и госпитализации, связанные с гриппом и респираторно-синцитиальным вирусом
Почти ежегодно вирус гриппа становится причиной большого числа смертей и госпитализаций 1–3, особенно среди пожилых людей и людей с заболеваниями высокого риска.Поэтому большинство стран рекомендуют вакцинацию против гриппа для этих групп 4. Недавно в США вакцинация была распространена на детей в возрасте 50–64 лет и детей младшего возраста с низким уровнем риска, а в Канаде была введена вакцинация для всех возрастов 5, 6. Многие европейские страны в настоящее время рассматривается вопрос о расширении рекомендаций по вакцинации против гриппа. Однако необходима дополнительная информация о потенциальном воздействии таких изменений в политике вакцинации. В частности, мало данных о госпитализации в связи с гриппом среди взрослых с низким риском7.
Трудно точно оценить нагрузку на здравоохранение, связанную с гриппом, поскольку инфекции, вызванные вирусом гриппа, обычно не подтверждаются вирусологически и часто не распознаются клинически 8, 9. Кроме того, инфекция, вызванная вирусом гриппа, может предрасполагать к другим состояниям, таким как бактериальная суперинфекция и сердечно-сосудистые осложнения 10–12. Совместная циркуляция других респираторных вирусов во время сезона гриппа, в частности респираторно-синцитиального вируса (RSV) 13, затрудняет косвенную оценку бремени, связанного с гриппом.Несколько исследований показали, что РСВ вызывает значительную заболеваемость и даже смертность не только у детей, но и у пожилых людей 2, 14–16. За последние 10 лет разработка вакцин против РСВ продвинулась вперед 17 , и хотя вакцина не ожидается в ближайшем будущем, было бы полезно получить представление о бремени, связанном с РСВ, для здравоохранения.
В отличие от предыдущих исследований 3, 7, данные эпиднадзора за вирусами в Нидерландах за 1997–2003 гг. выявили в основном отдельные пики активности вируса гриппа и РСВ, что позволило количественно оценить влияние обоих вирусов по отдельности.Цель настоящего исследования состояла в том, чтобы оценить смертность и госпитализацию, связанные с гриппом и РСВ, особенно бремя, связанное с гриппом, среди лиц с низким уровнем риска в возрасте ≤65 лет.
МЕТОДЫ
Вирусный надзор
В период 1997–2003 гг. лабораторный эпиднадзор за различными вирусами проводился системой Weekly Sentinel голландской рабочей группы по клинической вирусологии в Нидерландах. Группа из 17 вирусологических лабораторий еженедельно отчитывалась об абсолютном количестве пациентов, госпитализированных или посещающих поликлиники, у которых был положительный результат на определенный вирус.В настоящем исследовании использовались данные эпиднадзора за вирусом гриппа и РСВ из этой системы. Большинство лабораторных диагнозов инфекций, вызванных вирусом гриппа и РСВ, были поставлены путем выделения вируса на клеточной культуре или экспресс-тестов на антигены. Было продемонстрировано, что еженедельные вирусологические отчеты адекватно отражают тенденции национальной вирусной активности 18. Однако большинство данных эпиднадзора за РСВ (96%) были зарегистрированы у детей в возрасте до 5 лет 19. Подтип вируса гриппа считался доминирующим, когда на его долю приходилось ≥50% всех изолятов, которые были подтипированы в том сезоне.Данные эпиднадзора за вирусами гриппа и RSV обобщены в таблице 1⇓. Все сезоны гриппа были доминантными по h4N2 подтипа А, за исключением 2000–2001 гг., когда доминировал подтип А по h2N1.
Определение периодов обучения
С небольшими изменениями периоды исследования были определены в соответствии с Izurieta et al. 20. Для каждого зимнего сезона, с 40-й недели 1 года до 20-й недели следующего года, период активности вируса гриппа определялся как период продолжительностью не менее двух недель подряд, в течение которых на каждую неделю приходилось ≥5% сезонной активности. общее число лабораторно подтвержденных случаев гриппа 20.Точно так же период активности RSV был определен как период продолжительностью не менее 2 последовательных недель, в течение которых на каждую неделю приходилось ≥5% от общего числа пациентов с положительным результатом на RSV за сезон. Период с преобладанием гриппа определяли как недели активности вируса гриппа с <5% от общего числа положительных тестов на РСВ-20 за сезон. Перисезонный базовый период определяли как периоды продолжительностью не менее двух недель подряд в течение 40–40 недель. 20, в которых на каждую неделю приходилось <5% от общего числа случаев гриппа и РСВ-положительных случаев за сезон.Летний базовый период был определен как 21–39 неделя. В отличие от исследования Izurieta et al. 20, недели, в течение которых был выделен вирус парагриппа, не были исключены из исследования, поскольку в течение года сообщалось о (спорадических) изолятах. По той же причине из исследования не исключались недели, в течение которых в летний базовый период регистрировались спорадические изоляты вируса гриппа и РСВ.
В течение периода исследования было 92 недели активности гриппа и/или РСВ; 46 недель преобладания гриппа, 42 недели преобладания RSV и только 4 недели активности как вируса гриппа, так и активности RSV.
Данные о смертности и исходы
Национальные еженедельные данные о смертности были получены из Статистического управления Нидерландов (Ворбург/Херлен, Нидерланды). На этих рисунках не было информации о наличии состояний высокого риска. Еженедельные показатели госпитализации были предоставлены Prismant (Институт здравоохранения и консультирования, Утрехт, Нидерланды), который регистрирует все госпитализации по всей стране в соответствии с Международной классификацией болезней-9CM.В этом регистре были зарегистрированы все диагнозы при выписке из расчета на одну госпитализацию, причем первый диагноз был помечен как первичный. За исследуемый период все госпитализации с выпиской с диагнозом острого заболевания верхних дыхательных путей (460–465, 381–384, 034), острого или хронического заболевания нижних дыхательных путей (466, 480–487, 490–496, 510–518, 78609, 7862), сердечно-сосудистые заболевания (410–415, 420–422, 428–429, 7852), цереброваскулярные заболевания (431–437), бактериальные инвазивные заболевания (036, 038, 041, 320, 3220, 3229, 7280, 7907) или были собраны другие состояния, возможно связанные с респираторной инфекцией (293, 323, 390-392, 3483, 7803, 7806, 7784).Госпитализация была разделена на инфекции верхних дыхательных путей (ИВДП), инфекции нижних дыхательных путей (ИНДП) и заболевания легких, сердечно-сосудистые осложнения (ССО) и другие ( например, бактериально-инвазивное заболевание, бесочаговая лихорадка и делирий). Кроме диагноза при выписке регистрировали дату госпитализации, возраст и наличие состояний высокого риска. Состояние высокого риска считалось присутствующим, когда хотя бы один из 14 субдиагнозов указывал на хроническое заболевание органов дыхания (491–496, 500–508, 516–518, 5199, 71481), хроническое заболевание сердца (391, 393–396, 402, 404, 410–412, 414, 416, 424–429, 745–747), сахарный диабет (250–251), почечная недостаточность (581–591), гематологические злокачественные новообразования (2031, 2038, 204–208) или ВИЧ/СПИД (042–044).Когда хроническое сердечное или респираторное заболевание было отмечено как первичный диагноз при выписке, это также рассматривалось как наличие состояния высокого риска.
Статистический анализ
Население каждого года подряд на 1 января считалось населением, подверженным риску, при условии стабильного населения в течение года (Статистическое управление Нидерландов). За все годы вместе взятые рассчитаны средненедельная смертность и частота госпитализаций (на 100 000 человек) в разные периоды исследования, т.е.е. перисезонных и летних исходных периода и периодов, в которых преобладали вирусы гриппа или РСВ. Еженедельная избыточная смертность и госпитализации с 95% доверительными интервалами (ДИ), связанные с вирусом гриппа и РСВ, определялись путем вычитания летних и перисезонных исходных показателей из показателей в периоды преобладания вируса гриппа или РСВ. Кумулятивный годовой коэффициент избыточной активности в зимний период представлял собой общую избыточную активность на 100 000 субъектов, связанных с вирусом гриппа или РСВ в течение зимнего сезона, и рассчитывался путем умножения среднего недельного показателя избыточной активности в течение периода преобладания гриппа на количество недель активности вируса гриппа в течение этой зимы. время года.Коэффициенты превышения применялись к населению страны в 2005 г. (Статистическое управление Нидерландов) для оценки общего числа смертей и госпитализаций, связанных с вирусом гриппа и РСВ в Нидерландах. Доля населения с высоким риском заболевания, , т.е. заболеваний, которые связаны с более высоким риском осложненных инфекций, вызванных вирусом гриппа, была получена из Национальной информационной сети первичной медицинской помощи 21. Поскольку распространенность заболеваний высокого риска среди детей был относительно низким, анализ подмножеств в зависимости от наличия заболеваний высокого риска среди детей не проводился.Анализ подмножества в зависимости от наличия заболевания высокого риска также не проводился для субъектов в возрасте ≥ = 65 лет, поскольку этим субъектам уже рекомендована вакцинация против гриппа.
РЕЗУЛЬТАТЫ
Всего зарегистрировано 839 303 смерти от всех причин и 1 551 598 госпитализаций по поводу ОРВИ, ИНДП, ЦВК и других. Из этих смертей от всех причин 1% был зарегистрирован в возрасте 0–17 лет, 6% — в возрасте 18–49 лет, 13% — в возрасте 50–64 лет и 80% — в возрасте ≥65 лет. . Для госпитализаций эти цифры составили 14, 12, 23 и 51% соответственно.
Грипп
В возрастных категориях 0–1, 2–17 и 18–49 лет в периоды активности вируса гриппа не было обнаружено явного повышения смертности (таблица 2⇓). Однако среди лиц в возрасте ≥ 50 лет была зарегистрирована значительная избыточная смертность, связанная с гриппом. Среди лиц в возрасте 50–64 лет избыточная смертность, связанная с гриппом, была самой высокой в возрасте 60–64 лет (рис. 1⇓). Связанная с гриппом избыточная госпитализация была самой высокой среди детей в возрасте 0–1 года (таблица 3⇓). Младенцы, по-видимому, ответственны за наибольшую часть этой избыточной госпитализации по поводу ИНДП, а именно в среднем за год примерно 13–221 госпитализаций на 100 000 младенцев в возрасте до 1 года (соответственно с перисезонным и летним базовым периодом) и 13–221 госпитализаций на 100 000 младенцев в возрасте до 1 года. 64 госпитализации на 100 000 детей в возрасте 1 года.У взрослых значительное превышение госпитализаций по поводу ИНДП и ЦВК регистрировалось в течение недель активности вируса гриппа (таблица 4⇓). Превышения по всем категориям диагноза увеличивались с возрастом и увеличивались среди лиц 50–64 лет из группы низкого риска (рис. 2⇓). В абсолютных цифрах самая высокая нагрузка на здравоохранение, связанная с гриппом, приходилась на пожилых людей (рис. 3⇓).
РСВ
В период активности РСВ не было обнаружено явной избыточной смертности в возрастных категориях 0–1, 2–17 и 18–49 лет (таблица 2⇓).Самые маленькие дети, по-видимому, испытали наибольшую избыточную госпитализацию, связанную с РСВ, по поводу ИНДП (таблица 3⇓), со средним годовым числом госпитализаций ~870–1063 на 100 000 детей в возрасте до 1 года (с соответственно перисезонным и летним исходным периодом в качестве эталона). ) и 104–151 на 100 000 детей в возрасте 1 года. Значительная избыточная госпитализация была зарегистрирована у взрослых в течение РСВ-активных периодов, особенно у пожилых людей (таблица 4⇓). Общее абсолютное число избыточных госпитализаций, связанных с РСВ, было самым высоким и примерно одинаковым среди детей в возрасте 0–1 года и пожилых людей (рис.4⇓).
ОБСУЖДЕНИЕ
Это общенациональное ретроспективное исследование, охватывающее шесть недавних последовательных респираторных сезонов, показало, что смертность, связанная с гриппом, была значительной среди лиц в возрасте ≥50 лет. Госпитализация по поводу гриппа была значимой среди здоровых лиц всех возрастных категорий и наиболее высокой среди детей раннего возраста и пожилых людей. Самая высокая избыточная госпитализация, связанная с РСВ, также наблюдалась в самой молодой возрастной группе, но также была значительной у пожилых людей, у которых периоды активности РСВ также были связаны с повышенной смертностью.
Описано множество моделей для оценки бремени, связанного с гриппом, и большинство из них основано на определении избыточной частоты в периоды активности вируса гриппа по сравнению с исходными периодами с более низкой активностью вируса гриппа или без нее. Модель «скорость-разница» регулярно применялась 7, 20, 22, а также прямой вариант этих моделей, обеспечивающий понимание широкой публики. Из-за использования различных статистических моделей, в том числе различных определений вирусных сезонов и различных определений конечных точек ( e.г. культурально подтвержденный или неподтвержденный грипп), исследования трудно сравнивать 1–3, 7, 9, 20, 22–28. Различия в включенном периоде исследования (и, следовательно, различная активность вируса гриппа) и различия в системах здравоохранения также приводят к плохой сопоставимости, например, первичная помощь в Нидерландах с функцией контроля входа может повлиять на частоту госпитализаций.
В отличие от предыдущих исследований 2, 26, в которых сообщалось о ежегодных смертях, связанных с гриппом, 2–7 на 100 000 среди детей в возрасте 0–1 года и ∼1 на 100 000 среди детей в возрасте 1–4 лет, современные авторы не смогли выявить повышенную смертность среди детей в периоды активности вируса гриппа.Существующим методам может не хватать чувствительности для выявления небольшого превышения числа смертей, связанных с гриппом. Тем не менее, текущее исследование подтвердило, что среди детей и лиц в возрасте 18–64 лет, не имеющих заболеваний высокого риска, самая высокая избыточная госпитализация, связанная с гриппом, приходится на самых маленьких детей 3, 9, 20, 22–25 лет. Это говорит о том, что эта целевая группа может получить особую пользу от вакцинации против гриппа, особенно если принять во внимание связанные с гриппом обращения за первичной медико-санитарной помощью и невыходы родителей на работу 28.Кроме того, также считается, что дети являются основными распространителями гриппа 29, и поэтому вакцинация детей может ограничить распространение инфекции в обществе. Однако вакцина против гриппа в настоящее время не лицензирована для детей в возрасте до 6 месяцев, и данные об эффективности и действенности вакцины у детей в возрасте до 2 лет ограничены 30.
Настоящее исследование показывает, что периоды активности вируса гриппа были связаны с повышенной смертностью среди лиц в возрасте 50–64 лет.К сожалению, исследование не смогло оценить, какая часть этого превышения имела место у лиц с низким уровнем риска, поскольку информация о статусе риска не была доступна в цифрах смертности. Однако госпитализация, связанная с гриппом, была значительной среди лиц в возрасте 50–64 лет из группы низкого риска. Недавнее исследование не смогло продемонстрировать госпитализацию, связанную с гриппом, в этой группе, но это, вероятно, было связано с ограниченной статистической мощностью 7. Показатели госпитализации, обнаруженные в текущем исследовании среди лиц в возрасте 50–64 лет с низким уровнем риска, были явно ниже, чем у маленьких детей, но характер госпитализаций также может иметь значение.В то время как у детей избыточная госпитализация была в основном связана с респираторными заболеваниями, госпитализации по поводу CVC составляли наибольшую часть избыточной госпитализации среди 50-64-летних. Очевидно, что ожидается, что эти госпитализации окажут большое влияние на систему здравоохранения и финансовые ресурсы. Как избыточная смертность, связанная с гриппом, так и госпитализация, в частности по поводу CVC, увеличивались с возрастом, что указывает на то, что ежегодная вакцинация против гриппа принесет наибольшую пользу людям в возрасте 60–64 лет. Вакцина против гриппа доказала свою безопасность и эффективность среди взрослых, а также показала свою эффективность в предотвращении сердечно-сосудистых осложнений 31–34.Помимо потенциальной пользы для здоровья, анализ экономической эффективности с учетом как прямых, так и косвенных затрат, связанных с гриппом, таких как невыход на работу, важен для принятия решений об изменении политики вакцинации.
Несмотря на высокий охват вакцинацией против гриппа среди пожилых людей в Нидерландах (70–80%), в настоящем исследовании смертность, связанная с гриппом, оказалась высокой среди пожилых людей. Однако известно, что иммуногенность противогриппозной вакцины снижается с возрастом после 65 лет, что может привести к снижению эффективности 31, 35.Это подчеркивает необходимость дальнейшего улучшения защиты от гриппа, особенно у пожилых людей.
Как и ожидалось, самая высокая избыточная госпитализация, связанная с РСВ, наблюдалась в самой молодой возрастной группе 36, 37 лет, и это бремя оказалось значительно выше, чем бремя, связанное с гриппом. Связанную с РСВ смертность в этой возрастной категории показать не удалось. В связи с теми же проблемами мощности, что и связанная с гриппом смертность среди детей раннего возраста в текущем исследовании, нельзя исключить возможность смертности, связанной с РСВ, в этой возрастной категории.Предыдущие исследования сообщали о ежегодной смертности, связанной с РСВ, 5–8 случаев на 100 000 среди детей в возрасте 0–12 месяцев и примерно 1 случай на 100 000 среди детей в возрасте от 1 до 4 лет 2, 26. Значительная избыточная госпитализация также была продемонстрирована среди взрослых, особенно среди пожилой. Более того, РСВ-активные периоды оказались связаны с повышенной смертностью среди лиц в возрасте 50–64 лет и пожилых людей. Основные госпитализации, связанные с РСВ, были связаны с респираторными показаниями и, в меньшей степени, с CVC по сравнению с госпитализацией, связанной с гриппом, что согласуется с предыдущим исследованием 25.
Однако, чтобы оценить результаты настоящего исследования, необходимо обсудить некоторые аспекты. Поскольку для оценки бремени, связанного с гриппом и РСВ, использовались эпидемиологические данные, прямых доказательств в отношении возбудителя, который привел к госпитализации или смерти, не было. Поэтому результаты следует интерпретировать с осторожностью. Бремя, однако, будет недооценено только регистрацией лабораторно подтвержденных случаев гриппа и РСВ-инфекции из-за неполной диагностики и занижения отчетности, а также в случае вторичных осложнений (таких как бактериальные инфекции или другие возможные осложнения, такие как сердечно-сосудистые заболевания).Кроме того, вирус гриппа является широко изученным патогеном, который, как известно, является причиной значительной ежегодной заболеваемости и смертности. Напротив, роль РСВ в возникновении заболеваемости и смертности, особенно среди взрослых, менее ясна. В текущем исследовании была обнаружена явная избыточная смертность и заболеваемость в течение активных периодов РСВ. Тем не менее, большая часть современных данных эпиднадзора за РСВ была зарегистрирована у детей, и хотя авторы настоящего исследования предположили, что активность РСВ у взрослых аналогична таковой у детей, это еще не было должным образом доказано [38].Поэтому возможно, что некоторые из РСВ- и связанных с гриппом заболеваемости могли быть неправильно классифицированы, как и во всех других избыточных исследованиях. Это подчеркивает важность возрастного эпиднадзора за РСВ и должно быть рассмотрено в будущих исследованиях.
Оценки бремени, связанного с вирусом, сильно зависят от используемого базисного периода, поэтому оценки следует рассматривать с довольно большими погрешностями. Перисезонный базовый период является наиболее консервативным ориентиром, и его применение, вероятно, привело к недооценке бремени, связанного с вирусом, поскольку показатели превышения определяются в течение периодов, когда вирус гриппа и РСВ активны, хотя и в меньшей степени (недели с <5% от общего количества изолятов за сезон).И наоборот, потенциальная роль других респираторных вирусов или других сезонных факторов, таких как определенные метеорологические условия, влияющие на частоту госпитализаций и смертность, ограничена перисезонным базовым периодом в качестве контрольного. Другими словами, применяя перисезонный базовый период в качестве эталона, авторы настоящей статьи попытались скорректировать другие потенциально важные сезонные факторы. Таким образом, представляется, что истинная избыточная смертность и госпитализация, связанные с гриппом и РСВ, вероятно, находятся в пределах оценок, основанных на перисезонном и летнем базовом периоде.Тем не менее ожидается, что другие вирусы, такие как риновирусы и коронавирусы, вызывают более легкие клинические проявления респираторных инфекций, которые требуют обращения за первичной медицинской помощью. Кроме того, данные эпиднадзора в Нидерландах в течение текущего периода исследования показали, что риновирусы, аденовирусы и вирусы парагриппа, по-видимому, не имеют четкой сезонной картины, как вирусы гриппа и RSV, с довольно длительными периодами незначительного повышения активности или очень короткими пиками повышенной активности. (смотри Приложение).К сожалению, сезонный характер некоторых недавно открытых коронавирусов и метапневмовируса человека нельзя было оценить, поскольку в период исследования не было данных эпиднадзора.
Основным преимуществом настоящего исследования является включение большого числа пациентов по всей стране, что позволяет проводить субанализ в зависимости от возраста и наличия состояний с высоким риском госпитализации среди взрослых. Поскольку Нидерланды являются небольшой, но густонаселенной страной, характеристики населения относительно однородны по всей стране, а циркуляция вирусов по всей стране более или менее одновременна, что делает экологические исследования более надежными.Кроме того, период исследования охватывал 6 лет с различной частотой вирусных атак.
Таким образом, среди детей в возрасте 0–4 лет была обнаружена значительная избыточная госпитализация, связанная с гриппом, хотя смертность не могла быть связана с гриппом в этой возрастной группе. Среди лиц в возрасте 50–64 лет с низким уровнем риска также была зарегистрирована значительная избыточная госпитализация, связанная с гриппом, и, по-видимому, присутствовала даже избыточная смертность. Часть этого бремени можно было бы предотвратить путем введения ежегодной вакцинации против гриппа.Бремя, связанное с респираторно-синцитиальным вирусом, оказалось значительным, особенно у детей младшего возраста, но также и у пожилых людей, и поэтому роль будущей вакцины против респираторно-синцитиального вируса представляется многообещающей в снижении этого бремени для здравоохранения.
Структурная основа нейтрализации новым антителом с сайтом II/IV против слитого белка респираторно-синцитиального вируса
Abstract
Во всем мире респираторно-синцитиальный вирус человека (RSV) является ведущей причиной инфекций нижних дыхательных путей у новорожденных, детей младшего возраста и пожилых людей, против которых не существует вакцины.Гликопротеин слияния (F) RSV является основной мишенью для разработки вакцин. Здесь мы описываем новое моноклональное антитело (обозначенное как R4.C6), которое распознает F RSV как до, так и после слияния, и связывается с наномолярным сродством к уникальному сайту нейтрализации, состоящему из антигенных сайтов II и IV на глобулярной головке. Структура комплекса RSV F-R4.C6 Fab с разрешением 3,9 Å была получена с помощью криоэлектронной микроскопии отдельных частиц и трехмерной реконструкции. Структура раскрыла подробные взаимодействия R4.C6 с антигенным сайтом II на одном протомере и сайтом IV на соседнем протомере пост-слитого белка F RSV. Эти результаты значительно расширяют наше понимание антигенной сложности F-белка и позволяют по-новому взглянуть на дизайн вакцин против RSV.
Образец цитирования: Xie Q, Wang Z, Ni F, Chen X, Ma J, Patel N, et al. (2019)Структурная основа нейтрализации новым антителом сайта II/IV против слитого белка респираторно-синцитиального вируса. ПЛОС ОДИН 14(2): е0210749.https://doi.org/10.1371/journal.pone.0210749
Редактор: Стивен М. Варга, Университет Айовы, США
Поступила в редакцию: 17 сентября 2018 г.; Принято: 30 декабря 2018 г.; Опубликовано: 7 февраля 2019 г.
Авторское право: © 2019 Xie et al. Это статья с открытым доступом, распространяемая в соответствии с условиями лицензии Creative Commons Attribution License, которая разрешает неограниченное использование, распространение и воспроизведение на любом носителе при условии указания автора и источника.
Доступность данных: Крио-ЭМ карта и модель RSV F-R4.C6 Fab после слияния были депонированы в EMDB под кодом доступа EMD-7774 и в банке данных белков под кодом доступа 6CXC.
Финансирование: Q.W. признает поддержку по контракту с Novavax, Inc. и гранты от Национальных институтов здравоохранения (R01-GM127628, R01-GM116280) и Фонда Уэлча (Q-1826). JM благодарит за поддержку Национальные институты здравоохранения (R01-GM127628, R01-GM116280) и Фонд Уэлча (Q-1512).З.В. благодаря поддержке Welch Foundation (Q-1967). Ф.Н. был частично поддержан для постдокторских учебных стипендий от Центра Кека Учебной программы по вычислительной биологии рака Консорциумов побережья Мексиканского залива (финансируется грантом CPRIT № RP101489). Ядро Cryo-EM ATC финансируется Медицинским колледжем Бэйлора. Спонсоры не участвовали в разработке исследования, сборе и анализе данных, принятии решения о публикации или подготовке рукописи.
Конкурирующие интересы: Авторы ознакомились с политикой журнала и имеют следующие конфликты: NP, HL, YL, JHT, DF, MJM, LE, GG и GS являются нынешними или бывшими сотрудниками Novavax, Inc., а также владеть или держать опционы на акции. Нет никаких патентов, продуктов в разработке или продаваемых продуктов, которые нужно декларировать. Это не меняет нашей приверженности всем политикам PLOS ONE в отношении обмена данными и материалами.
Введение
Респираторно-синцитиальный вирус человека (RSV) является основной причиной пневмонии и бронхиолита у недоношенных новорожденных, детей младшего возраста и взрослых старше 65 лет. В Соединенных Штатах РСВ ежегодно является причиной более 2 миллионов амбулаторных посещений и почти 60 000 госпитализаций детей в возрасте до 5 лет и 11 000–17 000 смертей у взрослых [1–3].Во всем мире РСВ является причиной более 30 миллионов инфекций нижних дыхательных путей (ИНДП), 3 миллионов госпитализаций и 50 000–75 000 смертей ежегодно у детей в возрасте до 5 лет, причем большинство случаев приходится на развивающиеся страны [4–6]. На сегодняшний день не существует утвержденной вакцины против РСВ, а паливизумаб (Синагис) является единственным средством пассивной профилактики, одобренным для предотвращения инфекции РСВ у новорожденных в возрасте до 24 месяцев. Однако высокая стоимость и 5-дозовый режим лечения препятствуют использованию и доступности паливизумаба в развивающихся странах [7–9].
RSV человека представляет собой оболочечный РНК-вирус и член семейства Pneumoviridae , состоящего из подгрупп RSV/A и RSV/B [10–15]. Геном RSV представляет собой РНК с отрицательной цепью из 15 килобаз, которая кодирует 11 структурных и неструктурных белков. На поверхности вируса обнаруживаются три структурных белка: малый гидрофобный (SH) белок представляет собой пентамерный ионный канал; прикрепление (G) гликопротеина опосредует прикрепление вирусной частицы к бронхиальному эпителию; а слитый (F) гликопротеин опосредует слияние вирусной оболочки с мембраной хозяина, обеспечивая доставку вирусного генома в клетку [16, 17].
Гликопротеины G и F являются мишенями иммунного ответа хозяина. G-белок сильно гликозилирован, при этом более 60% его массы в 90 килодальтон (кДа) состоит из углеводов. Гликопротеины G гетерогенны с ограниченной гомологией последовательностей (53%) и небольшой антигенной перекрестной реактивностью между двумя подгруппами [18-21]. Напротив, последовательности гликопротеина F хорошо консервативны (> 90%) с высокой степенью перекрестной антигенной реактивности между подгруппами [22]. Следовательно, гликопротеин F был основной мишенью для разработки вакцин.
Гликопротеин F RSV человека первоначально синтезируют в виде одноцепочечного полипептида из 574 остатков (F0) с молекулярной массой ~70 кДа. F0 содержит два фуриноподобных сайта расщепления по остаткам 109 и 136. Расщепление обоих фуриновых сайтов на F0 необходимо для его инфекционности [23]. Двойное расщепление приводит к удалению промежуточного пептида из 27 остатков (пептид p27), образуя N-концевой фрагмент F2 (~ 20 кДа) и более крупный С-концевой фрагмент F1 (~ 48 кДа), которые ковалентно связаны двумя дисульфидные связи.Фрагмент F1 содержит гидрофобный слитый пептид (FP) на N-конце и гидрофобный трансмембранный домен (TM) и цитоплазматический хвост (CT) на C-конце. Фрагмент F2 имеет два гликана в остатках N27 и N70, а фрагмент F1 имеет один гликан в остатке N500. Субъединица F2-F1 самоассоциируется с образованием тримеров, которые закрепляются на вирусной оболочке посредством домена TM на F1. Сопровождая цикл вирусной инфекции, гликопротеин F претерпевает значительную однонаправленную перестройку из конформации до слияния в стабильную конформацию после слияния, облегчая слияние вирусной оболочки с мембраной хозяина [17].
Антитела, нейтрализующие вирусRSV, впервые были зарегистрированы более 30 лет назад [24], и широко распространено мнение, что они коррелируют с защитой от тяжелых инфекций нижних дыхательных путей [25]. Гуманизированное моноклональное антитело (мАт) паливизумаб в настоящее время является единственным иммунопрофилактическим средством, одобренным для лечения новорожденных с повышенным риском тяжелой инфекции [8, 26]. С тех пор кристаллические структуры гликопротеина F в конформациях до и после слияния в комплексе с mAb мыши и человека привели к идентификации и точному картированию ряда антигенных эпитопов [27, 28].Антигенный сайт II расположен на фрагменте F1, охватывающем аминокислотные остатки 254–278, который далее классифицируется как антигенный сайт IIa, распознаваемый нейтрализующими mAb паливизумабом и hRSV14N4, и антигенный сайт IIb, на который нацелены мотавизумаб и hRSV3J20 [29, 30]. Однако, учитывая тот факт, что мотавизумаб представляет собой вариант паливизумаба с созревшей аффинностью [31], подробные различия их эпитопов не могут быть очерчены без структур высокого разрешения этих mAb с RSV F. Кроме того, ненейтрализующие mAb человека (4B6, 9J5 и 12I1) связываются с антигенным сайтом II в положении, отличном от паливизумаба и мотавизумаба.Этот ненейтрализующий эпитоп был обозначен как антигенный сайт VII [30]. Антигенный сайт IV является еще одним нейтрализующим эпитопом, также расположенным на F1 и охватывающим остатки 422–471 [27]. МкАТ, нейтрализующие сайт IV, включают 101F [29, 32, 33] и гуманизированный RSHZ19 [34]. Эпитопы сайтов II, IV и VII консервативны между подгруппами RSV и присутствуют как в конформациях до слияния, так и в конформациях после слияния [33, 35]. Потенциальные нейтрализующие эпитопы также были идентифицированы и картированы в конформации перед слиянием F RSV.Нулевой антигенный сайт (Ø) является мишенью mAb человека D25 и AM22 [36] и мышиного 5C4 [17]. Эпитоп сайта Ø консервативен в подгруппе RSV/A и менее консервативен в подгруппе RSV/B [14].
Здесь мы представляем создание и характеристику ряда новых мышиных mAb, полученных с использованием наночастиц RSV F (NP). Интересно, что мы идентифицировали новое mAb, обозначенное как R4.C6, которое распознает F RSV как до, так и после слияния, и связывается с наномольным сродством к ранее неизвестному нейтрализующему эпитопу, расположенному в промежуточном положении между антигенными сайтами II и IV в Фрагмент F1.Криоэлектронную микроскопию отдельных частиц (крио-ЭМ) и трехмерную реконструкцию использовали для определения фрагмента антигенсвязывающей области (Fab) R4.C6 в комплексе с гликопротеином F после слияния RSV с разрешением 3,9 Å. Критическая информация о структуре нового нейтрализующего эпитопа, распознаваемого R4.C6, может помочь в разработке вакцины и дать понимание прогрессивных структурных изменений, которым подвергается белок F в процессе инфицирования RSV.
Результаты
Получение и характеристика mAb
мАт, специфичных к RSV F, были созданы с использованием модифицированных стандартных методов [37] у мышей BALB/c, иммунизированных RSV F NP [38].Для характеристики были отобраны четыре гибридомы, продуцирующие специфические mAb к RSV F. МкАТ были обозначены как R6.29 и R1.42 (подкласс IgG1), R4.C6 IgG2a и R6.46 IgG3 (таблица 1).
Аффинность связывания антител с RSV F NP и пептидом антигенного сайта II (остатки 254–278) определяли методом поверхностного плазмонного резонанса (SPR) с использованием прибора Biacore T200. R4.C6 связывал RSV F NP с K D = 0,07 нМ, что было в 7 раз выше, чем у паливизумаба ( K D = 0.51 нМ) и сравнимо с мотавизумабом ( K D = 0,04 нМ). R4.C6 связывал пептид сайта II (остатки 254–278) с K D = 12,5 нМ, что в 30 раз больше, чем у паливизумаба ( K D = 370 нМ), и сравнимо с мотавизумабом (39 D = 370 нМ). K D = 26,7 нМ). Кроме того, R6.46, R6.29 и R1.42 связывали RSV F NP с K D в концентрации 0,04–3,21 нМ. R6.46 также связывал пептид сайта II ( K D = 442 нМ), в то время как R1.42 и R6.29 не связывались (таблица 1, рис. S1).
Анализ нейтрализации вирусаиспользовали для определения нейтрализующей активности этих mAb. R4.C6 и R6.46 нейтрализовали RSV/A Long с IC 50 = 1078 и 727 нг/мл соответственно, что было немного выше, чем у паливизумаба (IC 50 = 323 нг/мл). MAb R1.42 обладало самой сильной нейтрализующей активностью из всех новых mAb, выявленных в этом исследовании (IC 50 = 19,6 нг/мл), которая была в 15 раз выше, чем у паливизумаба, и сходна с мотавизумабом (IC 50 = 19,6 нг/мл). 20.8 нг/мл). R6.29 не смог нейтрализовать RSV/A Long (IC 50 >10 мкг/мл) (таблица 1).
Биннинг эпитопов моноклональных антител с помощью биослойной интерферометрии (BLI)
Для дальнейшей характеристики антигенных сайтов, связанных с этими mAb, биннинг эпитопов был выполнен с помощью BLI с использованием системы Octet QK384. Помеченный гистидином RSV F710 после слияния был иммобилизован на наконечниках биосенсора против пентагистидина. Захваченный RSV F710 подвергали воздействию отдельных mAb в два этапа для определения конкуренции. Паливизумаб и RSV14N4 (участок IIa), мотавизумаб и RSV3J20 (участок IIb) и RSHZ19 (участок IV) использовали в качестве контролей для определения различных антигенных участков.
Антитела R6.29 и R6.46 конкурировали за связывание антител, специфичных к сайту IIa и сайту IIb (рис. 1А). Хотя оба антитела были специфичны к сайту II с одинаковой аффинностью связывания с RSV F NP ( K D 1,59 нМ и 3,21 нМ соответственно), было обнаружено, что R6.46 нейтрализует RSV/A Long и связывается с пептидом сайта II, в то время как R6.29 не обладал измеримой нейтрализующей активностью и не связывался с пептидом сайта II (таблица 1), что свидетельствует о том, что эти mAb связывались с сайтом II по-разному.Свойства R6.29 были аналогичны ненейтрализующим антителам, специфичным к сайту II, эпитоп которых недавно был обозначен как антигенный сайт VII [30]. Относительно более слабая нейтрализующая активность R6.46 сближала его с паливизумабом (участок IIa). С другой стороны, R1.42 конкурировал за связывание с RSVZ19, что указывает на то, что эти антитела нацелены на антигенный сайт IV (рис. 1А).
Рис. 1. Биннинг эпитопов и связывание mAb с F-гликопротеином RSV.
(A) Биннинг эпитопов для связывания mAb с RSF F710 после слияния.Перекрестную конкуренцию антител определяли с помощью BLI с использованием системы Octet QK384. Помеченный гистидином белок RSV F710 после слияния был иммобилизован на наконечниках биосенсора против пентагистидина. Данные показывают процент связывания конкурирующего второго антитела в присутствии первого антитела по сравнению с одним конкурирующим антителом. Черные клетки указывают на полную конкуренцию (процент связывания от 0% до 33%), светло-серые клетки указывают на промежуточное завершение (процент связывания от 34% до 60%), а темно-серые клетки указывают на отсутствие конкуренции (процент связывания >60%).Желтые клетки указывают на самоконкуренцию. Антигенные сайты IIa/IIb, VII, IV и II/IV обозначены сверху и сбоку окрашенными клетками. Клетки, обведенные красным, указывают на конкуренцию R4.C6 с антигенными сайт-специфическими контрольными антителами паливизумабом и RSV14N4 (участок IIa), мотавизумабом и RSV3J20 (участок IIb), R6.29 (участок VII), R1.42 и RSVZ19 (участок IV). Паливизумаб (Pali), мотавизумаб (Mota), не определено (n.d.). (B) Связывание mAb с RSV F NP после слияния и до слияния. Процент (%) связывания определяли с помощью BLI с использованием системы Octet QK384, относящейся к связыванию мАт F RSV с NP F RSV, F после слияния или F до слияния.Светло-серые клетки указывают на сильное связывание, темно-серые клетки указывают на промежуточное связывание, а черные клетки указывают на отсутствие связывания. (C) Кинетика связывания mAb с RSV F NP, после слияния и до слияния. K D : Константа кажущейся равновесной диссоциации рассчитывается как k d / k a ; k a : коэффициент ассоциации из кривых ассоциации; k d : скорость диссоциации по кривым диссоциации. Также см. рис. S2 для сенсограмм.
https://doi.org/10.1371/journal.pone.0210749.g001
Интересно, что R4.C6 в целом конкурировал за связывание антител, нацеленных на антигенный сайт IIa (паливизумаб, RSV14N4 и R6.46), сайт IIb (мотавизумаб и RSV3J20). ), сайт IV (RSHZ19 и R1.42) и ненейтрализующий сайт VII (R6.29) (рис. 1А). Эти результаты свидетельствуют о том, что R4.C6 однозначно распознает ранее неопределенный эпитоп, охватывающий нейтрализующие антигенные сайты IIa/b и IV и ненейтрализующий сайт VII.
Антигенный сайт II и сайт IV присутствуют как до, так и после слияния RSV F.Используя систему Octet QK384 на основе BLI, мы сравнили взаимодействия различных конформеров F RSV с панелью mAb (рис. 1B). D25 (сайт-Ø-специфическое антитело) [17] имел промежуточное связывание с NP RSV F, не связывался с F RSV после слияния и сильно связывался с F F RSV до слияния (рис. 1B). С другой стороны, паливизумаб, RSHZ19, R4.C6 и R1.42 имели одинаковое связывание со всеми тремя F-конформерами RSV, даже несмотря на то, что процент связывания R4.C6 и R1.42 был немного ниже, чем у паливизумаба и RSHZ19 (рис. 1Б).
Далее мы определили кинетику связывания панели моноклональных антител (D25, паливизумаб, мотавизумаб, RSHZ19, R1.42 и R4.C6) с различными конформерами F RSV с помощью SPR (рис. 1C, рис. S2). В соответствии с результатами связывания BLI на рис. 1B, D25 очень слабо взаимодействовал с вакциной RSV F NP, не связывался с RSV F после слияния и прочно связывался с F RSV до слияния ( K D = 1,60 нМ). . Все другие mAb, включая R4.C6, демонстрировали узкий диапазон K D при связывании с RSV F NP (0.04~0,51 нМ), до RSV F после слияния (0,04~0,34 нМ) и до F RSV до слияния (0,74~8,35 нМ).
Структура R4.C6 в комплексе с RSV F710 в состоянии после слияния
Из-за уникальных свойств связывания R4.C6 с антигенными сайтами II и IV мы сосредоточились на определении структурной основы этого антитела с RSV F. Очищенный комплекс RSV F710-R4.C6 Fab (рис. S3) использовали для единичного – крио-ЭМ анализ частиц (рис. 2). На рис. 2А показано репрезентативное необработанное изображение RSV F-R4 со льдом.Комплекс C6 на сетках из оксида графена, записанный с помощью камеры K2 Summit, а на рис. 2B показаны репрезентативные средние значения класса 2D для комплекса, полученные с помощью RELION2.0. Всего мы использовали 234 479 частиц в окончательной 3D-реконструкции и получили окончательную карту в диапазоне от 2,7 до 4,6 Å с общим разрешением 3,9 Å в соответствии с золотым стандартом корреляции оболочки Фурье (FSC) при 0,143 (таблица S1, рис. S4). .
Рис. 2. Крио-ЭМ очищенного после слияния RSV F710 в комплексе с R4.C6 Fab.
(A) Репрезентативное необработанное электронное изображение комплекса RSV F-R4.C6, встроенного в лед, на сетках из оксида графена, полученное с помощью камеры K2 Summit. Белые кружки обозначают частицы с видом сверху; черные кружки обозначают частицы с видом сбоку. Масштабная линейка, 200 Å. Показанное изображение скорректировано с помощью MotionCor2. (B) Репрезентативные средние значения класса 2D комплекса RSV F-R4.C6 Fab, полученные с использованием RELION2.0. Симметрия C3 очевидна в этих двухмерных средних классах. (C) Cryo-EM 3D-карта R4.C6 Fv в комплексе с RSV F, показанная как вид сбоку (слева) и вид сверху (справа).Также см. рис. S4 для крио-ЭМ 3D-реконструкции.
https://doi.org/10.1371/journal.pone.0210749.g002
При текущем разрешении мы можем уверенно распознать один F-тример RSV и три копии молекул R4.C6 (рис. 2C). Кристаллические структуры RSV F в конформации до слияния или после слияния (коды PDB: 4JHW и 3RRR) [17, 32] были индивидуально застыкованы на крио-ЭМ карте с помощью Chimera [39], где структура после слияния дал гораздо лучшее совпадение. Что касается части Fab, модель Fv включает известные структуры вариабельных доменов тяжелой цепи (HC) и легкой цепи (LC) с наивысшей гомологией последовательностей с R4.Использовался С6. Константная область трех молекул R4.C6 Fab не моделировалась из-за относительно плохой электронной плотности. Модель комплекса RSV F-R4.C6 была уточнена по крио-ЭМ карте с использованием Real-space-refine в Phenix [40], с последующей ручной корректировкой с помощью Coot [41] и, наконец, уточнением PCST для улучшения геометрии ( Таблица S1). Общее качество карты позволило разрешить большинство боковых цепей (S5 Fig).
Окончательная структурная модель RSV F-R4.C6 имеет тример F RSV, окруженный доменами Fv трех R4.Молекулы C6 Fab (рис. 3А). Центральный RSV F имеет три протомера, каждый из которых состоит из F2 и F1, которые ковалентно связаны двумя дисульфидными связями. N- и C-концевые домены F1 в каждом протомере упаковываются вместе, образуя пучок из шести спиралей, ключевая характеристика, присущая многим белкам слияния с мембраной в состоянии после слияния [42].
Рис. 3. Структура RSV F710 после слияния в комплексе с R4.C6.
(A) Представление ленты модели R4.C6 Fv, связанного с тримером гликопротеина F RSV в конформации после слияния, вид сбоку.Каждый протомер RSV F имеет свой цвет (голубой, желтый и зеленый). Для ясности показаны только две из трех молекул Fv R4.C6 (легкая цепь оранжевого цвета и тяжелая цепь синего цвета). Показаны фрагменты N-ацетил-D-глюкозамина, присоединенные к N70 и N500. (B) Интерфейс между тяжелой цепью RSV F и R4.C6 (HC, синий цвет) и легкой цепью (LC, оранжевый цвет). CDR помечены для R4.C6 Fv (HC, темно-синий цвет, LC, красный цвет). Также помечены антигенные сайты II и IV. Две области для увеличения (C) и (D) выделены пунктирными квадратами.(C) Подробные взаимодействия между R4.C6 и антигенным сайтом II RSV F. (D) Подробные взаимодействия между R4.C6 и антигенным сайтом IV RSV F. Сайт II F RSV окрашен в голубой цвет, а сайт IV окрашен в желтый цвет. Карты крио-ЭМ вокруг остатков в непосредственной близости от интерфейса RSV F-R4.C6 показаны серой сеткой. Та же цветовая схема используется в (B~D).
https://doi.org/10.1371/journal.pone.0210749.g003
Картирование эпитопа R4.C6
Крио-ЭМ карта на границе между тримером RSV F и каждым R4.C6 был четко определен, чтобы можно было уверенно идентифицировать эпитоп (рис. 3B–3D). Каждый R4.C6 распознает четвертичный эпитоп на F RSV, который состоит из антигенного сайта II на одном протомере и антигенного сайта IV на другом протомере (фиг. 3B). Четыре области, определяющие комплементарность (CDR) R4.C6, участвуют во взаимодействии с RSV F, что приводит к захоронению около 1571 A 2 площади поверхности между ними.
Тяжелая цепь HCDR2 и HCDR3 и легкая цепь LCDR1 и LCDR2 R4.C6 взаимодействует с антигенным сайтом II. На границе раздела остатки D53 на R4.C6 HCDR2 и K272 на RSV F, N99 на R4.C6 HCDR3 и D269 на RSV F, R48 на R4.C6 HCDR2 и N268 на RSV F, W31 на R4.C6 HC и D269/ K272 на RSV F находятся в непосредственной близости. Кроме того, R30 на R4.C6 LCDR1 и D263 на RSV F, L50 на R4.C6 LCDR2 и петля, образованная RSV F P265 и I266, находятся в тесном контакте (рис. 3C). Эти подробные взаимодействия между сайтом II F RSV в остатках 263–272 и R4.C6, выявленные нашей крио-ЭМ структурой, согласуются с SPR-анализом с использованием линейных пептидов сайта II, соответствующих остаткам F RSV 254-NSELLSLINDMPITNDQKKLMSNNV-278 и его различным N- терминальные и/или С-концевые усечения (табл. 2, S6 рис.).R4.C6 связывался с полноразмерным пептидом при K D 12,5 нМ и при сниженной аффинности с пептидами, укороченными на 6 или 10 остатков от N-конца. Кроме того, R4.C6 не связывался, когда С-концевые 6 или 10 остатки были удалены (таблица 2). Интересно, что R4.C6 не связывался с пептидом, содержащим остатки 254–273, несмотря на наличие остатков 263–272 (табл. 2). Это может быть связано с нарушением α-спирали, на которой находятся N268, D269 и K272, что приводит к потере оптимального представления этих остатков для взаимодействия с R4.C6 HC (рис. 3C).
Кроме того, R4.C6 LCDR2 и HCDR3 находятся в тесном контакте с антигенным сайтом IV RSV F, охватывая остатки 422–471 на соседнем протомере (рис. 3D), включая остатки S67 на R4.C6 LCDR2 с K427 и N428 на RSV F, R65 на R4.C6 LCDR2 с N428 на RSV F и S100 и E101 на R4.C6 HCDR3 с N454 на RSV F. Хотя нам не удалось напрямую проверить вклад сайта IV в связывание с R4.C6 дополнительными средствами, множественные ряд доказательств убедительно подтверждает его роль в этом отношении: (1) данные бинирования эпитопов на рис. 1A ясно продемонстрировали прямую конкуренцию между R4.mAb, связывающиеся с C6 и сайтом IV, такие как R1.42 и RSHZ19; (2) прямые межмолекулярные взаимодействия между сайтами IV и R4.C6 в структуре крио-ЭМ, которые мы только что описали; и (3) что более важно, R4.C6 связывается с F после слияния при K D 0,34 нМ (рис. 1C), что примерно в 30 раз сильнее, чем его связывание только с пептидом сайта II ( K D 12,5 нМ) (табл. 1).
Сравнение mAb сайта II и сайта IV с известными структурами
Антигенный сайт II F RSV делится на антигенный сайт IIa и IIb для нейтрализующих поз и сайт VII для ненейтрализующих поз [30].Существуют две известные структуры антител, специфичных к сайту II F RSV: hRSV14N4 связывается с антигенным сайтом IIa пост-слитого F RSV (код PDB: 5J3D) [30], а мотавизумаб связывает пептид из антигенного сайта IIb (код PDB: 3IXT). ) [43]. Хотя оба антитела нацелены на антигенный сайт II, мотавизумаб связывает RSV F под углом, который составляет 42° от угла связывания hRSV14N4 [30]. Путем наложения остатков с N254 по N277 антигенного сайта II комплекса hRSV14N4-RSV F и комплекса R4.C6-RSV F мы обнаружили частичное перекрытие их эпитопов в сайте II F RSV.Например, R4.C6 и hRSV14N4 имеют общие остатки D263, P265, I266, N268, D269 и K272 при связывании с антигенным сайтом II, но с остатками N262, T267 и K271, уникальными для hRSV14N4. Связывание этих двух антител с антигенным сайтом II связано с разницей углов в 150° и пространственной трансляцией в 1,1 Å по оценке DYNDOM [44] (рис. 4А). Кроме того, мотавизумаб и R4.C6 связываются с сайтом II с разницей углов 117° и пространственной трансляцией 0,7 Å (рис. 4B). Их эпитопы имеют общие остатки D263, N268, D269 и K272 с остатками P265 и I266, уникальными для R4.C6 и остатки N262, S275 и N276, уникальные для мотавизумаба.
Рис. 4. Сравнение известных структур F RSV после слияния и антител сайта II или сайта IV.
( A) Сравнение структуры RSV F-R4.C6 с RSV14N4, связанным с сайтом II F RSV (код PDB 5J3D). Слева: RSV F показан в виде поверхностной презентации, R4.C6 в виде лент, окрашенных в оранжевый цвет (легкая цепь) и синий (тяжелая цепь), и RSV14N4 в виде лент, окрашенных в зеленый цвет. Справа: перекрытие эпитопов R4.C6 и RSV14N4.Общие остатки между двумя эпитопами окрашены в красный цвет. Уникальные остатки для RSV14N4 окрашены в зеленый цвет. (B) Сравнение структуры RSV F-R4.C6 с пептидным комплексом мотавизумаб-сайт II (код PDB 3IXT). Слева: Мотавизумаб в лентах, окрашенных в желтый цвет. Справа: перекрытие эпитопов R4.C6 и мотавизумаба. Общие остатки между двумя эпитопами окрашены в красный цвет. Уникальные остатки мотавизумаба окрашены в желтый цвет. (C) Сравнение структуры RSV F-R4.C6 с пептидным комплексом Fab 101F-участок IV (код PDB 3O45).Слева: Fab 101F показан лентами голубого цвета. Справа: перекрытие эпитопов R4.C6 и Fab 101F. Уникальные остатки в сайте IV для Fab 101F окрашены в голубой цвет. На всех панелях уникальные остатки для R4.C6 окрашены в синий цвет для сайта II и оранжевый для сайта IV.
https://doi.org/10.1371/journal.pone.0210749.g004
Кроме того, мы также сравнили нашу структуру RSV F-R4.C6 с кристаллической структурой сайта IV-специфического mAb 101F с сайтом из 17 остатков. IV (код PDB: 3O45) [29] путем наложения на антигенный сайт IV остатков с N428 по N437.101F специфически связывается с антигенным сайтом IV RSV F в области остатков R429-S436. Эпитоп 101F не перекрывается с эпитопом R4.C6 (фиг. 4C). Угловая и пространственная трансляция R4.C6 при связывании с RSV F отличалась от таковой для 101F на 162° и 12,8 Å соответственно. Уникальный угол связывания R4.C6 облегчает его взаимодействие как с антигенным сайтом II, так и с сайтом IV.
Обсуждение
В этом исследовании мы сообщили об открытии четырех новых mAb, полученных у мышей, иммунизированных почти полноразмерными F NP RSV (таблица 1), после чего последовала серия подробных характеристик нового mAb, обозначенного как R4. .С6. Биннинг эпитопов с помощью BLI с использованием прибора Octet QK384 показал, что mAb R4.C6 широко конкурируют за связывание с нейтрализующими гуманизированными mAb и mAb человека, нацеленными на антигенный сайт IIa (паливизумаб, hRSV14N4 и R6.46) и сайт IIb (мотавизумаб и hRSV3J20), а также не- нейтрализующее связывание mAb (R6.29) с антигенным сайтом VII. Неожиданно mAb R4.C6 также конкурировало за связывание с нейтрализующими mAb RSHZ19 и R1.42, которые направлены на антигенный сайт IV. R4.C6 связывал RSV F NP и синтетический пептид сайта II с наномолярной аффинностью ( K D = 0.07 и 12,5 нМ соответственно), что в 7 и 30 раз выше, чем у паливизумаба (табл. 1). Однако эффективность нейтрализации R4.C6 была немного ниже, чем у паливизумаба (IC 50 = 1078 против 323 нг/мл). Более того, хотя R4.C6 имел такую же аффинность связывания с RSV F NP, что и R1.42 ( K D = 0,07 против 0,04 нМ), R4.C6 проявлял примерно в 50 раз более низкую нейтрализующую активность, чем R1.42 ( IC 50 = 1078 против 19,6 нг/мл). Таким образом, несмотря на четкую корреляцию аффинности связывания и нейтрализующей активности между паливизумабом и его вариантом с созревшей аффинностью мотавизумабом (табл. 1) [31], эта корреляция не всегда наблюдалась для других МкАТ.Вероятно, другие факторы, включая, помимо прочего, доступность целевого эпитопа(ов) на плотно упакованных гликопротеинах F RSV на поверхности вируса, также играют роль. Для лучшего понимания опосредованной mAb нейтрализации вируса RSV срочно необходимы дополнительные структурные и функциональные исследования F-специфических антител RSV, подобные описанному здесь.
R4.C6 уникален своей способностью связываться как с антигенным сайтом II, так и с сайтом IV гликопротеина F RSV. Крио-ЭМ и трехмерная реконструкция RSV F710-R4 с одной частицей.Комплекс C6 раскрыл структурную основу R4.C6 при распознавании этого нового эпитопа на F-тримере RSV после слияния. Было обнаружено, что три R4.C6 ассоциированы с одним тримером F RSV. Структура продемонстрировала, что R4.C6 распознает четвертичный эпитоп, который включает два протомера F-тримера RSV. Точное картирование показало, что два HCDR и два LCDR R4.C6 взаимодействовали с антигенными сайтами II и IV. Сравнение поз связывания с F RSV после слияния для R4.C6 с hRSV14N4 (сайт IIa), мотавизумабом (сайт IIb) и 101F (сайт IV) ясно показало, что R4.C6 связывается с RSV F под углом, отличным от этих антител (рис. 4).
Таким образом, гликопротеин F RSV является основным кандидатом для разработки вакцины. Однако он имеет сложную структуру с множественными конформациями и многочисленными антигенными эпитопами. Структуры F RSV в конформациях до слияния и после слияния в комплексе с различными mAb обеспечили значительное понимание тонкого картирования антигенных детерминант в различных конформациях. В этом отчете мы использовали крио-ЭМ и трехмерную реконструкцию одной частицы, чтобы определить структурную основу для взаимодействия R4.C6 с ранее неизвестным эпитопом, который охватывает антигенные сайты II и IV на тримере F RSV после слияния с разрешением 3,9 Å. Открытие и подробная характеристика нового эпитопа R4.C6 значительно углубили наше понимание антигенной сложности белка F. Кроме того, сравнение R4.C6 с группой других mAb с точки зрения аффинности связывания и нейтрализующей активности выявило наше неполное понимание структурных факторов и факторов окружающей среды, которые могут влиять на активность mAb in vitro и in vivo .Более подробная характеристика F-специфических антител RSV вдоль этой линии необходима для лучшего понимания mAb, направленных на вирус RSV.
Материалы и методы
Клеточные линии, вирусы, реагенты антител и синтетические пептиды
клеток HEp-2 (ATCC, CCL-23) поддерживали в MEM с солями Эрла, L-глютамином (Gibco Laboratories, Gaithersburg, MD, USA), 5% фетальной бычьей сывороткой (FBS, Hyclone, Logan UT, USA) и антибиотики (Life Technologies, Гранд-Айленд, Нью-Йорк, США).Клетки насекомых Spodoptera frugiperda (Sf9) (Invitrogen, Grand Island, NY, USA) поддерживали в бессывороточной среде в виде суспензионных культур. Клетки Trichoplusia ni High Five (BTI-TN-5B1-4, ATCC CRL-10859) поддерживали в среде Insect-XPRESS с L-глутамином и антибиотиками (Lonza, Walkersville, MD, USA). Эталонный штамм RSV/A Long (ATCC, VR-26) был получен от ATCC (Манассас, Вирджиния, США). Вирусный раствор готовили из осветленных супернатантов и хранили при -80°С в PBS с 25% сахарозой в качестве криопротектора.Паливизумаб (Синагис) был получен от MedImmune, Inc. (Гейтерсбург, Мэриленд, США), а мотавизумаб — от Национального института стандартов и технологий (Гейтерсбург, Мэриленд, США). D25 [17] (Creative Biolabs, Ширли, Нью-Йорк, США) и RSHZ19 [45] (Absolute Antibody, Оксфорд, Великобритания) были приобретены на коммерческой основе. RSV14N4 и RSV3J20 [30] были любезно предоставлены доктором Дж. Кроу (Университет Вандербильта, Нэшвилл, Теннесси, США). Синтетический пептид сайта II паливизумаба и его различные укорочения были коммерчески синтезированы пептидом 2.0 (Шантийи, Вирджиния, США).
Экспрессия и очистка RSV F NP, F до слияния и F после слияния
конструкций ДНК F RSV были синтезированы в соответствии с последовательностью гена RSV/A2 F0, кодирующей остатки 26–574 (инвентарный номер Genebank U63644), с добавлением сигнального пептида gp64 (SP) к 5′-концу всех конструкций и кодона, оптимизированного для экспрессии в клетках насекомых. (GeneArt, Регенсбург, Герм.). RSV F NP содержал интактный С-концевой трансмембранный (ТМ) и цитоплазматический хвостовой (СТ) домены, мутантный сайт расщепления II фурином (от KKRKRR до KKQKQQ) и делецию из 10 аминокислот (ΔF137—V146) в гидрофобном слитом пептиде ( ФП) [38, 46].F до слияния содержал интактный TM/CT, мутантный фуриновый сайт I (от RARR к RARQ), делецию полной области p27 (Δp27), ΔF137-V146 в FP и содержал три стабилизирующие аминокислотные замены N67I, S215P, и E487Q [47]. Пост-слитый F был сконструирован путем замены доменов TM/CT на C-концевую 6-гистидиновую метку [35]. Ген F до слияния был клонирован в бакуловирусный вектор переноса Bac I (EMD Millipore), гены F NP RSV и F после слияния были клонированы в pFastBac 1 (Invitrogen), ниже промотора полиэдра AcMNPV .Рекомбинантный бакуловирус (BV) с геном F до слияния был создан с использованием системы FlashBacGOLD BV, а вирусы с генами F NP и пост-слияния F были созданы с использованием бакуловирусной системы Bac-to-Bac. Для RSV F NP и F до слияния BV-инфицированные клетки Sf9 собирали центрифугированием и экстрагировали клеточный осадок. Клеточные лизаты осветляли и очищали, как описано ранее [38, 46]. Рекомбинантные НЧ F RSV с доменами TM/CT, извлеченными из мембран клеток насекомых, были собраны в наночастицы с морфологией, соответствующей олигомерам F [38].Для F после слияния BV-инфицированные клетки Sf9 культивировали в течение ~ 65 ч при 27 ° C, а супернатанты собирали центрифугированием (4000 × g). F после слияния очищали с помощью аффинной колонки с иммобилизованным металлом (IMAC) и ионообменной хроматографии. Эти F-белки RSV использовали для получения данных, представленных в таблице 1, фиг. 1B и 1C, фиг. S1 и S2.
Экспрессия и очистка RSV F710 после слияния
RSV F710 получен из конструкции RSV F NP с заменой доменов TM/CT на мотив тримеризации фолдона фибрина T4 (GSGYIPEAPRDGQAYVRKDGEWVLLSTFL) и добавлением 6-гистидиновой метки на С-конце фрагмента F1 [48, 49] .Ген был клонирован в сайт BamHI/Hind III вектора pFastBac DUAL (Thermo Fisher, Waltham, MA, USA) ниже промотора полиэдра AcMNPV. Кроме того, последовательность фурина Sf9 (номер доступа в Genbank CAA93116.1) была клонирована между сайтами XmaI/KpnI того же вектора pFastBac DUAL ниже промотора p10 AcMNPV. Рекомбинантную бакмидную ДНК экстрагировали из E . coli и трансфицировали в клетки Sf9 с использованием Cellfectin II (Invitrogen, Карлсбад, Калифорния, США). Собирали супернатанты трансфекции, очищали и амплифицировали рекомбинантные бляшки BV.Культуры клеток High Five при 1,5 × 10 90 103 6 90 104 клеток/мл инфицировали рекомбинантным BV, содержащим ген RSV F710, при множественности заражения = 2 и затем инкубировали при 27°C в течение 48–60 часов. Супернатант клеточной культуры, содержащий секретируемый RSV F710, собирали центрифугированием в течение 30 минут при 4000 g. Гликопротеин RSV F710 очищали путем связывания с IMAC и элюировали 250 мМ имидазолом. Далее белок очищали с помощью ионообменной хроматографии (Mono S 5/50 GL, GE Healthcare, США) и эксклюзионной хроматографии (Superdex 200 10/300 GL, GE Healthcare, США) в буфере, содержащем 20 мМ Hepes, pH 7.0 и 150 мМ NaCl. Этот белок использовался в исследовании крио-ЭМ, а также на рис. 1А и рис.
S3.Получение mAb
С использованием модифицированных стандартных методов было полученомоноклональных антител, специфичных к RSV F [37]. Вкратце, самок мышей BALB/c иммунизировали внутрибрюшинной инъекцией 5 мкг RSV F NP с интервалом в две недели. Через четыре дня после повторной иммунизации собирали селезенки и готовили суспензии отдельных клеток с помощью гомогенизатора. Спленоциты объединяли и удаляли IgM B-лимфоциты с помощью системы магнитной сортировки клеток (Miltenyi Biotec, Оберн, Калифорния, США).Обогащенные IgG спленоциты сливали с клетками миеломы P3X63.Ag.6.5.3 [37]. Гибридомы подвергали скринингу с помощью RSV F ELISA, а положительные культуры клонировали путем предельного разведения. Клеточные линии гибридом размножали в 75 см 2 Т-колбах в бессывороточной среде.
Протокол для мышей был одобрен комитетом A&G IACUC (номер гарантии благополучия животных D16-00700) с номером утверждения JH-01. Мышей подвергали эвтаназии путем вдыхания CO 2 с последующим смещением шейных позвонков. Ингаляцию CO 2 проводили методом постепенного заполнения со скоростью вытеснения от 10% до 30% объема камеры/мин.Чтобы уменьшить ненужный стресс, мышей усыпляли в клетке, когда это было возможно. Всего в исследовании использовали трех бестимусных мышей nude (Charles River, Wilmington, MA).
Анализ нейтрализации вируса
Вируснейтрализующую активность моноклональных антител определяли с помощью анализа микронейтрализации. Вкратце, очищенные mAb серийно разбавляли в диапазоне концентраций 0,004–10 мкг/мл в 96-луночных планшетах для тканевых культур и смешивали с 200–350 TCID 50 (50% инфекционной дозы тканевой культуры) RSV/A Long в течение 2 часов при 37°С.Клетки HEp-2 с малым пассажем (2,5 x 10 90 103 4 90 104 клеток) добавляли к смеси антитело/вирус при 37°C в инкубаторе с 5% CO 2 на 4–5 дней. Планшеты промывали и фиксировали. Инфекционный вирус выявляли путем добавления оптимально разведенных мышиных mAb против RSV M2-1 (клон RSV 5H5) (Novus Biologicals, LLC, Литтлтон, Колорадо, США). Планшеты промывали, добавляли козий антимышиный IgG пероксидазы хрена (HRP) с последующим добавлением субстрата TMB (3,3′,5,5′-тетраметилбензидин). Полумаксимальную ингибирующую концентрацию (IC 50 ) определяли путем подгонки кривой с 4 параметрами с использованием программного обеспечения Prism.
Биннинг эпитопов по BLI
Перекрестную конкуренцию антителпроводили с помощью BLI с использованием системы Octet QK384 (Pall Forte Bio, Fremont, CA, USA). Меченный гистидином белок RSV F710 (10 мкг/мл) иммобилизовали на наконечниках биосенсоров против пентагистидина. Захваченный RSV F710 подвергали воздействию mAb в два последовательных этапа. Наконечники Biosenor подвергали воздействию первого mAb (20 мкг/мл) в течение 5 минут с последующим погружением наконечников во второе антитело к анализируемому веществу (10 мкг/мл) еще на 5 минут. Анализы проводили при 30°C при непрерывном перемешивании со скоростью 1000 об/мин.Если связывание белка F RSV первым mAb предотвращало или уменьшало связывание конкурирующего второго mAb, считалось, что конкурирующее mAb связывается со сходными эпитопами. И наоборот, если первое mAb не мешало связыванию второго mAb, считалось, что антитела связываются с разными эпитопами. Процент (%) ингибирования связывания антител конкурирующими mAb рассчитывали с помощью программного обеспечения для анализа данных Octet HT10.0 по следующей формуле: % ингибирования = 100 – [связывание анализируемого mAb в присутствии конкурентного mAb / связывание анализируемого mAb отдельно] x 100.
MAb связывается с F-белками RSV по BLI
Антигенное сайт-специфическое связывание mAb с вакциной RSV F NP, конформерами до и после слияния определяли с помощью BLI с использованием прибора Octet OK384 (Pall FortéBio, Фремонт, Калифорния, США). Наконечники биосенсоров против Fc человека BLI использовали для иммобилизации mAb D25 (участок Ø), паливизумаб (участок IIa), RSHZ19 (участок IV) и наконечники биосенсоров против Fc мыши использовали для иммобилизации R1.42 и R4.C6. Наконечники подвергали воздействию mAb (10 мкг/мл) в течение ~600 секунд и уравновешивали исходный уровень в уравновешивающем буфере (Pall FortéBio) в течение 60 секунд.Наконечники с покрытием переносили в лунки, содержащие 20 мкг/мл вакцины RSV F NP, F после слияния или F до слияния, и оставляли для ассоциации на 600 секунд с последующей диссоциацией на 400 секунд. Процент связывания антител (% связывания) с RSV F анализировали с помощью программного обеспечения Octet HT 10.0 относительно контрольного буфера.
Аффинность связывания MAb с помощью поверхностного плазмонного резонанса
Поверхностный плазмонный резонанс (SPR) использовали для оценки аффинности связывания mAb с NP F RSV, F до слияния, F после слияния или различными синтетическими пептидами, полученными из последовательности антигенного сайта II F RSV (254-NSELLSLINDMPITNDQKKLMSNNV-278), с использованием прибор Biacore T200 (GE Healthcare, Балтимор, Мэриленд).Белок A или белок G (Thermo Fisher Scientific, Waltham, MA) иммобилизовали на чипах CM5 посредством реакции связывания с амином. Целевой уровень связывания превышал 3000 единиц ответа (RU). Все антитела разбавляли до 2 мкг/мл и вводили через чип с иммобилизованным белком A или белком G со скоростью приблизительно 10 мкл/мин в течение 45 секунд для анализа кинетики связывания F RSV или в течение 90 секунд для анализа кинетики связывания пептида антигенного участка II. RSV F вводили в возрастающих концентрациях (3,3, 10, 30, 90 нМ) на чип с иммобилизованным антителом при 40 мкл/мин в течение 180 секунд с последующим временем диссоциации 600 секунд.Аналогично, пептиды сайта II инъецировали в возрастающей концентрации (100, 200, 400, 800 нМ) в течение 180 секунд с последующим 600-секундным потоком буфера. Сенсорограммы были проанализированы с помощью кинетического анализа Biacore с использованием подходящей модели 1:1 для определения скоростей k a и k d . Константа кажущегося равновесия K D была рассчитана с использованием уравненияЧипы регенерировали путем введения 100 мМ HCl со скоростью 40 мкл/мин в течение 45 секунд.
Очистка R4.C6 и получение Fab
Для получения Fab R4.C6 гибридому выращивали в бессывороточной среде в биореакторе объемом 7 л (Southern Biotech, Бирмингем, Алабама, США). Очищенный супернатант концентрировали и наносили на аффинную колонку с белком G в соответствии с протоколом производителя (GE Healthcare Life Sciences). Очищенный R4.C6 расщепляли папаином (набор для подготовки Pierce Fab, Thermo Fisher Scientific) с умеренным восстановлением.Антигенсвязывающие фрагменты (Fab) очищали от нерасщепленных фрагментов IgG и Fc с помощью ионообменной хроматографии (Southern Biotech, Birmingham, AL, USA). Fab имел чистоту 98,8%, как определено ВЭЖХ с обращенной фазой.
Получение комплекса R4.C6 Fab и RSV F
Для получения Fab R4.C6 в комплексе с белком F RSV очищенный тример F710 RSV смешивали с R4.C6 в молярном соотношении 1:4. Это соотношение обеспечивало насыщение белка F RSV R4.C6. Смесь помещали на лед на 30 мин и затем очищали на колонке для гель-фильтрации Superdex 200 10/300 GL (GE Healthcare, США) с подвижным буфером 10 мМ Hepes, 100 мМ NaCl, pH 7.0. Комплекс элюировали в объеме 9,8 мл, а избыток R4.C6 элюировали в объеме 16 мл. По сравнению с профилем эксклюзионной хроматографии одного белка RSV F710 пик комплекса R4.C6-RSV F имел сдвиг объема элюции на 1,5 мл. Образцы каждого пика анализировали, используя 12% восстановленный Bis-Tris SDS-PAGE гель. Элюированный комплекс концентрировали до 2 мг/мл для хранения и подготовки образца крио-ЭМ.
Изготовление сеток с покрытием из оксида графена
Дисперсиюоксида графена (Sigma-Aldrich, США; 4 мг/мл в H 2 O) разбавляли до 0.2 мг/мл с водой Milli-Q (mqH 2 O) и центрифугировали при 300×g в течение 30 секунд для удаления крупных агрегатов. Сетки Quantifoil R1.2/1.3 с медными отверстиями 200 меш (Quantifoil, Йена, Германия) подвергали тлеющему разряду в течение 75 секунд. 3 мкл суспензии оксида графена добавляли к углеродной стороне сетки и инкубировали в течение 2 минут. После инкубации раствор оксида графена удаляли кратким промоканием фильтровальной бумагой Whatman № 1 сбоку с последующей промывкой mqH 2 O и промоканием.Покрытие оксида графена на сетке перед использованием визуализировали с помощью просвечивающего электронного микроскопа (ПЭМ) в режиме малого увеличения. Сетки, покрытые оксидом графена, использовались для глубокой заморозки без какой-либо дополнительной обработки.
Подготовка образца крио-ЭМ
Аликвоту 3,5 мкл комплекса, разбавленного до 0,05 мг/мл, наносили на медные перфорированные сетки Quantifoil R1.2/1.3 200 меш, покрытые оксидом графена. После 15-секундной инкубации сетка автоматически промокалась в течение 4 секунд со стороны образца с помощью Whatman No.1 фильтровальную бумагу и немедленно погружали в жидкий этан с использованием автоматического погружного морозильника Leica EM GP (Leica Microsystems, Вена, Австрия) с температурой камеры для окружающей среды, установленной на 22°C, и относительной влажностью 98%. Сетки переносили и хранили в жидком азоте перед визуализацией.
Сбор данных крио-ЭМ и обработка изображений
Все данные были собраны на криоэлектронном микроскопе JEM3200FSC (JEOL, Пибоди, Массачусетс, США), работающем при 300 кВ, с энергетической щелью внутриколоночного фильтра 20 эВ.Изображения были записаны с помощью камеры прямого детектора электронов (DDD) K2 Summit (Gatan, Inc, Уоррендейл, Пенсильвания, США) в режиме счета электронов сверхвысокого разрешения при 30000-кратном увеличении микроскопа (соответствует калиброванному физическому размеру пикселя 1,2546 Å). Мощность дозы составляет 5 электронов/Å 90 103 2 90 104 /сек, и за общее время экспозиции 10 секунд было получено 50 кадров. Всего было собрано 2734 стопки фильмов DDD.
Стеки необработанных изображений сверхвысокого разрешения, фракционированные по дозе, были объединены в бины 2 X 2 с помощью кадрирования Фурье, что привело к размеру пикселя, равному 1.2546 Å для дальнейшей обработки изображения. Каждый стек изображений (содержащий все 50 кадров) подвергался коррекции движения с помощью MotionCor2 [50]. Gctf [51] использовали для оценки параметров контрастной передаточной функции. 7456 частиц были помещены в бокс вручную с использованием «e2boxer.py» в EMAN2 [52] в качестве подмножества частиц для расчета безэталонных средних 2D-классов, которые затем использовались в качестве шаблонов для автоматического выбора частиц всего набора дат. В итоге было собрано 543 639 частиц. Исходная карта была сгенерирована с 3-кратной симметрией из двумерных средних без эталонных значений с использованием EMAN2.Эта первоначальная эталонная карта была замаскирована, так что была сохранена только F-часть RSV. Затем он был подвергнут низкочастотной фильтрации до разрешения 60 Å и использован в качестве исходной модели. Для последующей обработки изображений использовался пакет RELION2.0 [53]. Первоначальные прогоны 2D- и 3D-классификаций использовались для удаления ложноположительных частиц из автовыбора. Только те хорошие частицы были выбраны для дальнейшего анализа. Было выполнено несколько раундов итеративной 3D-классификации и 3D-автоматического уточнения. 234 479 частиц были использованы в окончательной доработке для достижения 3.Карта плотности с разрешением 9 Å. Мягкая маска в постобработке RELION была применена перед вычислением FSC. Окончательное разрешение оценивалось с использованием золотого стандарта FSC = 0,143. Карта плотности была уточнена путем применения коэффициента B -250 Å 2 , рассчитанного с помощью автоматизированной процедуры. Изменения локального разрешения оценивались с помощью ResMap [54] с использованием двух независимых карт.
Построение модели, уточнение и анализ комплекса РСВ F-R4.C6
Кристаллические структуры RSV F в конформации до или после слияния (коды PDB: 4JHW и 3RRR) были отдельно пристыкованы к карте с помощью Chimera [39], где структура после слияния подходила намного лучше.Поскольку для R4.C6 Fab нет известной структуры, была построена модель гомологии с использованием известных структур вариабельных доменов тяжелой и легкой цепей, которые демонстрируют наивысшую гомологию последовательности с R4.C6 (код PDB: 1I3G [55]). Метод гибкой подгонки молекулярной динамики (MDFF) [56] был использован для гибкой подгонки модели гомологии к крио-ЭМ карте. Затем модель комплекса была уточнена с помощью Phenix [40] в реальном пространстве с последующей ручной корректировкой с помощью Coot [41] для оптимизации локального соответствия плотности.Кроме того, применялся параллельный непрерывный имитируемый отпуск (PCST) с уточнением конструкции (F.N., Q.W. и J.M., неопубликованные данные). Алгоритм PCST реализован в программе Gromacs [57]. Структуры без ограничений во время моделирования были выделены и ранжированы по потенциалу GOAP [58]. Структура с наименьшей оценкой GOAP затем была помещена в карту EM с помощью программы phenix.real_space_refine. После уточнения PCST качество модели и статистика геометрии, рассчитанные MolProbity, были значительно улучшены.Для структурного анализа общую скрытую площадь поверхности между R4.C6 и RSV F710 рассчитывали с использованием AREAIMOL в CCP4 [59], а относительную ориентацию различных mAb при связывании с F-белком RSV оценивали с помощью DYNDOM [44] в CCP4 [59]. ].
Вспомогательная информация
S1 Рис. Сенсограммы SPR-анализа аффинности связывания между панелью mAb и RSV F NP или пептидом сайта II. Использовали
RSV F NP в концентрациях 3,33, 10, 30, 90 нМ или пептид сайта II в концентрациях 100, 200, 400, 800 нМ (от низкой до высокой).Черные кривые были аппроксимирующими кривыми. По оси абсцисс отложено время (секунды), а по оси ординат — резонансная единица (RU). Значения аффинности связывания представлены в таблице 1.
10.1371/journal.pone.0210749.s001
(TIF)
S2 Рис. Сенсограммы SPR-анализа аффинности связывания между панелью mAb и вакциной RSV F NP, тримером после слияния или тримером до слияния. Использовали
RSV F в концентрациях 3,33, 10, 30, 90 нМ (от низкой до высокой). По оси абсцисс отложено время (секунды), а по оси ординат — резонансная единица (RU).Черные кривые были аппроксимирующими кривыми. Значения аффинности связывания представлены на рис. 1С.
10.1371/journal.pone.0210749.s002
(TIF)
S3 Рис. Очистка Fab R4.C6 в комплексе с гликопротеином F710 RSV.
Профили эксклюзионной хроматографии комплекса RSV F-R4.C6 (черная сплошная линия) и отдельно тримера F-F RSV (синяя пунктирная линия) с использованием колонки Superdex 200 10/300 GL (GE Healthcare). Пики комплекса RSV F-R4.C6, тримера RSV F и избытка R4.C6 имеют маркировку. Окрашенный кумасси 12% восстановленный Bis-Tris SDS-PAGE гель показывает RSV F (F1 и F2) и R4.C6 Fab в комплексном пике. Белковые стандарты известной молекулярной массы маркируются.
10.1371/journal.pone.0210749.s003
(TIF)
S4 Рис. Крио-ЭМ 3D реконструкция комплекса RSV F-R4.C6 и оценка разрешения.
(A) Спектр мощности Фурье микрофотографии, показанной на рис. 2A, с помеченными кольцами Тона и водяным кольцом 3,5 Å. (B) График распределения углов Эйлера всех частиц, используемых для окончательной трехмерной реконструкции.Длина и цвет полосы (синий, низкий; красный, высокий) пропорциональны количеству частиц, участвующих в каждом конкретном представлении. Также показана уточненная карта реконструкции с разных ракурсов. (C) Крио-ЭМ карта R4.C6 Fv в комплексе с RSV F окрашена в соответствии с оценкой локального разрешения ResMap. Карта крио-ЭМ демонстрирует локальное разрешение в диапазоне от 2,7 до 4,6 Å. (D) Кривые FSC золотого стандарта для 3D-реконструкции (синяя кривая), созданные с помощью RELION2.0 и сопоставления и . модель (красная кривая), отмеченная разрешением, соответствующим FSC = 0.143.
10.1371/journal.pone.0210749.s004
(TIF)
S5 Рис. Репрезентативные крио-ЭМ карты конечного комплекса RSV F-R4.C6.
(A-E) Остатки RSV F. (A) Спираль в остатках 78–95; (Б) Спираль в остатках 227–239; (C) Спираль в остатках 205–227; (D) Остатки 29–42; (Е) Остатки 403–417. (F-G) Остатки R4.C6. (F) Остатки 66–81 тяжелой цепи R4.C6. (G) Остатки 62–76 легкой цепи R4.C6. Карта крио-ЭМ для каждой выбранной области показана черной сеткой и наложена на соответствующий RSV F-R4.C6 сложная модель. Атомы остатка окрашены следующим образом: C = голубой, N = синий, O = красный, S = желтый.
10.1371/journal.pone.0210749.s005
(TIF)
S6 Рис. Сенсограммы SPR-анализа аффинности связывания между пептидом сайта II или его укороченными вариантами и R4.C6 или паливизумабом.
Использовались пептиды сайта II в концентрациях 100, 200, 400, 800 нМ (от низких до высоких). Черные кривые были аппроксимирующими кривыми. По оси абсцисс отложено время (секунды), а по оси ординат — резонансная единица (RU).Значения аффинности связывания приведены в таблице 2.
10.1371/journal.pone.0210749.s006
(TIF)
Благодарности
ЯдроCryo-EM ATC поддерживается Медицинским колледжем Бэйлора.
Каталожные номера
- 1. Хейнс А.К., Прилл М.М., Иване М.К., Гербер С.И., Центры по болезням С, Профилактика. Респираторно-синцитиальный вирус — США, июль 2012 г. — июнь 2014 г. Еженедельный отчет MMWR о заболеваемости и смертности. 2014;63(48):1133–6. пмид: 25474034; Центральный PMCID PubMed: PMCPMC4584603.
- 2. Hall CB, Weinberg GA, Iwane MK, Blumkin AK, Edwards KM, Staat MA, et al. Бремя респираторно-синцитиальной вирусной инфекции у детей раннего возраста. N Engl J Med. 2009;360(6):588–98. пмид: 19196675; Центральный PMCID PubMed: PMCPMC4829966.
- 3. Уолш Э.Э., Фолси А.Р. Респираторно-синцитиальная вирусная инфекция у взрослых. Заразить мишени для наркотиков. 2012;12(2):98–102. пмид: 22335500.
- 4. Ши Т., Макаллистер Д.А., О’Брайен К.Л., Симоэс Э.А.Ф., Мадхи С.А., Гесснер Б.Д. и др.Глобальные, региональные и национальные оценки бремени острых инфекций нижних дыхательных путей, вызванных респираторно-синцитиальным вирусом, у детей раннего возраста в 2015 г.: систематический обзор и модельное исследование. Ланцет. 2017;390(10098):946–58. пмид: 28689664; Центральный PMCID PubMed: PMCPMC5592248.
- 5. Nair H, Nokes DJ, Gessner BD, Dherani M, Madhi SA, Singleton RJ и др. Глобальное бремя острых инфекций нижних дыхательных путей, вызванных респираторно-синцитиальным вирусом, у детей раннего возраста: систематический обзор и метаанализ.Ланцет. 2010;375(9725):1545–55. пмид: 20399493; Центральный PMCID PubMed: PMCPMC2864404.
- 6. Борхерс А.Т., Чанг С., Гершвин М.Е., Гершвин Л.Дж. Респираторно-синцитиальный вирус — всесторонний обзор. Клин Рев Аллергия Иммунол. 2013;45(3):331–79. Эпб 2013/04/12. пмид: 23575961.
- 7. Джонсон С., Оливер С., Принц Г.А., Хемминг В.Г., Пфарр Д.С., Ван С.К. и др. Разработка гуманизированного моноклонального антитела (MEDI-493) с мощной активностью in vitro и in vivo против респираторно-синцитиального вируса.J заразить Dis. 1997;176(5):1215–24. пмид:9359721.
- 8. Паливизумаб, гуманизированное моноклональное антитело к респираторно-синцитиальному вирусу, снижает частоту госпитализаций по поводу респираторно-синцитиальной вирусной инфекции у младенцев из группы высокого риска. Педиатрия. 1998;102(3):531–537. пмид:9724660.
- 9. Комитет Американской академии педиатрии по инфекционным заболеваниям D, Рекомендации Американской академии педиатрии по бронхиолиту C. Обновленное руководство по профилактике паливизумаба среди младенцев и детей младшего возраста с повышенным риском госпитализации по поводу респираторно-синцитиальной вирусной инфекции.Педиатрия. 2014;134(2):415–20. пмид: 25070315.
- 10. Мафсон М.А., Орвелл С., Рафнар Б., Норрби Э. Два различных подтипа респираторно-синцитиального вируса человека. Джей Ген Вирол. 1985; 66 (часть 10): 2111–24. пмид: 2413163.
- 11. Андерсон Л.Дж., Хирхольцер Дж.К., Цоу С., Хендри Р.М., Ферни Б.Ф., Стоун И. и др. Антигенная характеристика штаммов респираторно-синцитиальных вирусов моноклональными антителами. J заразить Dis. 1985;151(4):626–33. пмид: 2579169.
- 12. Перет Т.С., Холл К.Б., Шнабель К.С., Голуб Дж.А., Андерсон Л.Дж.Модели циркуляции генетически различных штаммов групп А и В респираторно-синцитиального вируса человека в сообществе. Джей Ген Вирол. 1998; 79 (часть 9): 2221–9. пмид:9747732.
- 13. Гимферрер Л., Кампинс М., Кодина М.Г., Мартин Мдель С., Фуэнтес Ф., Эсперальба Дж. и соавт. Молекулярная эпидемиология и молекулярная характеристика респираторно-синцитиальных вирусов в университетской больнице третичного уровня в Каталонии (Испания) в сезоне 2013–2014 гг. Джей Клин Вирол. 2015;66:27–32. пмид: 25866332.
- 14. Хаус А.М., Хенке Д.М., Авадханула В., Шоу К.А., Тапиа Л.И., Пьедра П.А. Изменчивость последовательности слитого гена респираторно-синцитиального вируса (RSV) среди современных и исторических генотипов RSV/A и RSV/B. ПЛОС Один. 2017;12(4):e0175792. пмид: 28414749; Центральный PMCID PubMed: PMCPMC5393888.
- 15. Гриффитс С., Дрюс С.Дж., Маршан Д.Дж. Респираторно-синцитиальный вирус: инфекция, обнаружение и новые возможности профилактики и лечения. Clin Microbiol Rev. 2017;30(1):277–319.Эпублик 2016/12/03. пмид: 273; Центральный PMCID PubMed: PMCPMC5217795.
- 16. Коллинз П.Л., Фернс Р., Грэм Б.С. Респираторно-синцитиальный вирус: вирусология, обратная генетика и патогенез заболевания. Курр Топ Микробиол Иммунол. 2013; 372:3–38. пмид: 24362682; Центральный PMCID PubMed: PMCPMC4794264.
- 17. McLellan JS, Chen M, Leung S, Graepel KW, Du X, Yang Y и др. Структура тримера слитого гликопротеина RSV, связанного со специфичным для слияния нейтрализующим антителом.Наука. 2013;340(6136):1113–7. пмид: 23618766; Центральный PMCID PubMed: PMCPMC4459498.
- 18. Букреев А., Ян Л., Фрике Дж., Ченг Л., Уорд Дж.М., Мерфи Б.Р. и др. Секретируемая форма гликопротеина G респираторно-синцитиального вируса помогает вирусу избежать опосредованного антителами ограничения репликации, действуя как антиген-приманка и воздействуя на лейкоциты, несущие рецептор Fc. Дж Вирол. 2008;82(24):12191–204. пмид: 18842713; Центральный PMCID PubMed: PMCPMC2593351.
- 19. Уолш Э.Э., Брандрис М.В., Шлезингер Дж.Дж.Иммунологические различия между оболочечными гликопротеинами двух штаммов респираторно-синцитиального вируса человека. Джей Ген Вирол. 1987; 68 (часть 8): 2169–76. пмид:3302101.
- 20. Джонсон П.Р., Сприггс М.К., Олмстед Р.А., Коллинз П.Л. Гликопротеин G респираторно-синцитиальных вирусов человека подгрупп А и В: значительное расхождение последовательностей между антигенно родственными белками. Proc Natl Acad Sci U S A. 1987;84(16):5625–9. пмид: 2441388; Центральный PMCID PubMed: PMCPMC298915.
- 21.Tan L, Lemey P, Houspie L, Viveen MC, Jansen NJ, van Loon AM и др. Генетическая изменчивость полных геномов подгруппы А респираторно-синцитиального вируса человека: связывание молекулярной эволюционной динамики и эпидемиологии. ПЛОС Один. 2012;7(12):e51439. пмид: 23236501; Центральный PMCID PubMed: PMCPMC3517519.
- 22. Мэн Дж., Стобарт К.С., Хотард А.Л., Мур М.Л. Обзор респираторно-синцитиального вируса. PLoS Патог. 2014;10(4):e1004016. пмид: 24763387; Центральный PMCID PubMed: PMCPMC3999198.
- 23. Гонсалес-Рейес Л., Руис-Аргуэлло М.Б., Гарсия-Баррено Б., Колдер Л., Лопес Дж.А., Альбар Дж.П. и др. Для активации слияния мембран требуется расщепление слитого белка респираторно-синцитиального вируса человека в двух разных местах. Proc Natl Acad Sci U S A. 2001;98(17):9859–64. Эпб 09.08.2001. пмид:11493675; Центральный PMCID PubMed: PMCPMC55543.
- 24. Уолш Э.Э., Хруска Дж. Моноклональные антитела к белкам респираторно-синцитиального вируса: идентификация слитого белка.Дж Вирол. 1983;47(1):171–7. пмид:6345804; Центральный PMCID PubMed: PMCPMC255221.
- 25. Kulkarni PS, Hurwitz JL, Simoes EAF, Piedra PA. Установление коррелятов защиты для разработки вакцин: соображения в отношении вакцин против респираторно-синцитиального вируса. Вирус Иммунол. 2018. пмид: 29336703; Центральный PMCID PubMed: PMCPMC5863081.
- 26. Beeler JA, van Wyke Coelingh K. Эпитопы нейтрализации гликопротеина F респираторно-синцитиального вируса: влияние мутации на функцию слияния.Дж Вирол. 1989;63(7):2941–50. пмид: 2470922; Центральный PMCID PubMed: PMCPMC250848.
- 27.
Росси И., Маклеллан Дж. С., Саленс Х., Схепенс Б. Клинический потенциал F-специфических антител перед слиянием RSV. Тенденции микробиол. 2018;26(3):209–19. Эпб 2017/10/22. пмид: 2
41. 49025 [pii] pmid:20124702; Центральный PMCID в PubMed: PMC2815670.- 28. Мелеро Дж. А., Мас В., Маклеллан Дж. С. Структурные, антигенные и иммуногенные особенности гликопротеинов респираторно-синцитиального вируса, имеющие значение для разработки вакцин. вакцина. 2017;35(3):461–8. Эпублик 2016/10/19.пмид: 27692522; Центральный PMCID PubMed: PMCPMC5189713.
- 29. Маклеллан Дж. С., Чен М., Чанг Дж. С., Ян И, Ким А., Грэм Б. С. и др. Структура основного антигенного сайта на слитом гликопротеине респираторно-синцитиального вируса в комплексе с нейтрализующим антителом 101F. Дж Вирол. 2010;84(23):12236–44. пмид: 20881049; Центральный PMCID PubMed: PMCPMC2976384.
- 30. Муса Дж.Дж., Зауэр М.Ф., Севи А.М., Финн Дж.А., Бейтс Дж.Т., Альварадо Г. и др. Структурная основа конкуренции ненейтрализующих антител в антигенном сайте II слитого белка респираторно-синцитиального вируса.Proc Natl Acad Sci U S A. 2016;113(44):E6849–E58. пмид: 277; Центральный PMCID PubMed: PMCPMC5098655.
- 31. Wu H, Pfarr DS, Johnson S, Brewah YA, Woods RM, Patel NK, et al. Разработка мотавизумаба, сверхмощного антитела для профилактики респираторно-синцитиальной вирусной инфекции верхних и нижних дыхательных путей. Дж Мол Биол. 2007;368(3):652–65. Эпб 2007/03/17. пмид: 17362988.
- 32. Маклеллан Дж. С., Ян И, Грэм Б. С., Квонг П. Д. Структура слитого гликопротеина респираторно-синцитиального вируса в конформации после слияния выявляет сохранение нейтрализующих эпитопов.Дж Вирол. 2011;85(15):7788–96. пмид: 21613394; Центральный PMCID PubMed: PMCPMC3147929.
- 33. Маклеллан Дж.С. Нейтрализующие эпитопы на гликопротеине слияния респираторно-синцитиального вируса. Карр Опин Вирол. 2015;11:70–75. пмид: 25819327; Центральный PMCID PubMed: PMCPMC4456247.
- 34. Арбиза Дж., Тейлор Дж., Лопес Дж. А., Фурз Дж., Уайлд С., Уайт П. и др. Характеристика двух антигенных сайтов, распознаваемых нейтрализующими моноклональными антителами, направленными против слитого гликопротеина респираторно-синцитиального вируса человека.Джей Ген Вирол. 1992; 73 (часть 9): 2225–34. пмид: 1383404.
- 35. Суонсон К.А., Сеттембре Э.К., Шоу К.А., Дей А.К., Раппуоли Р., Мандл К.В. и соавт. Структурная основа для иммунизации гликопротеином F слитого респираторно-синцитиального вируса после слияния (RSV F) для получения высоких титров нейтрализующих антител. Proc Natl Acad Sci U S A. 2011;108(23):9619–24. пмид: 21586636; Центральный PMCID PubMed: PMCPMC3111287.
- 36. Kwakkenbos MJ, Diehl SA, Yasuda E, Bakker AQ, van Geelen CM, Lukens MV, et al.Создание стабильных моноклональных антител, продуцирующих В-клеточный рецептор, позитивных В-клеток памяти человека с помощью генетического программирования. Нат Мед. 2010;16(1):123–8. пмид: 20023635; Центральный PMCID PubMed: PMCPMC2861345.
- 37. Apiratmateekul N, Phunpae P, Kasinrerk W. Метод модифицированной гибридомы для получения моноклональных антител, имеющих желаемые изотипы. Цитотехнология. 2009;60(1–3):53. пмид: 19705290; Центральный PMCID PubMed: PMCPMC2780549.
- 38. Смит Г., Рагунандан Р., Ву Ю., Лю Ю., Массаре М., Натан М. и др.Гликопротеин слияния респираторно-синцитиального вируса, экспрессируемый в клетках насекомых, образует белковые наночастицы, которые индуцируют защитный иммунитет у хлопчатобумажных крыс. ПЛОС Один. 2012;7(11):e50852. пмид: 23226404; Центральный PMCID PubMed: PMCPMC3511306.
- 39. Петтерсен Э.Ф., Годдард Т.Д., Хуанг С.К., Коуч Г.С., Гринблатт Д.М., Мэн Э.К. и др. UCSF Chimera — система визуализации для поисковых исследований и анализа. J Comput Chem. 2004;25(13):1605–12. пмид: 15264254.
- 40. Адамс П.Д., Афонин П.В., Бункоци Г., Чен В.Б., Дэвис И.В., Эколс Н. и др.PHENIX: комплексная система на основе Python для решения макромолекулярной структуры. Acta Crystallogr D Биол Кристаллогр. 2010; 66 (часть 2): 213–21. Эпублик 2010/02/04. S0
- 41. Эмсли П., Коутан К. Кут: инструменты построения моделей для молекулярной графики. Acta Crystallogr D Биол Кристаллогр. 2004; 60 (часть 12 часть 1): 2126–32. Эпублик 2 декабря 2004 г. S049158 [pii] pmid:15572765.
- 42. Скехел Дж. Дж., Уайли, округ Колумбия.Спиралевидные спирали как во внутриклеточных везикулах, так и в слиянии мембран вирусов. Клетка. 1998;95(7):871–4. пмид:9875840
- 43. McLellan JS, Chen M, Kim A, Yang Y, Graham BS, Kwong PD. Структурные основы нейтрализации респираторно-синцитиального вируса мотавизумабом. Nat Struct Mol Biol. 2010;17(2):248–50. пмид: 20098425; Центральный PMCID PubMed: PMCPMC3050594.
- 44. Хейворд С., Ли Р.А. Усовершенствования в анализе доменных движений в белках по конформационным изменениям: DynDom версии 1.50. Графовая модель J-Mol. 2002;21(3):181–3. пмид:12463636.
- 45. Everitt DE, Davis CB, Thompson K, DiCicco R, Ilson B, Demuth SG, et al. Фармакокинетика, антигенность и ингибирующая слияние активность RSHZ19, гуманизированного моноклонального антитела к респираторно-синцитиальному вирусу, у здоровых добровольцев. J заразить Dis. 1996;174(3):463–9. пмид:8769601.
- 46. Raghunandan R, Lu H, Zhou B, Xabier MG, Massare MJ, Flyer DC, et al. Вакцина F наночастиц респираторно-синцитиального вируса (RSV), полученная из клеток насекомых, индуцирует антитела антигенного участка II и защищает от заражения RSV у хлопчатобумажных крыс посредством активной и пассивной иммунизации.вакцина. 2014;32(48):6485–92. пмид: 25269094.
- 47. Krarup A, Truan D, Furmanova-Hollenstein P, Bogaert L, Bouchier P, Bisschop IJ, et al. Высокостабильная префузионная вакцина RSV F, полученная в результате структурного анализа механизма слияния. Нац коммун. 2015;6:8143. Эпб 2015/09/04. пмид: 26333350; Центральный PMCID PubMed: PMCPMC4569726.
- 48. Ни Ф., Кондрашкина Е., Ван К. Структурно-функциональные исследования гемагглютинина вируса гриппа A/H6. ПЛОС Один. 2015;10(7):e0134576.пмид: 26226046; Центральный PMCID PubMed: PMCPMC4520562.
- 49.
Ни Ф., Кондрашкина Е., Ван К. Детерминант переключения рецептор-предпочтение в гемагглютинине гриппа. Вирусология. 2018; 513: 98–107. пмид: 2
55. - 50. Чжэн С.К., Паловчак Э., Армаш Д.П., Верба К.А., Ченг Ю., Агард Д.А. MotionCor2: анизотропная коррекция движения, вызванного лучом, для улучшения криоэлектронной микроскопии. Нат Методы. 2017;14(4):331–2. пмид: 28250466; Центральный PMCID PubMed: PMCPMC5494038.
- 51.Чжан К. Gctf: определение и коррекция CTF в реальном времени. J Struct Biol. 2016;193(1):1–12. пмид: 26592709; Центральный PMCID PubMed: PMCPMC4711343.
- 52. Тан Г., Пэн Л., Болдуин П.Р., Манн Д.С., Цзян В., Рис И. и др. EMAN2: расширяемый пакет обработки изображений для электронной микроскопии. J Struct Biol. 2007;157(1):38–46. пмид: 16859925.
- 53. Шерес Ш. RELION: реализация байесовского подхода к определению структуры крио-ЭМ. J Struct Biol.2012;180(3):519–30. пмид: 23000701; Центральный PMCID PubMed: PMCPMC36.
- 54. Кукукельбир А., Сигворт Ф.Дж., Тагаре Х.Д. Количественная оценка локального разрешения крио-ЭМ карт плотности. Нат Методы. 2014;11(1):63–5. пмид: 24213166; Центральный PMCID PubMed: PMCPMC35.
- 55. Burmester J, Spinelli S, Pugliese L, Krebber A, Honegger A, Jung S, et al. Отбор, характеристика и рентгеновская структура фрагментов одноцепочечного Fv против ампициллина из библиотек мышиных антител с фаговым дисплеем.Дж Мол Биол. 2001;309(3):671–85. пмид: 11397088.
- 56. Trabuco LG, Villa E, Schreiner E, Harrison CB, Schulten K. Гибкая установка молекулярной динамики: практическое руководство по объединению криоэлектронной микроскопии и рентгеновской кристаллографии. Методы. 2009;49(2):174–80. пмид: 19398010; Центральный PMCID PubMed: PMCPMC2753685.
- 57. Хесс Б., Кутцнер К., ван дер Споэль Д., Линдал Э. GROMACS 4: Алгоритмы для высокоэффективного, сбалансированного по нагрузке и масштабируемого молекулярного моделирования.J Chem Theory Comput. 2008;4(3):435–47. пмид: 26620784.
- 58. Чжоу Х., Сколник Дж. GOAP: обобщенный статистический потенциал всех атомов, зависящий от ориентации, для предсказания структуры белка. Биофиз Дж. 2011;101(8):2043–52. пмид: 22004759; Центральный PMCID PubMed: PMCPMC3192975.
- 59. Совместный вычислительный проект N. Пакет CCP4: программы для кристаллографии белков. Acta Crystallogr D Биол Кристаллогр. 1994; 50 (часть 5): 760–3. пмид: 15299374.
.

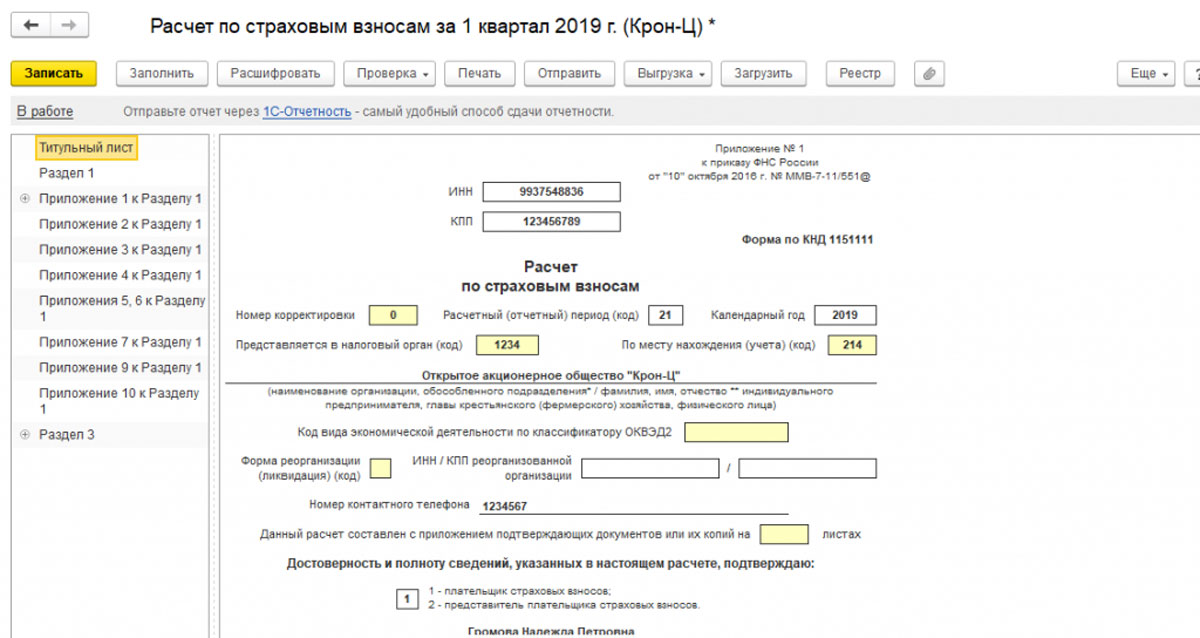 2.1 раздела 3 указывать соответствующий код категории застрахованного лица «НР», «ВЖНР», «ВПНР»;
2.1 раздела 3 указывать соответствующий код категории застрахованного лица «НР», «ВЖНР», «ВПНР»; Если в выборку попали сотрудники с одинаковыми СНИЛС, ошибочно внесенные в список, или была допущена ошибка при заполнении, то пользователь может сразу исправить ошибку. Более подробно про подачу корректировок читайте в справке.
Если в выборку попали сотрудники с одинаковыми СНИЛС, ошибочно внесенные в список, или была допущена ошибка при заполнении, то пользователь может сразу исправить ошибку. Более подробно про подачу корректировок читайте в справке.