Утверждение инструкций по охране труда в организации: V. Разработка и утверждение инструкций по охране труда для работников / КонсультантПлюс
V. Разработка и утверждение инструкций по охране труда для работников / КонсультантПлюс
V. Разработка и утверждение инструкций
по охране труда для работников
5.1. Инструкция по охране труда для работника разрабатывается исходя из его должности, профессии или вида выполняемой работы.
5.2. Разработка инструкции по охране труда для работника осуществляется с учетом главы 212 Трудового кодекса Российской Федерации.
КонсультантПлюс: примечание.
В официальном тексте документа, видимо, допущена опечатка: имеется в виду статья 212 Трудового кодекса РФ, а не глава 212, которая отсутствует в указанном документе.
5.3. Инструкция по охране труда для работника разрабатывается на основе межотраслевой или отраслевой типовой инструкции по охране труда (а при ее отсутствии – межотраслевых или отраслевых правил по охране труда), требований безопасности, изложенных в эксплуатационной и ремонтной документации организаций-изготовителей оборудования, а также в технологической документации организации с учетом конкретных условий производства.
Примерный вид титульного листа инструкций по охране труда для работников при их издании рекомендуется оформлять в соответствии с приложением N 8 к настоящим Методическим рекомендациям.
5.4. Работодатель обеспечивает разработку и утверждение инструкций по охране труда для работников с учетом изложенного в письменном виде мнения выборного профсоюзного или иного уполномоченного работниками органа. Коллективным договором, соглашением может быть предусмотрено принятие инструкций по охране труда по согласованию с представительным органом работников.
5.5. Для вводимых в действие новых и реконструированных производств допускается разработка временных инструкций по охране труда для работников.
Временные инструкции по охране труда для работников обеспечивают безопасное ведение технологических процессов (работ) и безопасную эксплуатацию оборудования. Они разрабатываются на срок до приемки указанных производств в эксплуатацию.
5.6. Проверку и пересмотр инструкций по охране труда для работников организует работодатель. Пересмотр инструкций должен производиться не реже одного раза в 5 лет.
5.7. Инструкции по охране труда для работников могут досрочно пересматриваться:
а) при пересмотре межотраслевых и отраслевых правил и типовых инструкций по охране труда;
б) изменении условий труда работников;
в) внедрении новой техники и технологии;
г) по результатам анализа материалов расследования аварий, несчастных случаев на производстве и профессиональных заболеваний;
д) по требованию представителей органов по труду субъектов Российской Федерации или органов федеральной инспекции труда.
5.8. Если в течение срока действия инструкции по охране труда для работника условия его труда не изменились, то ее действие продлевается на следующий срок.
5.9. Действующие в подразделении инструкции по охране труда для работников структурного подразделения организации, а также перечень этих инструкций хранится у руководителя этого подразделения.
5.10. Местонахождение инструкций по охране труда для работников рекомендуется определять руководителю структурного подразделения организации с учетом обеспечения доступности и удобства ознакомления с ними.
Инструкции по охране труда для работников могут быть выданы им на руки для изучения при первичном инструктаже либо вывешены на рабочих местах или участках, либо хранятся в ином месте, доступном для работников.
Рекомендуемые формы журналов учета инструкций по охране труда для работников и учета выдачи инструкций по охране труда для работников подразделений организации приведены в приложениях N 9 и 10 к настоящим Методическим рекомендациям.
Открыть полный текст документа
Кем разрабатываются инструкции по охране труда? Кто их должен согласовывать и утверждать? Для всех ли работников они должны разрабатываться?
Работодатель должен обеспечить наличие инструкций по охране труда по всем должностям и видам работ. Их составление, как правило, поручается руководителям структурных подразделений. Инструкции согласовываются с профсоюзным органом, утверждаются работодателем и доводятся до работников под подпись.
Их составление, как правило, поручается руководителям структурных подразделений. Инструкции согласовываются с профсоюзным органом, утверждаются работодателем и доводятся до работников под подпись.
Обоснование. Согласно абз. 22 ч. 2 ст. 212 ТК РФ работодатель обязан обеспечить, среди прочего, разработку и утверждение правил и инструкций по охране труда для работников. Поручить составление инструкций работодатель может специализированным организациям либо своим работникам, как правило руководителям структурных подразделений. В любом случае обязанность по разработке инструкций следует включить в должностную инструкцию работника.
Согласно Методическим рекомендациям по разработке инструкций по охране труда, утвержденным Минтрудом РФ 13.05.2004 (далее — Рекомендации), инструкция по охране труда для работника разрабатывается на основе межотраслевой или отраслевой типовой инструкции по охране труда (а при ее отсутствии — межотраслевых или отраслевых правил по охране труда), требований безопасности, изложенных в эксплуатационной и ремонтной документации организаций — изготовителей оборудования, а также в технологической документации организации с учетом конкретных условий производства.
Также можно воспользоваться Методическими рекомендациями по разработке государственных требований охраны труда, утвержденными Постановлением Минтруда РФ от 17.12.2002 N 80.
Инструкции по охране труда разрабатываются как на отдельные профессии, так и на определенные виды работ.
Разработка инструкции по охране труда для работников осуществляется на основании приказа работодателя.
Как и любой другой локальный нормативный акт, инструкция по охране труда может быть согласована, например, с юридической службой, службой охраны труда и другими заинтересованными лицами исходя из порядка согласования локальных нормативных актов, установленного в организации.
При этом ст. 212 ТК РФ предусмотрена обязанность по согласованию инструкций и правил по охране труда с соответствующим профсоюзным или иным представительным органом в порядке ст. 372 ТК РФ. Отметка о согласовании с профсоюзом делается на титульном листе. Также необходимо указать и дату принятия инструкции, поскольку в силу Рекомендаций не реже одного раза в пять лет инструкции должны пересматриваться.
Если инструкция согласована с профсоюзом, она утверждается работодателем.
Инструкции по охране труда должны быть составлены по всем должностям, профессиям и видам работ, поскольку за отсутствие инструкции работодатель может быть привлечен к административной ответственности в соответствии со ст. 5.27 КоАП РФ.
Работник должен быть ознакомлен с инструкцией под подпись.
Форма приказа на утверждение инструкций по охране труда
Бадагуев, юрист, член Союза журналистов России 14 В соответствии со статьей ТК РФ работодатель обязан обеспечить разработку и утверждение правил и инструкций по охране труда для работников с учетом мнения выборного органа первичной профсоюзной организации или иного уполномоченного работниками органа. Порядок разработки инструкций по охране труда устанавливается Методическими рекомендациями по разработке инструкций по охране труда, утвержденными Министерством труда и социального развития РФ 13 мая г.
Дорогие читатели! Наши статьи рассказывают о типовых способах решения юридических вопросов, но каждый случай носит уникальный характер.
Если вы хотите узнать, как решить именно Вашу проблему – обращайтесь в форму онлайн-консультанта справа или звоните по телефонам, представленным на сайте. Это быстро и бесплатно!
образец приказа о введении в действие инструкций по охране труда.

Сразу ответим на главный вопрос: приказ лучше выпустить. Хотя действующие нормативные акты не утверждают, что издавать его необходимо, наличие такого локального документа лишним не будет.
В нем содержатся все необходимые рекомендации, порядок разработки, согласования, утверждения, учета, выпуска, распространения ЛНА по ОТ на предприятии. Образец приказа об утверждении инструкций по охране труда. Другие обязательные документы. Важность приказа об утверждении перечня инструкций по охране труда в том, что он дает возможность эффективно контролировать наличие необходимых документов и, как следствие, соблюдать требования к ОТ, которые выдвигает законодательство.
К тому же его выпуск позволит сэкономить время. Никакой обязательной формы до сих пор не утверждено, как и нет рекомендованного бланка. При составлении этой бумаги придется руководствоваться общими правилами оформления, которые приняты в организации. Тем не менее, вы можете скачать примерный образец приказа об утверждении перечня инструкций по охране труда, чтобы на его основе выпустить собственный документ.
Найдите нужный вам образец документа по охране труда в самой полной библиотеке шаблонов Справочной системы “Охрана труда”. Наши эксперты подготовили уже шаблонов! Предписания Министерства труда РФ гласят, что работодатель обязан разрабатывать инструкции по ОТ , исходя из тех профессий и видов работ, которые существуют на его предприятии.
Задача по выпуску соответствующего приказа тоже ложится на работодателя. Это может быть руководитель, его секретарь, специалист по ОТ. При этом должно быть учтено мнение первичной профсоюзной организации на предприятии, а также требования, которые изложены в Методических рекомендациях Минтруда России от Утверждение инструкций по охране труда руководителем может происходить в отдельности, либо утверждается приказ, в котором будет содержаться их полный перечень.
Важно помнить, что за хранение самих ИОТ , а также их перечня отвечает руководитель структурного подразделения. Он же должен обеспечить доступ к ним для каждого работника.
Не стоит забывать про журналы учета инструкций и учета их выдачи. Ответственность за их ведение, хранение также несет глава структурного подразделения. В справочной Системе “Охрана труда”. Поговорим о том, как правильно составить этот документ. Его шапка будет абсолютно стандартной: название организации, наименование самого документа, дата, регистрационный номер, место составления.
После этого необходимо прописать заголовок, а затем переходить непосредственно к тексту. Он будет состоять из констатирующей и распорядительной частей. В первой нужно перечислить причины выпуска, а также предоставить ссылки на нормативные акты, служащие основанием для его подготовки. Для большей наглядности эту часть лучше разделить на пункты, пронумерованные арабскими цифрами с точками. В каждом из них содержится предписываемое действие подготовить, обеспечить, организовать. Далее идет утверждаемый перечень ИОТ по профессиям для слесарей-сантехников , для электросварщиков, для уборщиков и так далее.
Далее идет утверждаемый перечень ИОТ по профессиям для слесарей-сантехников , для электросварщиков, для уборщиков и так далее.
В самом конце ставится подпись. Важно отметить, что при составлении самих инструкций нужно придерживаться одного плана.
Каждая из них должна состоять из следующих разделов:. Все права защищены. Это бесплатно и займет всего одну минуту! Вам станут доступны для скачивания более форм и образцов документов. Электронные сервисы помогут сдать отчетность без ошибок. О портале Ввести код доступа Подписка 8 А еще Статьи Инструкция по охране труда. Приказ об утверждении инструкций по охране труда. Темы: Инструкция по охране труда. Для чего оформляется приказ об утверждении инструкции по охране труда Сразу ответим на главный вопрос: приказ лучше выпустить.
Скачайте документы из статьи: Образец приказа об утверждении инструкций по охране труда. DOC Другие обязательные документы. Читайте по теме в электронном журнале.
Анастасия Бакулина – Главный редактор сайта Trudohrana. Скачайте образцы нужных документов, которые подготовили для вас наши эксперты: Предписание специалиста по охране труда. Список контингента работников, подлежащих медицинским осмотрам. Не пропустите! Попробуйте совершенно бесплатно Систему Охрана труда. Готовые решения по действующему законодательству Более 3 заполненных шаблонов Возможность задать вопрос в экспертную поддержку.
Скачайте образцы нужных документов, которые подготовили для вас наши эксперты: Предписание специалиста по охране труда. Список контингента работников, подлежащих медицинским осмотрам. Не пропустите! Попробуйте совершенно бесплатно Систему Охрана труда. Готовые решения по действующему законодательству Более 3 заполненных шаблонов Возможность задать вопрос в экспертную поддержку.
Узнать подробнее. Читайте также 5 ситуаций, когда сотрудников забывают обучить охране труда Инструкция по охране труда для кладовщика Кто разрабатывает инструкции по охране труда в организации.
Обзор изменений законодательства Электронные сервисы, с которыми без ошибок сдадите январские отчеты по охране труда Новый регламент проверок ГИТ: поблажки и неприятные сюрпризы для работодателя Приказы по охране труда: как разработать и когда обновить Как провести оценку профессиональных рисков Аттестация по промбезопасности: как организовать по новым правилам. Оформить бесплатный доступ. Правовая база. Налоговый кодекс Гражданский кодекс.
Опрос недели. Как вы считаете, установка вендингового оборудования для выдачи СИЗ сократит трудозатраты? Да, точно сократит. На нашем предприятии успешно используем вендинговые автоматы. Да, сократит. Хотелось бы их установить у нас в организации. Нет, с этими автоматами работы только прибавится. Я не знаю, как выдавать СИЗ с помощью вендингового оборудования. Новости по теме. Минтруд уточнил, можно ли оформлять журналы инструктажей не по ГОСТу. Программы обучения и инструктажей по охране труда дополнят новым модулем.
Вводный инструктаж по охране труда может проводить назначенный работник. Статьи по теме. Типовые инструкции по охране труда – как применять. Инструкция по охране труда при работе на персональном компьютере Журнал учета присвоения 1 группы по электробезопасности неэлектротехническому персоналу. Перечень инструкций по охране труда.
Инструкция по охране труда для офисных работников. Вопросы по теме. При переводе инженера-технолога из отдела главного металлурга инженером-технологом в цех гальванопокрытий обязателен ли будет вводный инструктаж по охране труда?
Как проводить вводный инструктаж для подрядчиков? На каком основании разрабатываются программы проведения инструктажей на рабочих местах? Кто может заменить ответственного работника за инструктажи по ОТ в бухгалтерии? Где взять программу дублирования оператора котельной, аппаратчика ХВО, машиниста насосных установок? Получить демодоступ или сразу подписаться.
Мобильная версия Контакты Обратная связь Рекламодателям Интернет-магазин Официальные представители Политика по обработке персональных данных. Нарушение авторских прав влечет за собой ответственность в соответствии с законодательством РФ. Настоящий сайт не является средством массовой информации. Мы в соцсетях. У меня есть пароль.
Пароль отправлен на почту Ввести. Введите эл. Неверный логин или пароль. Неверный пароль. Введите пароль. Я тут впервые. Пройдите простую регистрацию за одну минуту и получите бесплатный доступ к прочтению материала прямо сейчас.
Приказ по инструкциям по охране труда
Приказ об утверждении инструкций по охране труда для работников. При утверждении документа должностным лицом гриф утверждения должен состоять из слова УТВЕРЖДАЮ реквизит без ковывек , наименования должности лица, утверждающего документ, личной подписи, её расшифровки и даты утверждения. Главный реквизит при утверждении это дата, которая должна полностью проставляться от руки руководителем, это — число, месяц и год.
Главный реквизит при утверждении это дата, которая должна полностью проставляться от руки руководителем, это — число, месяц и год.
Образец журнала трехступенчатого контроля по охране труда. Удостоверение о проверке знаний требований охраны труда. Инструкция по охране труда.
Разработка инструкций и правил по охране труда согласно ст. Согласно этого НПА:. Пунктом 5. Инструкция может быть продлена на следующий срок только в том случае, если условия труда работника, для которого она разрабатывалась, не изменились — п. Методических рекомендаций.
Приказ об утверждении инструкций по охране труда
Подписка 8 Подпишитесь по акции на журнал. У некоторых специалистов по ОТ нередко возникает вопрос: как правильно оформить приказ об утверждении инструкций по охране труда, и нужно ли вообще это делать? Мы постараемся разобраться в ситуации, объяснить тонкости подготовки этого документа. Кроме того, в статье вы найдете готовый образец. Сразу ответим на главный вопрос: приказ лучше выпустить. Хотя действующие нормативные акты не утверждают, что издавать его необходимо, наличие такого локального документа лишним не будет. В нем содержатся все необходимые рекомендации, порядок разработки, согласования, утверждения, учета, выпуска, распространения ЛНА по ОТ на предприятии.
Кроме того, в статье вы найдете готовый образец. Сразу ответим на главный вопрос: приказ лучше выпустить. Хотя действующие нормативные акты не утверждают, что издавать его необходимо, наличие такого локального документа лишним не будет. В нем содержатся все необходимые рекомендации, порядок разработки, согласования, утверждения, учета, выпуска, распространения ЛНА по ОТ на предприятии.
Приказ об утверждении инструкций по охране труда для работников
Приложение На основании п. Методических рекомендаций по разработке государственных нормативных требований по охране труда, утвержденных постановлением Министерства труда и социального развития Российской Федерации от В соответствии с п. Методических рекомендаций по разработке государственных нормативных требований охраны труда, утвержденных постановлением Министерства труда и социального развития Российской Федерации от
.
.
.
.
Каждый работодатель обязан издать приказ об утверждении инструкций по охране труда. Как его оформить? Приводим образец.
.
.
.
.
.
.
Департамент труда и производственных отношений
Формы
Детский труд/разрешение на работу несовершеннолетних
- CL-1 Заявление о детском труде (для несовершеннолетних в возрасте 14 и 15 лет)
- eCL-3 Онлайн-заявление о детском труде (для 16- и 17-летних работников)
Формы работодателя
- UC-1 Отчет для определения ответственности в соответствии с Законом Гавайев о гарантии занятости
Используйте эту форму, чтобы зарегистрировать свой бизнес в Отделе страхования на случай безработицы при приеме на работу.
- LIR#27 Заявление на получение сертификата соответствия разделу 3-122-112, HAR
- UC-25 Уведомление об изменениях
- UC-86 Отказ от трудовой книжки работодателя
- *UC-B6 Ежеквартальный отчет об оценке заработной платы, взносов, занятости и обучения
(*Недоступно в Интернете — для получения помощи звоните по телефону 586-8915 или 586-8916)
Отпуск по семейным обстоятельствам
- HFLL-1 Факультативная форма для подтверждения серьезного состояния здоровья поставщиком медицинских услуг
Апелляционный совет по трудовым и производственным отношениям на Гавайях
- LIRAB 1 – Первоначальное заявление конференции
- LIRAB 2 – Уведомление о неуслышанном движении
- LIRAB 3 – Уведомление о слушании
- LIRAB 4 – Идентификация безымянного свидетеля
- LIRAB 5 – Опознание живого свидетеля
- LIRAB 6 – Уведомление об апелляции
- LIRAB 7 – Соглашение о продолжении конференции
- LIRAB 8 – Сертификат обслуживания
- LIRAB 9 – Положение о временном заключении под стражу
- LIRAB 10 – Отзыв апелляции
- LIRAB 11 – Положение о роспуске партии
- LIRAB 12 – Запрос приказа о протоколе судебного заседания
- LIRAB 13 – Назначение представителя
- LIRAB 14 – Положение об отказе от раскрытия информации и судебного разбирательства
- LIRAB 15 – Запрос об утверждении гонорара адвоката
Совет по трудовым отношениям Гавайев
- HLRB 1 Заявление о сертификации
- HLRB 2 Ходатайство о разъяснении или изменении соответствующей единицы переговоров
- HLRB 3 Заявление об отказе от сертификации
- HLRB 4 Жалоба на запрещенные действия
- HLRB 5 Ходатайство о пересмотре возмещения
- HLRB 6 Заявление о возражениях против проведения выборов
- HLRB 7 Петиция, касающаяся финансового отчета организации сотрудников
- HLRB 8 Ходатайство об определении подразделения CB и избрании
- HLRB 9 Петиция о референдуме
- HLRB 10 Заявление об отказе от сертификации
- HLRB 11 Жалоба на недобросовестную трудовую практику
- HLRB 12 Ходатайство о принятии декларативного решения
- HLRB 13 Ходатайство о вмешательстве
- HLRB 14 Заявление о выдаче повестки в суд
- HLRB 15 Повестка в суд
- HLRB 16 Повестка в суд Duces Tecum
- HLRB 17 Образец формы заявления для первоначальной конференции HIOSH
Отдел охраны труда и здоровья на Гавайях
- Форма заявки на участие в Консультативном совете
- Котлы и лифты
- Сертификат пригодности для взрывчатых веществ
- Сертифицированный специалист по безопасности и охране здоровья
- Консультативный совет операторов подъемных машин
Гавайская комиссия по гражданским правам
- ФОРМА PCQ-Employment: Анкета для подачи жалобы Employment
- ФОРМА PCQ-Доступ к государственным/финансируемым услугам : Анкета для подачи жалобы
- ФОРМА PCQ-Общественное размещение : Анкета для подачи жалобы
- ФОРМА PCQ-Сделка с недвижимостью : Анкета для подачи жалобы
Персонал
Здравоохранение с предоплатой
- HC-4 Опросник медицинского страхования
- HC-5 Уведомление работника работодателю
- HC-6 Мелкие работодатели, подлежащие PHC/требованиям работодателя о доплате к страховым взносам
- HC-61 Заявление на получение разрешения на самострахование
Государственная пожарная служба
- SFC 1-99 Отчет о пожарной инспекции
Страхование временной нетрудоспособности
- TDI-14 Таблицы эквивалентности
- TDI-15 Подтверждение и соглашение о плане самострахования TDI
Страхование от безработицы (работодатели)
- LIR#27 Заявление на получение сертификата соответствия разделу 3-122-112 HAR (используйте эту форму, чтобы запросить налоговую очистку от Министерства труда и производственных отношений для получения наград за профессиональные услуги)
- UC-1 Отчет для определения ответственности в соответствии с Законом о гарантиях занятости Гавайских островов
Используйте эту форму, чтобы зарегистрировать свой бизнес в Отделе страхования на случай безработицы при приеме на работу.
- *UC-B6 Ежеквартальный отчет об оценке заработной платы, взносов, занятости и обучения (*Недоступно в Интернете – для получения помощи звоните по телефону 586-8915 или 586-8916)
- UC-25 Уведомление об изменениях (используйте эту форму, чтобы уведомить Отдел страхования по безработице о любых изменениях адреса или статуса работодателя)
- UC-336 Выбор семейной корпорации для исключения из страхового покрытия В соответствии с разделом 383-7(20) HRS (Используйте эту форму, чтобы выбрать исключение из страхового покрытия по безработице для семейной корпорации)
- UC-347 Уведомление о приобретениях или передачах (используйте эту форму, чтобы сообщать о приобретениях или передачах в соответствии с Разделом 383-66(b) HRS, если между нанимающими подразделениями, перевод между единицей-работодателем и лицом, не являющимся единицей-работодателем.Департамент будет определять по существу общую собственность, управление или контроль.
 Все стороны, участвующие в приобретении или передаче, должны заполнить форму отдельно.
Все стороны, участвующие в приобретении или передаче, должны заполнить форму отдельно. - UC-348 Информация о частичной безработице (Информация для заявителей и работодателей об определении, оценке и установлении частичной безработицы. Также включает форму «Подтверждение статуса частичной безработицы» для работодателей, чтобы они могли конкурировать и возвращаться, чтобы подтвердить частичную безработицу своего работника. статус.Эта форма должна быть заполнена в течение 5 рабочих дней с даты подачи заявки.)
- UC-86 Отказ от сведений об опыте работы работодателя (используйте эту форму, чтобы запросить получение сведений об опыте предыдущего работодателя)
- Самофинансирование некоммерческих организаций (НКО)
Некоммерческие организации (религиозные, благотворительные и образовательные), имеющие право на освобождение от подоходного налога в соответствии с Разделом 501(c)(3) Налогового кодекса, могут подать заявление на освобождение от уплата взносов путем запроса статуса самофинансирования в соответствии с положениями главы 383-62 (d) Закона о гарантии занятости Гавайских островов. Индийские племена или племенные единицы могут выбрать самофинансирование.
Индийские племена или племенные единицы могут выбрать самофинансирование.
Страхование по безработице (заявители по безработице)
- UC-BP-1SAB Форма ручной подачи заявления на получение государственных дополнительных пособий (SAB) 2016. Эта программа начинается 4 сентября 2016 г. и заканчивается 28 октября 2017 г.
- UC-253 Запись рабочих контактов.
- UC-161(a) Инструкции по частичной и частичной подаче истцом требования в Интернете.В дополнение к подаче еженедельного или двухнедельного подтверждения заявки ваш работодатель должен подать «Еженедельный отчет о низком заработке», чтобы подтвердить ваш заработок, готовность к работе и продолжение занятости за каждую неделю, на которую вы заявляете.
- UC-226 Проверка регистрации в реферальном союзе. Если вы сообщаете, что получите работу через направляющий профсоюз, попросите уполномоченного представителя профсоюза заполнить и отправить эту форму в местный отдел по рассмотрению заявлений в течение 7 календарных дней после подачи заявления.

- UC-275 Заявление об отзыве претензии
- UC-348 Информация о частичной безработице (Информация для заявителей и работодателей об определении, оценке и установлении частичной безработицы. Также включает форму «Подтверждение статуса частичной безработицы» для работодателей, чтобы они могли конкурировать и возвращаться, чтобы подтвердить частичную безработицу своего работника. Эта форма должна быть заполнена в течение 5 рабочих дней с даты подачи заявки.)
Компенсация работникам
- WC-1 Отчет работодателя о производственном травматизме
- WC-2 Отчет врача
- WC-5 Заявление работника о компенсации работникам
- WC-5A Требование компенсации иждивенцев
- WC-14 Отчет о заработной плате сотрудника
- WC-21 Заявление на получение разрешения на самострахование
- WC-77 Заявление о слушании
- WC-77a Ответ на заявление о проведении слушания
- LIR#27 Заявление на получение сертификата соответствия разделу 3-122-112, HAR
Использование респираторов, одобренных NIOSH | НПТЛ | NIOSH
Остерегайтесь покупателя
Информация о средствах защиты органов дыхания
NIOSH предоставляет рекомендации пользователям в информационных уведомлениях о средствах защиты органов дыхания. Эти уведомления включают рекомендации по таким темам, как инструкции для пользователя и снижение производительности продукта. Кроме того, NIOSH предоставляет список уведомлений для пользователей респираторов, выпущенных производителями, чтобы информировать пользователей о потенциальных рисках или условиях, существующих с респираторами, одобренными NIOSH. Пользователи и покупатели могут также обратиться к веб-сайту производителя за уведомлениями для пользователей, касающимися их продуктов.
Эти уведомления включают рекомендации по таким темам, как инструкции для пользователя и снижение производительности продукта. Кроме того, NIOSH предоставляет список уведомлений для пользователей респираторов, выпущенных производителями, чтобы информировать пользователей о потенциальных рисках или условиях, существующих с респираторами, одобренными NIOSH. Пользователи и покупатели могут также обратиться к веб-сайту производителя за уведомлениями для пользователей, касающимися их продуктов.
Поддельные респираторы / искажение утверждения NIOSH
Поддельные респираторы сами по себе не проходили тестирование и оценку NIOSH, а были специально изготовлены для имитации респиратора, получившего одобрение NIOSH.Искажение утверждения NIOSH происходит, когда продукт респиратора ложно рекламируется и продается как одобренный NIOSH. Оба типа продуктов могут быть не в состоянии обеспечить надлежащую защиту органов дыхания работникам. При получении сообщений о подделке или искажении информации NIOSH размещает информацию об этих респираторах на веб-странице «Поддельные респираторы / искажение сведений об одобрении NIOSH», чтобы предупредить пользователей, покупателей и производителей.
NIOSH известно о ложном использовании таких терминов, как «одобрено NIOSH» и «NIOSH N95» на упаковке респираторов.Поэтому работодатели и пользователи респираторов должны использовать список сертифицированного оборудования NIOSH или список утвержденных NIOSH респираторов с фильтрующей маской, чтобы убедиться, что респираторы одобрены NIOSH. Кроме того, важно убедиться, что название модели продукта и номер разрешения NIOSH соответствуют списку сертифицированного оборудования.
Маркировка и таблички с разрешениями
Некоторые продукты могут выглядеть очень похожими на респираторы, одобренные NIOSH. Однако есть два основных способа идентифицировать респираторы, одобренные NIOSH: номер одобрения NIOSH и ярлык одобрения .Все респираторы, одобренные NIOSH, имеют номер утверждения. С 2008 года NIOSH требует, чтобы владельцы разрешений размещали номер разрешения (например, TC 84A-XXXX) на лицевой части респиратора или ремнях. На рис. 1 показан пример правильной маркировки FFR, одобренного NIOSH.
В дополнение к номеру одобрения респираторы, одобренные NIOSH, имеют этикетку одобрения, расположенную на упаковке респиратора или внутри нее. Этикетка одобрения NIOSH содержит контактную информацию производителя, предостережения и ограничения по использованию, а также указания по правильному использованию.На рис. 2 показан пример этикетки одобрения NIOSH.
Принудительный труд | Служба таможенного и пограничного контроля США
Январь объявлен Национальным месяцем предотвращения торговли людьми
31 декабря 2021 года президент Байден издал указ президента о проведении в январе 2022 года Национального месяца предотвращения торговли людьми.
Принудительный труд – это нарушение прав человека, которое наносит ущерб уязвимым работникам, законопослушным предприятиям и потребителям. Соединенные Штаты не потерпят принудительного труда в наших цепочках поставок и будут продолжать выступать против жестокой и бесчеловечной практики труда.CBP является мировым лидером в области принудительного труда, установив рекорды по принудительному труду за последние два года. CBP является мировым лидером в области принудительного труда и разработала надежную программу гражданских расследований для выявления и предотвращения ввоза в Соединенные Штаты товаров, изготовленных с использованием принудительного труда.
CBP является мировым лидером в области принудительного труда и разработала надежную программу гражданских расследований для выявления и предотвращения ввоза в Соединенные Штаты товаров, изготовленных с использованием принудительного труда.
Мы выполнили некоторые из наших основных ресурсов, чтобы предоставить моментальную картину принудительного труда CBP. Изучите ниже, чтобы узнать больше.
Информация и ресурсы для общественности
CBP борется с принудительным трудом
Расследования и заявления о принудительном труде – Как написать заявление о принудительном труде
Что такое принудительный труд?
CBP определяет принудительный труд как любую работу или услугу, требуемую от какого-либо лица под угрозой какого-либо наказания за ее невыполнение, и для которой работник не предлагает работу или услугу добровольно.Наемный труд определяется как работа или услуга, выполняемая в соответствии с контрактом, принудительное исполнение которого может быть достигнуто посредством процесса или штрафов. Это включает принудительный или кабальный детский труд.
Это включает принудительный или кабальный детский труд.
Процесс принудительного труда CBP
Как CBP решает проблему принудительного труда?
CBP применяет Раздел 307 Закона о тарифах от 1930 г. (19 USC §1307) путем издания приказов об удержании выпуска (WRO) и выводов, чтобы предотвратить ввоз в страну товаров, полностью или частично произведенных в иностранном государстве с использованием принудительного труда. Соединенные Штаты.
CBP отвечает за предотвращение попадания на рынок США товаров, изготовленных с использованием принудительного труда, путем расследования и принятия мер в связи с заявлениями о принудительном труде в цепочках поставок.
Руководство Юридического центра по борьбе с торговлей людьми за июнь 2020 г., Свобода импорта: использование Закона США о тарифах для борьбы с принудительным трудом в цепочках поставок , может использоваться, чтобы помочь торговому сообществу усилить петиции в CBP, и является одним из нескольких предлагаемых инструментов бороться с принудительным трудом.
Приостановление распоряжения о выдаче и списка выводов
Подлежат ли ваши импортные товары WRO или заключению? Проверьте список приказов об удержании и выводах для получения информации о любых товарах, которые могут подлежать исключению и/или конфискации.Вы обязаны быть в курсе своей деятельности в цепочке поставок.
Правоприменительные меры
Статистика принудительного труда на 31 декабря 2021 г.* (публикуется ежеквартально)
Каковы показатели принудительного труда?
Перечисленные ниже показатели были разработаны Международной организацией труда. Они предназначены для оказания помощи «передовым» сотрудникам уголовных правоохранительных органов, инспекторам, профсоюзным деятелям, работникам НПО и другим лицам в выявлении лиц, которые, возможно, попали в ловушку принудительного труда и которым может потребоваться срочная помощь.Эти индикаторы представляют собой наиболее распространенные признаки, указывающие на возможное существование случая принудительного труда.
Показатели МОТ о принудительном труде
Изображения выше получены с помощью Adobe Stock.
Ссуды на эксплуатацию фермы
Прямые ссуды на эксплуатацию фермы FSA являются ценным ресурсом для открытия, содержания и укрепления фермы или ранчо. Для новых сельскохозяйственных производителей прямые ссуды на содержание ферм FSA обеспечивают важный доступ к сельскохозяйственному производству, финансируя расходы на эксплуатацию фермы.При максимальной сумме кредита в размере 400 000 долларов США все прямые операционные кредиты FSA финансируются и обслуживаются Агентством через местных кредитных специалистов и управляющих фермерскими кредитами. Финансирование поступает из ассигнований Конгресса в рамках бюджета Министерства сельского хозяйства США.
*Все заявки на прямой кредит FSA требуют одних и тех же основных форм.
Одновременные заявки на прямой кредит в собственность фермы и прямой операционный кредит должны быть объединены в одной форме заявки на кредит.
Когда вы встретитесь с сотрудниками программы кредитования фермерских хозяйств округа FSA, вам будет предложено заполнить дополнительные формы в соответствии с применимыми требованиями программы кредитования для данного типа кредита.
Часто задаваемые вопросы
Цели кредита
Операционные кредиты должны быть необходимы для успеха сельскохозяйственной деятельности и только для следующих целей:
- Затраты, связанные с реорганизацией фермы для повышения прибыльности, например:
- приобретение оборудования для перехода от традиционного производства к нулевой обработке почвы
- переход от выращивания откорма к выращиванию коров и телят
- переход от выращивания пропашных культур к производству овощей
- приобретение оборудования для сушки и хранения зерна для улучшения сбыта кооперативы по переработке и сбыту продукции с добавленной стоимостью
Максимальные ограничения по кредиту
Максимальная сумма кредита для прямого кредита на эксплуатацию фермы составляет 400 000 долларов США. Требований по первоначальному взносу нет.
Требований по первоначальному взносу нет.
Условия погашения
Условия погашения кредита Direct Farm Operating варьируются в зависимости от цели кредита, платежеспособности соискателя кредита и прогнозируемого дохода. Общие операционные расходы и расходы на проживание семьи обычно подлежат уплате в течение 12 месяцев или после продажи сельскохозяйственной продукции. Для более крупных покупок, таких как оборудование, мелкий ремонт или домашний скот, срок не будет превышать 7 лет.
Процентная ставка
Взимаемая процентная ставка всегда представляет собой более низкую ставку, действующую на момент утверждения или закрытия кредита для желаемого типа кредита.Процентные ставки рассчитываются и публикуются 1 числа каждого месяца.
Критерии приемлемости
Существует 2 различных типа квалификаций, которым необходимо соответствовать:
- приемлемое фермерское предприятие
- общие квалификационные требования
Во-первых, деятельность должна быть правомочным фермерским предприятием. Средства операционного кредита не могут использоваться для финансирования несельскохозяйственных предприятий, таких как экзотические птицы, тропические рыбы, собаки или лошади, используемые для несельскохозяйственных целей (скачки, развлечения, шоу и питание).
Средства операционного кредита не могут использоваться для финансирования несельскохозяйственных предприятий, таких как экзотические птицы, тропические рыбы, собаки или лошади, используемые для несельскохозяйственных целей (скачки, развлечения, шоу и питание).
Общие квалификационные требования включают:
- отсутствие судимостей на федеральном уровне или штате за посадку, культивирование, выращивание, производство, сбор, хранение, торговлю или владение контролируемыми веществами
- юридическую способность брать на себя ответственность за кредит обязательство
- приемлемая кредитная история
- быть гражданином Соединенных Штатов, негражданином или законным резидентом Соединенных Штатов, включая Пуэрто-Рико, Виргинские острова США, Гуам, Американское Самоа и некоторые бывшие тихоокеанские подопечные территории
- отсутствие предыдущего прощения долга Агентством, включая выплату гарантийных убытков по кредиту
- невозможность получить достаточный кредит в другом месте, с гарантией кредита FSA или без нее
- отсутствие просрочки по федеральному долгу, кроме налогового долга IRS, на момент закрытие кредита
- отсутствие права на участие из-за дисквалификации в результате нарушения Федерального страхования урожая 900 11 обладают достаточными управленческими способностями, чтобы обеспечить разумное ожидание погашения кредита
Пояснение к «управленческим способностям»
Управленческие способности демонстрируются Агентству посредством любого сочетания образования, обучения на рабочем месте и опыта работы на ферме или выполнив хотя бы 1 из этих критериев. Требуемый уровень управленческих способностей будет зависеть от сложности операции и суммы запроса на получение кредита. Каждая заявка оценивается в индивидуальном порядке.
Требуемый уровень управленческих способностей будет зависеть от сложности операции и суммы запроса на получение кредита. Каждая заявка оценивается в индивидуальном порядке.
Образование:
- 4 года обучения в колледже или высшее образование в области, связанной с сельским хозяйством
- 2 года обучения в техническом колледже в области, связанной с сельским хозяйством Служба, местный колледж, профессиональная сельскохозяйственная программа для взрослых или университет с земельным грантом
- успешное завершение местных, национальных, некоммерческих или аналогичных программ сельскохозяйственных семинаров
- профессиональные или общие занятия по сельскому хозяйству в средней школе в дополнение к работе на ферме и участие и успешное завершение сельскохозяйственных проектов в 4-H, FFA, племенных молодежных организациях, Grange Youth или другом сельскохозяйственном членском клубе
Обучение на рабочем месте:
- работает или недавно работал наемный сельскохозяйственный труд с управленческими обязанностями (принятие повседневных решений)
- завершение или недавно выполненное завершили программу наставничества, стажировки или ученичества на ферме с упором на требования к управлению и повседневные решения на ферме
- участие или недавно участие в городских или поддерживаемых сообществом сельскохозяйственных программах, которые включают базовое сельскохозяйственное обучение
Опыт работы на ферме:
- владелец, управляющий или оператор сельскохозяйственного предприятия в течение как минимум 1 полного производственно-сбытового цикла в течение 5 лет с даты подачи заявки на получение кредита и маркетинговый цикл с обязанностями, связанными с управлением культурами и полями, здоровьем скота, надзором за племенным выращиванием, управлением трудом или наймом, или общим управлением фермой производственно-сбытового цикла
- получено и успешно погашено в минимум 1 Молодежный кредит FSA
Основы кредитного рейтинга
FSA не использует кредитный рейтинг. Ожидается, что соискатели кредита будут иметь приемлемую историю погашения с другими кредиторами, включая федеральное правительство. Заявители на получение ссуды не дисквалифицируются автоматически в случае единичных случаев несвоевременных платежей; отсутствие кредитной истории; или если можно доказать, что любые недавние нежелательные кредитные проблемы были временными и неподконтрольными заявителю на получение ссуды. «Нет истории» кредитной операции соискателя кредита автоматически не указывает на неприемлемую кредитную историю.
Ожидается, что соискатели кредита будут иметь приемлемую историю погашения с другими кредиторами, включая федеральное правительство. Заявители на получение ссуды не дисквалифицируются автоматически в случае единичных случаев несвоевременных платежей; отсутствие кредитной истории; или если можно доказать, что любые недавние нежелательные кредитные проблемы были временными и неподконтрольными заявителю на получение ссуды. «Нет истории» кредитной операции соискателя кредита автоматически не указывает на неприемлемую кредитную историю.
Техническая помощь
Многие ответы можно найти в нашей брошюре «Ваш путеводитель по фермерским кредитам FSA» (pdf, 2.53 МБ). Также рекомендуется позвонить и договориться о встрече с ближайшим сотрудником по кредитованию фермы или менеджером по кредитованию фермы. Должностные лица агентства обязаны:
- помогать заявителям на получение кредита заполнять формы FSA и собирать информацию, необходимую для заполнения заявки;
- объясните процедуру подачи заявки, процесс и требования к полной заявке;
- помогать заявителям на получение кредита в заполнении форм FSA и определении источников информации, необходимой для заполнения заявки, если требуется помощь;
- информируйте соискателей кредита о других поставщиках технической помощи, которые могут оказать помощь за минимальную плату или бесплатно.
 Некоторые примеры включают, помимо прочего, Кооперативную службу распространения знаний, некоммерческие организации и учреждения, Межплеменной сельскохозяйственный совет и другие подобные организации; и
Некоторые примеры включают, помимо прочего, Кооперативную службу распространения знаний, некоммерческие организации и учреждения, Межплеменной сельскохозяйственный совет и другие подобные организации; и - информируют заявителей об альтернативах, которые помогут преодолеть любые возможные барьеры на пути к признанию правомочным на получение кредита FSA.
Предложения для первой встречи с FSA
- Имейте общее представление о том, что вы хотите сделать, и будьте в состоянии определить свои цели.Какой тип операции у вас есть или вы хотите сделать? Что вам нужно, чтобы управлять этой фермой или ранчо? Как вы будете продвигать свой продукт? Сколько тебе нужно? Каковы ваши прогнозы?
- Хорошее ведение документации очень важно. Если у вас нет систематизированных записей, рекомендуется попытаться представить все свои доходы и расходы в понятном формате. Это не должно быть причудливым. Кроме того, то, что происходит внутри дома, так же важно, как и потребности вашего бизнеса.
 Такие расходы, как еда, одежда, ипотека или аренда, страховка, налоги, медицинские расходы, платежи по кредитным картам, расходы на образование и другие потребительские долги, являются частью расчетов плана фермы.Знайте свои расходы. Возьмите с собой свои записи.
Такие расходы, как еда, одежда, ипотека или аренда, страховка, налоги, медицинские расходы, платежи по кредитным картам, расходы на образование и другие потребительские долги, являются частью расчетов плана фермы.Знайте свои расходы. Возьмите с собой свои записи. - Не забудьте взять с собой любые финансовые отчеты, которые могут включать налоговые декларации, для самого последнего производственного цикла, чтобы помочь в прогнозировании движения денежных средств для вашего предложения по кредиту. Если для погашения ссуды вам необходимо полагаться на доход от несельскохозяйственной деятельности, принесите несколько последних платежных квитанций.
- Возьмите с собой в офис копии любых письменных договоров аренды, если вы арендуете землю или оборудование.
- Перед подачей заявки на кредит рекомендуется проверить свой кредитный отчет.Это позволяет вам обнаружить любые ошибки или исследовательские события, которые могли негативно повлиять на ваш кредит. Закон о справедливой кредитной отчетности (FCRA) требует, чтобы каждая общенациональная кредитная компания — Equifax, Experian и TransUnion — предоставляла вам бесплатную копию вашего кредитного отчета по вашему запросу раз в 12 месяцев.
 FCRA способствует точности и конфиденциальности информации в файлах национальных кредитных компаний. Федеральная торговая комиссия (FTC), национальное агентство по защите прав потребителей, обеспечивает соблюдение FCRA в отношении компаний, предоставляющих кредитную отчетность.
FCRA способствует точности и конфиденциальности информации в файлах национальных кредитных компаний. Федеральная торговая комиссия (FTC), национальное агентство по защите прав потребителей, обеспечивает соблюдение FCRA в отношении компаний, предоставляющих кредитную отчетность.
Дополнительная информация
Мы рекомендуем вам обратиться в местный офис или в сервисный центр Министерства сельского хозяйства США, чтобы узнать больше о наших программах и информацию, которая вам понадобится для подачи полного заявления. Вы также должны быть в состоянии найти список в телефонном справочнике в разделе, предназначенном для правительственных/общественных организаций при Министерстве сельского хозяйства США, Агентство сельскохозяйственных услуг. Наши местные офисы FSA будут рады помочь вам.
| 11.01.2022 | Обзор FDA: 11 января 2022 г. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов объявило в письме о правоприменении, что оно не намерено возражать против использования определенных квалифицированных заявлений о пользе для здоровья, касающихся потребления магния и снижения риска высокого кровяного давления (гипертонии). | Пресс-релиз / публичное заявление |
| 07.01.2022 | Коронавирус (COVID-19) Обновление: FDA сокращает интервал для бустерной дозы вакцины Moderna COVID-19 до пяти месяцев Сегодня FDA внесло поправки в разрешение на экстренное использование (EUA) вакцины Moderna против COVID-19, чтобы сократить время между завершением первичной серии вакцины и бустерной дозой как минимум до пяти месяцев для лиц в возрасте 18 лет и старше. старшая. | Пресс-релиз / публичное заявление |
| 03.01.2022 | Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США предпринимает ряд действий для расширения использования вакцины Pfizer-BioNTech против COVID-19 Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) внесло поправки в разрешение на экстренное использование вакцины Pfizer-BioNTech против COVID-19, предприняв несколько действий, которые расширят использование вакцины в определенных группах населения. | Пресс-релиз / публичное заявление |
| 17.12.2021 | Коронавирус (COVID-19) Обновление Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) одобрило изменение производства для Comirnaty, включив в него состав, в котором используется другой буфер; и сокращенное применение нового препарата для повышения артериального давления у взрослых с вазодилататорным шоком, у которых сохраняется гипотензия, несмотря на прием жидкости и катехоламинов (класс нейротрансмиттеров). | Обновление COVID-19 |
| 14.12.2021 | Коронавирус (COVID-19) Обновление Информационные бюллетени Janssen COVID-19 были обновлены, чтобы включить противопоказания для людей с историей тромбоза с тромбоцитопенией после вакцины Janssen против COVID-19 или любой другой вакцины против COVID-19 с аденовирусным вектором. | Обновление COVID-19 |
09. 12.2021 12.2021 | Коронавирус (COVID-19) Обновление: FDA расширяет право на получение бустерной дозы Pfizer-BioNTech COVID-19 для 16- и 17-летних Сегодня FDA внесло поправки в разрешение на экстренное использование (EUA) вакцины Pfizer-BioNTech против COVID-19, разрешив использование одной бустерной дозы для введения лицам в возрасте 16 и 17 лет не менее чем через шесть месяцев после завершения первичной вакцинации. с вакциной Pfizer-BioNTech COVID-19. | Пресс-релиз / публичное заявление |
| 30.11.2021 | Коронавирус (COVID-19) Обновление: FDA активно работает над расследованием и устранением потенциальных последствий варианта Omicron; Призывает к вакцинации и ревакцинациям FDA сотрудничает с федеральными партнерами, международными регулирующими органами и компаниями по производству медицинских товаров, чтобы быстро устранить любые потенциальные последствия варианта омикрон. | Пресс-релиз / публичное заявление |
19. 11.2021 11.2021 | Управление по санитарному надзору за качеством пищевых продуктов и медикаментов расширяет право на использование бустеров вакцины против COVID-19 Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) внесло поправки в разрешения на использование в экстренных случаях (EUA) для вакцин Moderna и Pfizer-BioNTech против COVID-19, разрешив использование одной бустерной дозы для всех лиц в возрасте 18 лет и старше после завершения первичной вакцинации любым разрешенным FDA или одобренная вакцина против COVID-19. | Пресс-релиз / публичное заявление |
| 29.10.2021 | Коронавирус (COVID-19) Обновление FDA обсудило действия агентства по расширению использования разовой бустерной дозы для вакцин против COVID-19 в подходящих группах населения. Кроме того, FDA санкционировало 11-й безрецептурный (OTC) тест на COVID-19 и исследует некоторые импортные медицинские перчатки, которые, по-видимому, были переработаны, очищены или переработаны и проданы как новые. | Обновление COVID-19 |
| 29.10.2021 | FDA разрешает вакцину против COVID-19 детям от 5 до 11 лет Разрешение было основано на тщательной и прозрачной оценке FDA данных, которая включала вклад независимых экспертов консультативного комитета, которые подавляющим большинством голосов проголосовали за предоставление вакцины детям этой возрастной группы. | Пресс-релиз / публичное заявление |
| 26.10.2021 | Заседание Консультативного комитета по вакцинам и родственным биологическим продуктам Комитет обсудит запрос на внесение поправок в Разрешение Pfizer-BioNTech на экстренное использование (EUA) для введения их мРНК-вакцины против COVID-19 детям в возрасте от 5 до 11 лет.Посмотреть прямую трансляцию. | Событие |
| 22.10.2021 | Коронавирус (COVID-19) Обновление Сегодня FDA начало публиковать материалы для следующего заседания Консультативного комитета по вакцинам и родственным биологическим продуктам (VRBPAC), которое состоится во вторник, 26 октября. | Обновление COVID-19 |
| 20.10.2021 | FDA принимает дополнительные меры в отношении использования бустерной дозы для вакцин против COVID-19 Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) предприняло дополнительные действия в отношении бустерных доз вакцин против COVID-19, в том числе разрешило вводить гетерологичные (или «смешивать и сочетать») бустерные дозы подходящим лицам после завершения первичной вакцинации другой доступной вакциной против COVID-19. Прослушайте звонок СМИ. | Пресс-релиз / публичное заявление |
| 14.10.2021 – 15.10.2021 | Заседание Консультативного комитета по вакцинам и родственным биологическим продуктам Комитет обсудит разрешение на экстренное использование (EUA) вакцины ModernaTX Inc. | Событие |
| 01.10.2021 | FDA проведет заседания Консультативного комитета для обсуждения разрешений на экстренное использование бустерных доз и вакцин против COVID-19 для детей младшего возраста FDA объявляет о двух предстоящих заседаниях своего Консультативного комитета по вакцинам и родственным биологическим продуктам (VRBPAC) для обсуждения новых доступных данных по доступным в настоящее время вакцинам против COVID-19. | Пресс-релиз / публичное заявление |
| 01.10.2021 | Коронавирус (COVID-19) Обновление FDA выдает разрешение на экстренное использование одной дополнительной партии вакцины Janssen против COVID-19, а исполняющая обязанности комиссара FDA д-р Джанет Вудкок обсуждает разрешение на одну бустерную дозу вакцины Pfizer-BioNTech против COVID-19. | Обновление COVID-19 |
| 24.09.2021 | Обращение к заинтересованным сторонам: Бустерная доза вакцины против COVID-19 компании Pfizer-BioNTech Исполняющая обязанности комиссара FDA, Джанет Вудкок, М.D. и директор Центра оценки и исследований биологических препаратов FDA, Питер Маркс, доктор медицинских наук, обсуждают бустерную дозу вакцины Pfizer-BioNTech против COVID-19. | Подкаст / Видео |
| 22.09.2021 | FDA разрешает бустерную дозу вакцины Pfizer-BioNTech против COVID-19 для определенных групп населения FDA внесло поправки в разрешение на экстренное использование (EUA) вакцины Pfizer-BioNTech против COVID-19, чтобы разрешить использование одной бустерной дозы, которая должна быть введена не менее чем через шесть месяцев после завершения первичной серии вакцин Pfizer-BioNTech COVID-19. 19 Вакцинация некоторых групп населения. | Пресс-релиз / публичное заявление |
20. 09.2021 09.2021 | Подкаст: Бустеры вакцины против COVID-19 и вакцины против COVID-19 для детей Исполняющая обязанности комиссара FDA д-р Джанет Вудкок обсуждает дополнительные прививки вакцины против COVID-19 («бустеры») и вакцины против COVID-19 для детей до 12 лет | Подкаст / Видео |
| 17.09.2021 | Коронавирус (COVID-19) Обновление Управление по санитарному надзору за качеством пищевых продуктов и медикаментов предприняло следующие действия в рамках продолжающегося реагирования агентства на пандемию COVID-19: выпустило письмо для поставщиков медицинских услуг о возможности получения ложноположительных результатов с помощью Abbott Alinity m SARS-CoV-2 AMP и Alinity m Resp-4- Комплекты Plex AMP; пересмотрено Разрешение на экстренное использование (EUA) для бамланивимаба и этесевимаба, вводимых вместе, чтобы включить экстренное применение в качестве постконтактной профилактики COVID-19 у взрослых и детей (в возрасте 12 лет и старше с массой тела не менее 40 кг), которые с высоким риском прогрессирования COVID-19 в тяжелую форму; выпустила пересмотренное руководство, чтобы помочь расширить доступность лицевых масок, барьерных покрытий для лица и лицевых щитков для населения, включая медицинский персонал, а также хирургических масок и респираторов с фильтром для лица (FFR) (включая респираторы N95) для здравоохранения. | Обновление COVID-19 |
| 17.09.2021 | Консультативный комитет по вакцинам и родственным биологическим продуктам Консультативный комитет по вакцинам и родственным биологическим продуктам проведет открытое заседание для обсуждения вопроса о дополнительных дозах вакцин против COVID-19 и, в частности, для обсуждения заявки на получение дополнительной лицензии на биопрепараты Pfizer-BioNTech для введения третьей («бустерной») дозы Comirnaty (вакцина против COVID-19, мРНК) у лиц в возрасте 16 лет и старше.Посмотреть прямую трансляцию. | Событие |
| 10.09.2021 | Коронавирус (COVID-19) Обновление Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) утвердило сокращенную заявку на новое лекарство, предназначенное для седации первоначально интубированных и находящихся на искусственной вентиляции легких пациентов во время лечения в отделении интенсивной терапии, разрешило использование – в соответствии с разрешением на экстренное использование (EUA) для вакцины Janssen против COVID-19 – – одной дополнительной партии вакцинного лекарственного вещества, произведенного на предприятии Emergent, и выпустили пересмотренное руководство, в котором представлены общие рекомендации для потенциальных заявителей на непатентованные лекарственные средства в форме вопросов и ответов, которые были рассмотрены во время чрезвычайной ситуации в области общественного здравоохранения, связанной с COVID-19. | Обновление COVID-19 |
| 10.09.2021 | FDA будет следить за научными данными о вакцинах против COVID-19 для детей младшего возраста Руководство FDA описывает шаги, которые FDA предпримет для обеспечения безопасности и эффективности вакцин против COVID-19 для детей младшего возраста. | Пресс-релиз / публичное заявление |
| 02.09.2021 | Доктор FDAДжанет Вудкок о вакцинах и методах лечения COVID-19 Исполняющая обязанности комиссара FDA Джанет Вудкок, доктор медицинских наук, обсуждает вакцины против COVID-19 для детей, дополнительные дозы вакцины и последние новости о лечении COVID-19 с помощью WebMD. | Подкаст / Видео |
| 01.09.2021 | Кратко о FDA: FDA проведет собрание Консультативного комитета для обсуждения заявки Pfizer-BioNTech на бустер COVID-19 Сегодня У. | Пресс-релиз / публичное заявление |
| 24.08.2021 | Коронавирус (COVID-19) Обновление Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) обновило разрешение Pfizer-BioNTech на экстренное использование (EUA), чтобы поддержать продление срока годности вакцины Pfizer-BioNTech COVID-19, хранящейся при температуре от -90 до -60 градусов Цельсия, с 6 до 9 месяцев. | Обновление COVID-19 |
23. 08.2021 08.2021 | FDA одобрило первую вакцину против COVID-19 Сегодня Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США одобрило первую вакцину против COVID-19, известную как вакцина Pfizer-BioNTech COVID-19, которая теперь продается как Comirnaty (koe-mir’-na-tee), для профилактики COVID-19. заболевание у лиц в возрасте 16 лет и старше. | Пресс-релиз / публичное заявление |
| 18.08.2021 | Совместное заявление экспертов в области общественного здравоохранения и медицинских работников HHS о бустерных прививках от COVID-19 Общественное здравоохранение и медицинские эксперты из США.Министерство здравоохранения и социальных служб С. опубликовало заявление о плане администрации по проведению повторных прививок от COVID-19 для американского народа. | Пресс-релиз / публичное заявление |
| 13.08.2021 | Коронавирус (COVID-19) Обновление В новом информационном бюллетене FDA для потребителей освещаются 5 вещей, которые нужно знать о вакцинации против COVID-19 для подростков, и эксперт FDA по вакцинам, доктор Питер Маркс, принял участие в серии видеороликов HHS «Спросите эксперта», чтобы ответить на некоторые из ваших наиболее часто задаваемых вопросов о COVID-19. | Обновление COVID-19 |
| 12.08.2021 | FDA разрешает дополнительную дозу вакцины для людей с ослабленным иммунитетом Сегодня Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США внесло поправки в разрешения на использование в чрезвычайных ситуациях (EUA) как для вакцины Pfizer-BioNTech COVID-19, так и для вакцины Moderna COVID-19, чтобы разрешить использование дополнительной дозы у определенных лиц с ослабленным иммунитетом, в частности, реципиенты трансплантатов солидных органов или те, у кого диагностированы состояния, которые считаются имеющими эквивалентный уровень иммунодефицита. | Пресс-релиз / публичное заявление |
| 06.08.2021 | Коронавирус (COVID-19) Обновление Сегодня Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) объявило, что оно признало определенные партии вакцинного препарата Astra Zeneca COVID-19, произведенного на предприятии Emergent в Балтиморе, штат Мэриленд, приемлемыми для потенциального экспорта. | Обновление COVID-19 |
| 03.08.2021 | Коронавирус (COVID-19) Обновление В середине июля FDA провело совещание с заинтересованными сторонами для обсуждения вакцин против COVID-19, включая предварительные отчеты о синдроме Гийена-Барре после вакцинации Janssen (Johnson & Johnson) против COVID-19. Исполняющая обязанности комиссара FDA Джанет Вудкок, доктор медицинских наук, и директор Центра оценки и исследований биологических препаратов FDA Питер Маркс, М.Д., к.т.н. выступили спикеры. Обращение можно найти на странице FDA на YouTube. | Обновление COVID-19 |
| 30.07.2021 | Коронавирус (COVID-19) Обновление В среду Управление по санитарному надзору за качеством пищевых продуктов и медикаментов одобрило продление срока годности охлажденной вакцины Janssen (Johnson & Johnson) против COVID-19, что позволяет хранить продукт при температуре 2–8 градусов Цельсия в течение шести месяцев. | Обновление COVID-19 |
| 16.07.2021 | Коронавирус (COVID-19) Обновление Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) официально принимает приоритетное рассмотрение заявки на получение лицензии на биопрепараты (BLA) для их мРНК-вакцины для профилактики COVID-19 у лиц в возрасте 16 лет и старше. | Обновление COVID-19 |
| 13.07.2021 | Коронавирус (COVID-19) Обновление Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) объявляет о внесении изменений в информационные бюллетени для получателей вакцин и поставщиков вакцин для вакцины против COVID-19 компании Johnson & Johnson (Janssen). | Обновление COVID-19 |
| 08.07.2021 | Совместное заявление CDC и FDA о бустерах вакцин полностью вакцинированных американцев в настоящее время не нуждаются в ревакцинации. | Пресс-релиз / публичное заявление |
| 06.07.2021 | Коронавирус (COVID-19) Обновление Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) проводит телеконференцию с заинтересованными сторонами с группами «Вакцинируйте свою семью», а также педиатрическими и медицинскими группами. | Обновление COVID-19 |
| 02.07.2021 | Коронавирус (COVID-19) Обновление Управление по санитарному надзору за качеством пищевых продуктов и медикаментов санкционировало использование в рамках разрешения на экстренное использование (EUA) вакцины Janssen против COVID-19 дополнительной партии вакцинного лекарственного вещества, произведенного на предприятии Emergent.Кроме того, FDA выпустило обновленное письмо медицинскому персоналу и учреждениям, в котором говорится, что FDA больше не разрешает использование одноразовых респираторов, не одобренных NIOSH, или дезактивированных респираторов. | Обновление COVID-19 |
| 29.06.2021 | Веб-семинар: новости о миокардитах и перикардитах Исполняющая обязанности комиссара FDA Джанет Вудкок, доктор медицинских наук, и директор Центра оценки и исследований биологических препаратов FDA Питер Маркс, М.D., Ph.D., обсуждают предполагаемый повышенный риск миокардита и перикардита после вакцинации против COVID19. | Подкаст / Видео |
| 25.06.2021 | Коронавирус (COVID-19) Обновление FDA объявило о пересмотре информационных бюллетеней пациентов и поставщиков вакцин Moderna и Pfizer-BioNTech COVID-19 в отношении предполагаемого повышенного риска миокардита (воспаление сердечной мышцы) и перикардита (воспаление ткани, окружающей сердце) после вакцинации. ; и достиг рубежа в утверждении 1000 оригинальных и дополнительных заявок на непатентованные препараты для лечения пациентов с COVID-19 с начала пандемии. | Обновление COVID-19 |
| 15.06.2021 | Коронавирус (COVID-19) Обновление FDA публикует обновленные переводы информационного бюллетеня Pfizer-BioNTech о вакцине COVID-19 для получателей и лиц, осуществляющих уход, и выпускает обновленный краткий обзор мер реагирования FDA на COVID-19. | Обновление COVID-19 |
| 11.06.2021 | FDA предпринимает шаги для повышения доступности вакцины против COVID-19 После тщательного рассмотрения и обсуждения U.S. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов предпринимает важные шаги, которые позволят обеспечить критически необходимый запас вакцины Janssen (Johnson & Johnson) против COVID-19. | Пресс-релиз / публичное заявление |
| 10.06.2021 | Консультативный комитет по вакцинам и родственным биологическим продуктам Консультативный комитет по вакцинам и родственным биологическим продуктам проведет открытое заседание, чтобы обсудить в целом данные, необходимые для поддержки авторизации и/или лицензирования вакцин против COVID-19 для использования в педиатрической популяции. | Событие |
| 25.05.2021 | Коронавирус (COVID-19) Обновление Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) обновило свое руководство «Разрешение на экстренное использование вакцин для предотвращения COVID-19», включив в него новый раздел, в котором разъясняется, как агентство намерено расставлять приоритеты при рассмотрении запросов EUA на оставшуюся часть чрезвычайной ситуации в области общественного здравоохранения, связанной с COVID-19. Кроме того, FDA выпустило отчет, в котором описаны некоторые подходы, используемые правительством Южной Кореи для борьбы с COVID-19, в частности, в отношении разработки, авторизации и использования диагностических тестов. | Обновление COVID-19 |
| 19.05.2021 | Кратко о FDA: FDA разрешает более длительное хранение в холодильнике размороженной вакцины Pfizer-BioNTech COVID-19 перед разбавлением, что делает вакцину более доступной FDA разрешило хранить неразбавленные размороженные флаконы с вакциной Pfizer-BioNTech COVID-19 в холодильнике при температуре от 2°C до 8°C (от 35°F до 46°F) на срок до 1 месяца. | Пресс-релиз / публичное заявление |
| 11.05.2021 | Коронавирус (COVID-19) Обновление FDA расширило разрешение на экстренное использование вакцины Pfizer-BioNTech против COVID-19, включив в нее детей в возрасте от 12 до 15 лет, и выпустило обновленный краткий обзор мер реагирования FDA на COVID-19. | Обновление COVID-19 |
| 11.05.2021 | Обновленная информация от федеральных официальных лиц об усилиях по борьбе с COVID-19 Слушание в Комитете Сената США по здравоохранению, образованию, труду и пенсиям; Директор Центра оценки и исследований биологических препаратов FDA, Питер Маркс, доктор медицины, доктор философии. свидетельствует в пользу FDA. Посмотреть письменные показания. | Событие |
| 10.05.2021 | FDA разрешает Pfizer-BioNTech вакцину против COVID-19 для экстренного использования у подростков Сегодня У. | Пресс-релиз / публичное заявление |
| 10.05.2021 | FDA проведет совещание Консультативного комитета по вакцинам и родственным биологическим продуктам для обсуждения использования вакцин против COVID-19 в педиатрии У.Центр оценки и исследований биологических препаратов (CBER) Управления по санитарному надзору за качеством пищевых продуктов и медикаментов (S. Food and Drug Administration) созовет виртуальное совещание Консультативного комитета по вакцинам и сопутствующим биологическим продуктам (VRBPAC) 10 июня 2021 года посредством веб-трансляции. | Пресс-релиз / публичное заявление |
| 27.04.2021 | Коронавирус (COVID-19) Обновление FDA отменило рекомендуемую паузу в использовании вакцины против COVID-19 Janssen (Johnson & Johnson) после тщательного анализа безопасности; и разослали предупреждающие письма компаниям, продающим неутвержденные продукты, с мошенническими заявлениями о COVID-19. | Обновление COVID-19 |
| 23.04.2021 | FDA и CDC рекомендуют приостановить использование вакцины против COVID-19 Johnson & Johnson (Janssen) после тщательного анализа безопасности После тщательной проверки безопасности Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США и Центры США по контролю и профилактике заболеваний определили, что рекомендуемая пауза в отношении использования вакцины Johnson & Johnson (Janssen) против COVID-19 в США. | Пресс-релиз / публичное заявление |
| 21.04.2021 | FDA продолжает важные шаги по обеспечению качества, безопасности и эффективности разрешенных вакцин против COVID-19 FDA очень серьезно относится к своей ответственности за обеспечение качества, безопасности и эффективности медицинской продукции. Американская общественность доверяет агентству в обеспечении того, чтобы все медицинские продукты, включая вакцины против COVID-19, соответствовали стандартам агентства в отношении качества, безопасности и эффективности. | Пресс-релиз / публичное заявление |
| 16.04.2021 | Коронавирус (COVID-19) Обновление Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) публикует заявление относительно вакцины Janssen против COVID-19, выпускает предупреждающее письмо и обновляет часто задаваемый вопрос о вакцине Moderna против COVID-19. | Обновление COVID-19 |
| 13.04.2021 | Совместное заявление CDC и FDA о вакцине Johnson & Johnson против COVID-19 По состоянию на 12 апреля более 6.8 миллионов доз вакцины Johnson & Johnson (Janssen) были введены в CDC США, и FDA изучает данные о шести зарегистрированных в США случаях редкого и тяжелого типа образования тромбов у людей после введения вакцины J&J. | Пресс-релиз / публичное заявление |
| 12.04.2021 | Готовность к вакцинации: устранение неравенства в отношении здоровья в связи с COVID-19 среди сообществ расовых и этнических меньшинств Поскольку FDA отмечает Месяц здоровья национальных меньшинств, мы работаем над устранением опасений по поводу вакцин среди различных сообществ, а также над защитой и укреплением здоровья различных групп населения, сосредоточив наши усилия на стратегиях, направленных на устранение различий в состоянии здоровья. | Сообщение в блоге |
| 01.04.2021 | Коронавирус (COVID-19) Обновление: FDA вносит две поправки в Разрешение на экстренное использование вакцины Moderna COVID-19, чтобы помочь увеличить количество доступных доз вакцины Сегодня Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США объявило о двух пересмотрах количества доз на флакон вакцины Moderna COVID-19. | Пресс-релиз / публичное заявление |
| 26.03.2021 | Коронавирус (COVID-19) Обновление Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) выдает компании разрешение на экстренное использование (EUA) для анализа SARS-CoV-2 NGS и предоставляет потребителям обновленную информацию по часто задаваемым вопросам о вакцинах против COVID-19. | Обновление COVID-19 |
| 24.03.2021 | Узнайте больше о вакцинах против COVID-19 от FDA Ответы FDA на распространенные вопросы о вакцинах против COVID-19. | Информация для потребителей |
| 17.03.2021 | Слушание подкомитета палаты представителей по вакцинации против COVID-19 Руководство FDA примет участие в слушаниях подкомитета Палаты представителей по надзору и расследованиям Комитета по энергетике и торговле под названием «Впереди: действия администрации Байдена по увеличению числа вакцинаций против COVID-19».” Просмотр прямой трансляции и письменных показаний | Событие |
| 05.03.2021 | Мошенничество в сфере здравоохранения и COVID-19: что вам нужно знать Управление FDA по вопросам здоровья меньшинств и справедливости в отношении здоровья обсуждает усилия агентства по предотвращению попадания на наши рынки мошеннических продуктов, особенно тех, которые утверждают, что предотвращают, лечат или излечивают COVID-19. | Подкаст / Видео |
| 02.03.2021 | Национальная неделя защиты прав потребителей: FDA проявляет бдительность в защите потребителей от мошенничества с вакцинами против COVID-19 Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) располагает всеми необходимыми средствами для выявления и пресечения мошенничества с медицинскими изделиями, пока по всей стране идет распространение вакцины. | Сообщение в блоге |
| 02.03.2021 | Коронавирус (COVID-19) Обновление Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) выпускает «Голоса» о защите потребителей от мошенничества с вакцинами против COVID-19 и выпускает предупреждающее письмо компании, продающей неутвержденные продукты с мошенническими заявлениями о COVID-19. | Пресс-релиз / публичное заявление |
| 27.02.2021 | FDA выдает разрешение на экстренное использование третьей вакцины против COVID-19 Сегодня У.S. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов выдало разрешение на экстренное использование (EUA) третьей вакцины для профилактики коронавирусной болезни 2019 года (COVID-19), вызванной коронавирусом тяжелого острого респираторного синдрома 2 (SARS-CoV-2). | Пресс-релиз / публичное заявление |
26. 02.2021 02.2021 | Заявление FDA о вакцинах и связанных с ними биологических продуктах Заседание Консультативного комитета После положительного исхода сегодняшнего заседания консультативного комитета в отношении компании Janssen Biotech Inc.Вакцины против COVID-19 FDA проинформировало спонсора о том, что оно будет быстро работать над завершением и выдачей разрешения на экстренное использование. | Пресс-релиз / публичное заявление |
| 26.02.2021 | Коронавирус (COVID-19) Обновление Сегодня FDA добавило новые устройства в список устройств, снятых с производства, включая продукты для стерилизации и консерванты кислорода. | Обновление COVID-19 |
| 26.02.2021 | Консультативный комитет по вакцинам и родственным биологическим продуктам Консультативный комитет по вакцинам и родственным биологическим продуктам проведет открытое заседание, чтобы обсудить разрешение на использование в чрезвычайных ситуациях (EUA) компании Janssen Biotech Inc. | Событие |
| 25.02.2021 | Коронавирус (COVID-19) Обновление: FDA допускает более гибкие условия хранения и транспортировки для вакцины Pfizer-BioNTech против COVID-19 Сегодня Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) объявило, что оно разрешает транспортировку и хранение неразбавленных замороженных флаконов вакцины Pfizer-BioNTech против COVID-19 при обычных температурах, обычно встречающихся в фармацевтических морозильных камерах, в течение периода до двух недель. | Пресс-релиз / публичное заявление |
| 23.02.2021 | Коронавирус (COVID-19) Обновление Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) выпустило руководство для разработчиков медицинских изделий в связи с появлением и возможным будущим появлением вариантов SARS-CoV-2. | Пресс-релиз / публичное заявление |
| 22.02.2021 | Коронавирус (COVID-19) Обновление: FDA выпускает политики, которые помогут разработчикам медицинских продуктов обращаться с вариантами вируса Сегодня Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) выпустило руководство для разработчиков медицинских продуктов, специально касающееся вакцин, диагностических и терапевтических продуктов, для решения проблемы появления и потенциального появления в будущем вариантов SARS-CoV-2, вируса, вызывающего COVID-19. | Пресс-релиз / публичное заявление |
| 12.02.2021 | Коронавирус (COVID-19) Обновление FDA выдало разрешение на экстренное использование (EUA) для лечения COVID-19 легкой и средней степени тяжести у взрослых и детей, а также пересмотрело свое руководство «Исследовательская реконвалесцентная плазма COVID-19». | Пресс-релиз / публичное заявление |
| 05.02.2021 | Коронавирус (COVID-19) Обновление FDA запланировало совещание своего Консультативного комитета по вакцинам и родственным биологическим продуктам; предупредил медицинских работников и производителей компаундов о потенциальных рисках, связанных с смешиванием лекарственных препаратов ремдесивир; пересмотрено Разрешительное письмо для реконвалесцентной плазмы COVID-19; и опубликовал заявление о том, что FDA продолжает важную работу по поддержке разработки медицинских продуктов для борьбы с новыми вариантами вируса. | Пресс-релиз / публичное заявление |
| 04.02.2021 | Коронавирус (COVID-19) Обновление: FDA объявляет о заседании Консультативного комитета для обсуждения вакцины-кандидата против COVID-19 от Janssen Biotech Inc. FDA запланировало заседание своего Консультативного комитета по вакцинам и родственным биологическим продуктам (VRBPAC) на 26 февраля 2021 г. | Пресс-релиз / публичное заявление |
| 04.02.2021 | Коронавирус (COVID-19) Обновление: FDA продолжает важную работу по поддержке разработки медицинских продуктов для борьбы с новыми вариантами вируса Как агентство общественного здравоохранения, отвечающее за регулирование медицинской продукции, мы должны обеспечить, чтобы поставщики медицинских услуг имели в своем арсенале самые современные средства диагностики, лечения и вакцины для борьбы с этой пандемией. | Пресс-релиз / публичное заявление |
| 29.01.2021 | Коронавирус (COVID-19) Обновление Управление по санитарному надзору за качеством пищевых продуктов и медикаментов поместило все дезинфицирующие средства для рук на спиртовой основе из Мексики в режим предупреждения об импорте по всей стране; совместно с Федеральной торговой комиссией направили письма-предупреждения двум компаниям, продающим неутвержденные продукты с мошенническими заявлениями о COVID-19; и обновил часто задаваемые вопросы о COVID-19 (FAQ). | Пресс-релиз / публичное заявление |
| 29.01.2021 | Вебинар по вакцине против COVID-19 Питер В.Маркс, доктор медицинских наук, доктор медицинских наук, обсуждает вакцины против COVID-19 с Американской медицинской ассоциацией в Эпизоде 5: Безопасность и доставка вакцин серии вебинаров «Что нужно знать врачам». | Подкаст / Видео |
| 14.01.2021 | Я цветная женщина-инвалид. Вот как я преодолела страх перед вакциной от COVID Сотрудник FDA обсуждает, как ее прежняя нерешительность и страх переросли в надежду и готовность получить вакцину от COVID-19. | Мнение |
| 04.01.2021 | Заявление FDA о соблюдении разрешенных графиков дозирования вакцин против COVID-19 Соблюдение разрешенных графиков дозирования вакцин против COVID-19 | Пресс-релиз / публичное заявление |
28. 12.2020 12.2020 | Коронавирус (COVID-19) Обновление FDA публикует обновленное письмо-разрешение, информационный бюллетень поставщика медицинских услуг и часто задаваемые вопросы о количестве доз Pfizer-BioNTech во флаконе, обновляет список нехватки устройств и предоставляет обновленную информацию о тестировании. | Пресс-релиз / публичное заявление |
| 28.12.2020 | Обсуждение видео: Вакцины против COVID-19 В этом 30-минутном видеообсуждении комиссар FDA д-р Стивен Хан и директор Центра оценки и исследований биологических препаратов (CBER) д-р Питер Маркс рассказывают WebMD о том, что мы знаем, чего мы не знаем и что мы можем узнать. в будущем о вакцинах против COVID-19. | Подкаст / Видео |
| 22.12.2020 | Коронавирус (COVID-19) Обновление FDA публикует переводы информационного бюллетеня Moderna COVID-19 Vaccine на несколько языков, выпускает новые ANDA и предоставляет обновленную информацию о тестировании. | Пресс-релиз / публичное заявление |
| 21.12.2020 | Коронавирус (COVID-19) Обновление FDA публикует переводы информационного бюллетеня Pfizer-BioNTech по вакцине против COVID-19 на несколько языков, выпускает новое руководство и предоставляет обновленную информацию о тестировании. | Пресс-релиз / публичное заявление |
| 18.12.2020 | Брифинг для СМИ FDA Комиссар FDA Стивен Хан и директор CBER Питер Маркс обсуждают EUA, выпущенную для вакцины Moderna COVID-19, 18 декабря 2020 г. | Событие |
| 18.12.2020 | FDA принимает дополнительные меры по борьбе с COVID-19, выдав разрешение на экстренное использование второй вакцины против COVID-19 Сегодня FDA выдало разрешение на экстренное использование (EUA) второй вакцины для профилактики коронавирусной болезни 2019 (COVID-19), вызванной коронавирусом тяжелого острого респираторного синдрома 2 (SARS-CoV-2). | Пресс-релиз / публичное заявление |
| 18.12.2020 | Расскажите мне больше о безопасности вакцин Узнайте больше о мониторинге безопасности вакцины против COVID-19 от комиссара FDA доктора Б.Стивен Хан | Подкаст / Видео |
| 17.12.2020 | Заявление FDA о вакцинах и связанных с ними биологических продуктах Заседание Консультативного комитета После положительного исхода сегодняшнего заседания консультативного комитета по вакцине Moderna COVID-19 FDA проинформировало спонсора о том, что оно будет быстро работать над завершением и выдачей разрешения на экстренное использование. | Пресс-релиз / публичное заявление |
| 17.12.2020 | Консультативный комитет по вакцинам и родственным биологическим продуктам Консультативный комитет по вакцинам и родственным биологическим продуктам проведет открытое заседание, чтобы обсудить разрешение на использование в чрезвычайных ситуациях (EUA) компании Moderna Inc. | Событие |
| 14.12.2020 | Коронавирусная вакцина Обновление FDA Питер В. Маркс, доктор медицины, доктор философии. и Стивен М. Хан, доктор медицины, возвращаются к серии вопросов и ответов JAMA, чтобы обсудить вакцины Pfizer/BioNTech и Moderna: данные, обозначение EUA на выходных (Pfizer/BioNTech), а также процесс будущего полного лицензирования и постмаркетингового надзора за безопасностью. | Подкаст / Видео |
| 12.12.2020 | Виртуальная пресс-конференция: Первая вакцина против COVID-19 В рамках приверженности FDA прозрачности мы приглашаем вас посмотреть нашу виртуальную пресс-конференцию, которая будет транслироваться в прямом эфире через учетные записи FDA на YouTube, Facebook и Twitter 12 декабря 2020 г. в 9:00 по восточноевропейскому времени. | Событие |
| 11.12.2020 | Управление по санитарному надзору за качеством пищевых продуктов и медикаментов принимает ключевые меры в борьбе с COVID-19, выдав разрешение на экстренное использование первой вакцины против COVID-19 Сегодня FDA выдало первое разрешение на экстренное использование (EUA) вакцины для профилактики коронавирусной болезни 2019 (COVID-19), вызванной коронавирусом тяжелого острого респираторного синдрома 2 (SARS-CoV-2), у лиц в возрасте 16 лет. и старше. | Пресс-релиз / публичное заявление |
| 11.12.2020 | Заявление FDA о вакцинах и связанных с ними биологических продуктах Заседание Консультативного комитета Заявление комиссара FDA Стивена М. Хана, доктора медицины, и директора Центра оценки и исследований биологических препаратов Питера Маркса, доктора медицины, доктора философии. | Пресс-релиз / публичное заявление |
10. 12.2020 12.2020 | Новости о коронавирусе (COVID-19): FDA проводит совещание Консультативного комитета для обсуждения авторизации вакцины-кандидата против COVID-19 в рамках проверки Агентством данных о безопасности и эффективности Заявление комиссара FDA Стивена М.Хан, доктор медицины, | Пресс-релиз / публичное заявление |
| 10.12.2020 | Консультативный комитет по вакцинам и родственным биологическим продуктам Консультативный комитет по вакцинам и сопутствующим биологическим продуктам Центра оценки и исследований биологических препаратов FDA (VRBPAC) проведет открытое заседание, чтобы обсудить разрешение на экстренное использование (EUA) вакцины Pfizer-BioNTech COVID-19 для профилактики COVID-19 у людей. 16 лет и старше.Посмотреть прямую трансляцию | Событие |
| 04.12.2020 | Замечания доктора Хана в ратуше Национальной медицинской академии о вакцине против COVID-19 | Событие |
30. 11.2020 11.2020 | Коронавирус (COVID-19) Обновление: FDA объявляет о заседании Консультативного комитета для обсуждения второго кандидата на вакцину против COVID-19 FDA запланировало совещание своего Консультативного комитета по вакцинам и родственным биологическим продуктам (VRBPAC) на декабрь.17, чтобы обсудить запрос на разрешение на экстренное использование (EUA) вакцины против COVID-19 от Moderna Inc. | Пресс-релиз / публичное заявление |
| 20.11.2020 | Коронавирус (COVID-19) Обновление: FDA объявляет о заседании Консультативного комитета для обсуждения вакцины-кандидата против COVID-19 FDA запланировало заседание своего Консультативного комитета по вакцинам и родственным биологическим продуктам (VRBPAC) на 10 декабря, чтобы обсудить запрос на разрешение на экстренное использование (EUA) вакцины против COVID-19 от Pfizer, Inc.в партнерстве с BioNTech Manufacturing GmbH. | Пресс-релиз / публичное заявление |
20. 11.2020 11.2020 | Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) опубликовало новую информацию о процессе разработки и проверки вакцины: | Информация для потребителей |
| 19.11.2020 | Управление по санитарному надзору за качеством пищевых продуктов и медикаментов и организация вакцинации вашей семьи Обсудите COVID с лидерами сообщества меньшинств руководителя FDA участвуют в виртуальной встрече с членами сообщества расовых и этнических меньшинств, посвященной работе FDA над вакциной против COVID-19. | Событие |
| 17.11.2020 | Обновление COVID-19: постоянное стремление FDA к прозрачности для EUA COVID-19 Заявление, подтверждающее приверженность FDA прозрачности в отношении процесса EUA и обновления плана FDA по предоставлению дополнительной информации о решениях о выдаче, пересмотре или отзыве EUA для лекарств и биологических продуктов, включая вакцины. | Пресс-релиз / публичное заявление |
| 09.11.2020 | Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) предлагает рекомендации по расширению разнообразия клинических испытаний и поощрению инклюзивности при разработке медицинских продуктов Заявление комиссара FDA доктораСтивен Хан об опубликованном сегодня окончательном руководстве, в котором представлены текущие взгляды агентства на шаги по расширению разнообразия в клинических испытаниях любого медицинского продукта, такого как методы лечения или вакцины от COVID-19, а также медицинских продуктов в более широком смысле. | Пресс-релиз / публичное заявление |
| 01.11.2020 | Уроки, извлеченные из COVID Выступление д-ра Стивена Хана на Глобальном форуме лидеров фармацевтического производства | Событие |
| 27.10.2020 | Я представитель FDA по вакцинам против COVID-19. Директор Центра оценки и исследований биологических препаратов FDA д-р Питер Маркс | Мнение |
| 27.10.2020 | Комиссар FDA Стивен Хан в эфире: COVID-19 и FDA Комиссар FDA Стивен Хан присоединяется к утреннему радиошоу, чтобы обсудить роль FDA в борьбе с COVID-19. | Подкаст |
| 22.10.2020 | Консультативный комитет по вакцинам и родственным биологическим продуктам Комитет проведет открытое заседание, чтобы обсудить в целом вопросы разработки, выдачи разрешений и/или лицензирования вакцин для профилактики COVID-19.На этой встрече не будет обсуждаться конкретное применение. Посмотреть веб-трансляцию | Событие |
| 22.10.2020 | Комиссар FDA беседует с AARP о вакцинах против COVID-19 Доктор Стивен Хан объясняет роль FDA в обеспечении безопасности и эффективности вакцин против COVID-19. | Информация для потребителей |
| 20.10.2020 | Консультативный комитет FDA по вакцинам и родственным биологическим продуктам и его роль в консультировании Агентства по вакцинам против COVID-19 На этой неделе Консультативный комитет FDA по вакцинам и связанным с ними биологическим продуктам собирается, чтобы обсудить в целом разработку, разрешение и/или лицензирование вакцин для предотвращения COVID-19. | Сообщение в блоге |
| 20.10.2020 | Консультативный комитет по вакцинам против COVID-19 Д-р Питер Маркс представляет обновленную информацию о вакцинах против COVID-19 и обсуждает предстоящее заседание Консультативного комитета по вакцинам и сопутствующим биологическим продуктам. | Подкаст / Видео |
| 16.10.2020 | Разрешение на экстренное использование вакцин против Covid — соображения безопасности и эффективности | Мнение |
08. 10.2020 10.2020 | Процесс рассмотрения вакцин для профилактики COVID-19: обсуждение Комиссар FDA Dr.Стивен Хан обсудил процесс проверки вакцины против COVID-19 с Центром исследований и политики в области инфекционных заболеваний и другими организациями. | Подкаст / Видео |
| 08.10.2020 | Интервью: Комиссар FDA по вакцинам против COVID-19 и другим медицинским контрмерам Комиссар FDA доктор Стивен Хан рассказал о процессе разработки вакцины против COVID-19 и других медицинских мерах противодействия COVID-19. | Подкаст / Видео |
| 07.10.2020 | Обновление вакцины против коронавируса Беседа с директором Центра оценки и исследований биологических препаратов Питером Марксом, М.Д., к.т.н. | Подкаст / Видео |
| 06.10.2020 | Кратко о FDA: FDA выпускает руководство по разрешению на экстренное использование вакцин против COVID-19 Рекомендации для спонсоров вакцин в отношении научных данных и информации, которые могут помочь в выдаче разрешения на экстренное использование (EUA) для экспериментальной вакцины, предназначенной для предотвращения COVID-19. | Пресс-релиз / публичное заявление |
| 06.10.2020 | Расскажите мне больше о вакцинах Узнайте больше о том, как разрабатываются вакцины от U.S. Руководители Департамента здравоохранения и социальных служб. | Подкаст / Видео |
| 30.09.2020 | Замечания д-ра Хана в адрес Глобальной коалиции научных исследований в области регулирования | Событие |
| 29.09.2020 | Замечания доктора Хана Национальной лиге потребителей о процессе проверки вакцин Взгляд потребителей на пандемию Covid-19: разговор с FDA | Событие |
| 29.09.2020 | Замечания уполномоченного Хана друзьям по исследованию рака | Событие |
| 23.09.2020 | COVID-19: обновленная информация о федеральных ответных мерах — вступительное слово FDA Слушание в Сенатском комитете по здравоохранению, образованию, труду и пенсиям; Комиссар FDA Стивен М. | Событие |
| 21.09.2020 | Остерегайтесь поддельных тестов на коронавирус, вакцин и методов лечения Узнайте больше о том, как выявлять мошеннические заявления и ложную информацию о продуктах, которые якобы диагностируют, лечат или предотвращают коронавирус. | Информация для потребителей |
| 11.09.2020 | Научный и нормативный надзор FDA за вакцинами жизненно важен для общественного здравоохранения FDA обязуется принимать решения относительно авторизации или одобрения вакцин против COVID-19, руководствуясь научными данными и данными. | Сообщение в блоге |
| 28.08.2020 | Коронавирус (COVID-19) Обновление: FDA объявляет о заседании Консультативного комитета для обсуждения вакцин против COVID-19 FDA объявило, что открытое заседание Консультативного комитета по вакцинам и родственным биологическим продуктам состоится 22 октября 2020 г. | Пресс-релиз / публичное заявление |
| 20.08.2020 | Лидерство FDA в ускорении выздоровления от COVID-19 Замечания заместителя комиссара по медицинским и научным вопросам Ананда Шаха, М.D. в Альянс за политику здравоохранения | Событие |
| 18.08.2020 | Обеспечение безопасности и эффективности вакцины против COVID-19 | Сообщение в блоге |
| 18.08.2020 | Мошенничество в сфере здравоохранения и COVID-19 Доктор Джуди МакМикин, помощник комиссара по вопросам регулирования, присоединяется к доктору Шаху в шоу, чтобы обсудить борьбу FDA с мошенничеством в сфере здравоохранения во время пандемии COVID-19. | Подкаст / Видео |
| 10.08.2020 | Критическая роль медицинских работников во время COVID-19 Замечания комиссара FDA Стивена М. | Событие |
| 07.08.2020 | Неизменные нормативные гарантии для вакцин против COVID-19 | Мнение |
| 05.08.2020 | Комиссар FDA: несмотря ни на что, только безопасная и эффективная вакцина получит наше одобрение | Мнение |
| 30.07.2020 | COVID-19 и FDA Доктор Хан обсуждает роль агентства в реагировании на пандемию COVID-19. | Подкаст / Видео |
| 28.07.2020 | Информация FDA: вакцины от COVID-19, часть 2 Доктор Питер Маркс возвращается для более подробного обсуждения вакцин в связи с COVID-19. Узнайте больше о «коллективном иммунитете», операции Warp Speed и распространении вакцины в этом выпуске. | Подкаст / Видео |
21. 07.2020 07.2020 | Информация FDA: вакцины от COVID-19, часть 1 В Части 1 серии вакцин FDA Insight, Dr.Шах приветствует доктора Питера Маркса, директора Центра оценки и исследований биологических препаратов FDA, для обсуждения основ разработки вакцины против COVID-19. | Подкаст / Видео |
| 30.06.2020 | COVID-19: обновленная информация о прогрессе в обеспечении безопасного возвращения на работу и в школу Слушание в Сенатском комитете по здравоохранению, образованию, труду и пенсиям; Комиссар FDA Стивен М. Хан, доктор медицины, свидетельствовал от имени FDA. | Событие |
| 30.06.2020 | Новости о коронавирусе (COVID-19): FDA принимает меры, чтобы способствовать своевременной разработке безопасных и эффективных вакцин против COVID-19 FDA опубликовало руководящий документ для содействия своевременной разработке безопасных и эффективных вакцин для предотвращения COVID-19, содержащий рекомендации для тех, кто разрабатывает вакцины против COVID-19 для конечной цели лицензирования. | Пресс-релиз / публичное заявление |
| 25.06.2020 | Партнерство с Европейским союзом и глобальными регулирующими органами по борьбе с COVID-19 FDA и Европейский союз, включая Европейскую комиссию и ее Европейское агентство по лекарственным средствам, сотрудничают по многим научным и нормативным направлениям в рамках нашего ответа на COVID-19. | Сообщение в блоге |
| 23.06.2020 | Слушание в комитете Палаты представителей по энергетике и торговле: надзор за реакцией администрации Трампа на пандемию COVID-19 Комиссар FDA Стивен М.Хан, доктор медицины, будет давать показания в FDA. | Событие |
| 01.06.2020 | Замечания комиссара Стивена Хана, доктора медицины — Пандемия COVID-19 — Поиск решений, применение извлеченных уроков Комиссар Хан беседует с Альянсом за усиление FDA | Событие |
12. 05.2020 05.2020 | Слух – COVID-19: безопасное возвращение на работу и в школу Комиссар FDA Стивен М.Хан дал показания перед Комитетом Сената США по здравоохранению, образованию, труду и пенсиям . | Событие |
| 17.04.2020 | NIH запустит государственно-частное партнерство для ускорения вакцинации и лечения COVID-19 FDA примет участие в партнерстве ACTIV, направленном на разработку системы сотрудничества между всеми партнерами для быстрого реагирования на COVID-19 и будущие пандемии. | Пресс-релиз / публичное заявление |
| 10.04.2020 | Взгляд на реакцию FDA на COVID-19 Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) играет важную роль в борьбе с коронавирусом, используя науку и инновационные подходы для принятия широкого спектра мер, способствующих реагированию нашей страны. | Сообщение в блоге |
| 23.03.2020 | FDA и EMA сотрудничают для содействия разработке вакцины против SARS-CoV-2 FDA и Европейское агентство по лекарственным средствам совместно возглавили первую глобальную встречу регулирующих органов, чтобы обсудить пути оптимизации разработки вакцин против SARS-CoV-2. | Сообщение в блоге |
| 03.03.2020 | должностных лица HHS дали показания на слушаниях в Сенате HELP «Новая угроза заболевания: как США.С. Реагирует на COVID-19, новый коронавирус.
 | Событие |
| 14.02.2020 | Действия FDA в ответ на новый коронавирус 2019 г. в стране и за рубежом FDA является активным партнером в борьбе с новым коронавирусом (COVID-19), тесно сотрудничая с нашим правительством и партнерами в области общественного здравоохранения по всей территории США.S. Департамент здравоохранения и социальных служб, а также с нашими международными партнерами. Наша работа многогранна и направлена на активное содействие усилиям по диагностике, лечению и профилактике заболеваний; надзор за цепочкой поставок медицинской продукции на предмет потенциальной нехватки или сбоев и, при необходимости, помощь в смягчении таких воздействий; и использование всего спектра наших инструментов общественного здравоохранения, поскольку мы контролируем безопасность и качество продуктов, регулируемых FDA, для американских пациентов и потребителей. | Пресс-релиз / публичное заявление |
Положение об охране труда в организации: образец
Одной из основных обязанностей работодателя является обеспечение надлежащих условий для работников. Речь идет, прежде всего, о безопасности в процессе трудовой деятельности. Для его обеспечения компания разрабатывает комплекс специальных мероприятий. Они отражены в Положении об организации системы управления охраной труда. Рассмотрим его содержание.
Речь идет, прежде всего, о безопасности в процессе трудовой деятельности. Для его обеспечения компания разрабатывает комплекс специальных мероприятий. Они отражены в Положении об организации системы управления охраной труда. Рассмотрим его содержание.
Общие сведения
Среди всех локальных документов в РФ Положение об охране труда в организации (образец документа представлен в статье) считается одним из основных. Он устанавливает профилактические, социально-экономические, организационные, технические и другие мероприятия, направленные на охрану жизни и здоровья работников.
Имеется типовой Положение об охране труда. Однако в организации этот документ корректируется с учетом специфики деятельности. Он включает не только перечень мероприятий, обеспечивающих безопасность персонала, но и сведения о лицах, ответственных за выполнение требований нормативных актов, принятых в области охраны труда, должностных обязанностях работников, ответственности за нарушения.
Типовой образец Положения об охране труда в организации утверждается Минтруда.Именно это агентство осуществляет контроль за выполнением правил. В случае выявления нарушений к руководителю и иным виновным лицам применяются меры ответственности.
Стоит отметить, что многие предприятия дополнительно разрабатывают Положение об организации обучения по охране труда. Между тем, этот локальный документ может быть включен в Общее положение об ОТ. Персонал проходит инструктаж, после чего проверяется знание техники безопасности при выполнении той или иной работы.
Назначение документа
Положение об организации охраны труда в учреждениях, предприятиях и организациях:
- Уточняет, распределяет права и обязанности ответственных лиц и других штатных работников.
- Уточняет планы мероприятий, проводимых в области ОС.
- Устанавливает порядок осуществления контрольных мероприятий в отношении отдела охраны труда и надзора за соблюдением правил техники безопасности.

- Устанавливает правила проведения обучения по ОТ для специалистов и руководителей. В Положении по охране труда в организации, в частности, закреплено количество часов для каждого работника, а также методы обучения и проверки знаний.
- Определяет правила формирования комиссии по оценке условий труда предприятия.
- Устанавливает порядок финансирования мероприятий по охране труда. В Положении об охране труда в организации должны быть отражены статьи расходов, а также источники поступления денежных средств.
Особенности составления
При составлении документации по охране труда следует использовать типовой образец Положения по охране труда в организации, утвержденного приказом Минтруда № 438н от 2016 г., ГОСТ 12.0.230 -2007.
Руководитель компании также может заказать документ у специализированной компании или у частного специалиста. В этом случае придется заплатить достаточно крупную сумму.
Другой вариант – составить свой образец Положения об организации работы по охране труда. Для этого вам придется провести некоторые подготовительные мероприятия. В первую очередь необходимо ознакомиться с нормативными требованиями в области охраны окружающей среды, оценить условия труда на предприятии. Если предприятие большое, целесообразно всю эту деятельность доверить группе сотрудников.
Для этого вам придется провести некоторые подготовительные мероприятия. В первую очередь необходимо ознакомиться с нормативными требованиями в области охраны окружающей среды, оценить условия труда на предприятии. Если предприятие большое, целесообразно всю эту деятельность доверить группе сотрудников.
Структура документа
Положение о системе охраны труда в организации включает несколько разделов:
- Общие положения В этом разделе раскрывается цель деятельности по охране труда, дается краткое содержание, указывается область применения документа.
- Политика компании в области ОТ. В данном разделе Положения по охране труда в организации приведены принципы, на которых основывается деятельность, связанная с обеспечением безопасности.
- Обеспечение функционирования системы менеджмента и охраны труда. Вот обязанности сотрудников, отвечающих за безопасность на предприятии.
- События ОТ. В данном разделе перечислены конкретные мероприятия, направленные на обеспечение безопасных условий труда, порядок обучения правилам техники безопасности, перечень вредных факторов и профессий, представляющих потенциальную опасность.

- Планирование мероприятий. В данном разделе устанавливается порядок составления, корректировки и доработки Положения об охране труда в организации.
- Меры контроля. Описаны вопросы, связанные с контролем за обстановкой на предприятии, контролем за соблюдением правил по охране труда.
- Планирование улучшений. Настоящий раздел предназначен для определения порядка разработки плана совершенствования системы охраны труда на предприятии, круга лиц, уполномоченных вносить предложения.
- Действия при наступлении обстоятельств непреодолимой силы.
- Управление документацией на СОУТ. В этом разделе должны быть закреплены правила составления документов по охране окружающей среды, порядок ознакомления с ними персонала, хранения и использования их в деятельности предприятия.
В Положение о ТО можно включить раздел, в котором подробно описан процесс изучения правил безопасности при выполнении работ. Он устанавливает круг лиц, обязанных проходить обучение, периодичность и обучение.
Финансирование
Положение может содержать раздел, в котором будут описаны меры, средства индивидуальной защиты, оборудование и лекарства, требующие определенных затрат.
Следует отметить, что затраты на ТО не облагаются налогом. Но в этой сфере есть ряд нюансов. В первую очередь они касаются типового перечня мероприятий по улучшению условий труда на предприятии. Минздравсоцразвития поддерживает идею включения в Положение мер, не вошедших в этот перечень.Но сейчас налоговая инспекция руководствуется приказами и разъяснениями Минфина. В связи с этим при формировании перечня мероприятий следует руководствоваться типовым перечнем.
Ответственность
В Положении должны быть установлены меры воздействия на работников, нарушающих правила охраны труда. В этом случае следует обратиться к конкретному законодательству.
В этом же разделе можно закрепить порядок расследования несчастных случаев на производстве.
Заявки
Целесообразно включать в документацию конкретные планы, графики, инструкции, описания. Например, в виде приложения состав аптечки, порядок оказания первой помощи, действия персонала при возникновении ЧС, планы эвакуации и т.д. должен быть подписан работником, ответственным за обеспечение охраны труда на предприятии, и утвержден руководителем.
Например, в виде приложения состав аптечки, порядок оказания первой помощи, действия персонала при возникновении ЧС, планы эвакуации и т.д. должен быть подписан работником, ответственным за обеспечение охраны труда на предприятии, и утвержден руководителем.
С документом необходимо ознакомиться всему персоналу организации.
Правила ОТ в строительной организации
При составлении документации по охране труда необходимо руководствоваться не государственными стандартами, а СНиПами.
Положение должно содержать часть, в которой раскрываются все используемые в тексте термины и определения. Как и в типовом образце, в документации на строительную организацию ОТ указывают цели деятельности, требования к квалификации работников.
Правила ОТ в школе
В документ могут быть включены следующие разделы:
- Политика вуза.
- Организация системы управления.
- Функции преподавателей и директоров.
- Формирование специальной службы безопасности.

- Перечень обязанностей отдельных работников.
- Перечень локальных актов в области ОТ.
- Процедура расследования несчастного случая.
При оформлении документа необходимо учитывать высокий риск получения травм у детей.Поэтому вопросам безопасности в образовательном учреждении следует уделять повышенное внимание. За нарушения правил необходимо установить строгие санкции в рамках закона.
Немаловажное значение в работе по обеспечению безопасных условий проживания граждан в учреждениях образования имеют профилактические мероприятия. И с детьми, и с педагогами, и с родителями надо проводить профилактическую работу.
Особенности обучения и проверки знаний по охране здоровья
Как правило, ответственность за организацию инструктажа возлагается на руководителя предприятия.Инструктаж по охране труда может быть первичным, повторным, целевым, внеплановым и др.
Обязательна на всех предприятиях, проводимых вводный инструктаж. В ходе нее сотруднику разъясняются основные положения локальных документов в области охраны труда и техники безопасности, действующих в организации. Многие работодатели игнорируют необходимость вводного обучения, что зачастую приводит к крайне негативным последствиям.
В ходе нее сотруднику разъясняются основные положения локальных документов в области охраны труда и техники безопасности, действующих в организации. Многие работодатели игнорируют необходимость вводного обучения, что зачастую приводит к крайне негативным последствиям.
Приказом руководителя должен быть определен работник, ответственный за проведение инструктажей и проверку знаний правил безопасности с другими работниками.
В некоторых случаях возникает необходимость проведения целевого обучения. Такой инструктаж направлен на разъяснение правил выполнения конкретных работ, не входящих в перечень должностных обязанностей. Работники могут быть вовлечены в такую деятельность только с их согласия. Сотрудник может отказаться от выполнения непроизводственных задач. В этом случае он может не проходить целевую подготовку. Однако это правило не применяется в случае чрезвычайной ситуации, стихийного бедствия или иного чрезвычайного положения.
По окончании обучения проводится проверка знаний.


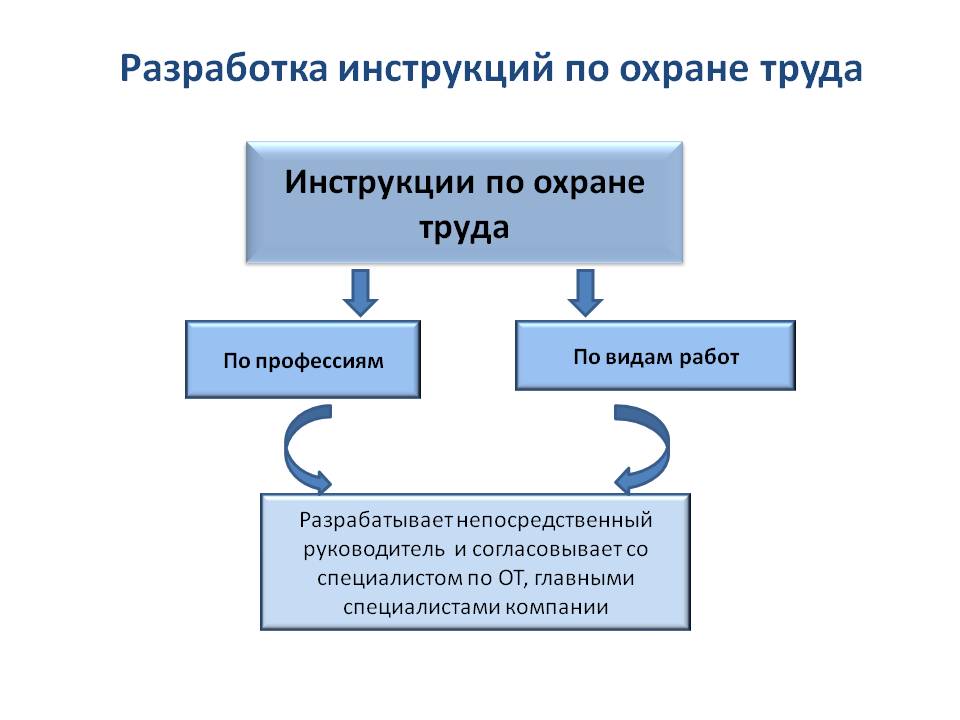
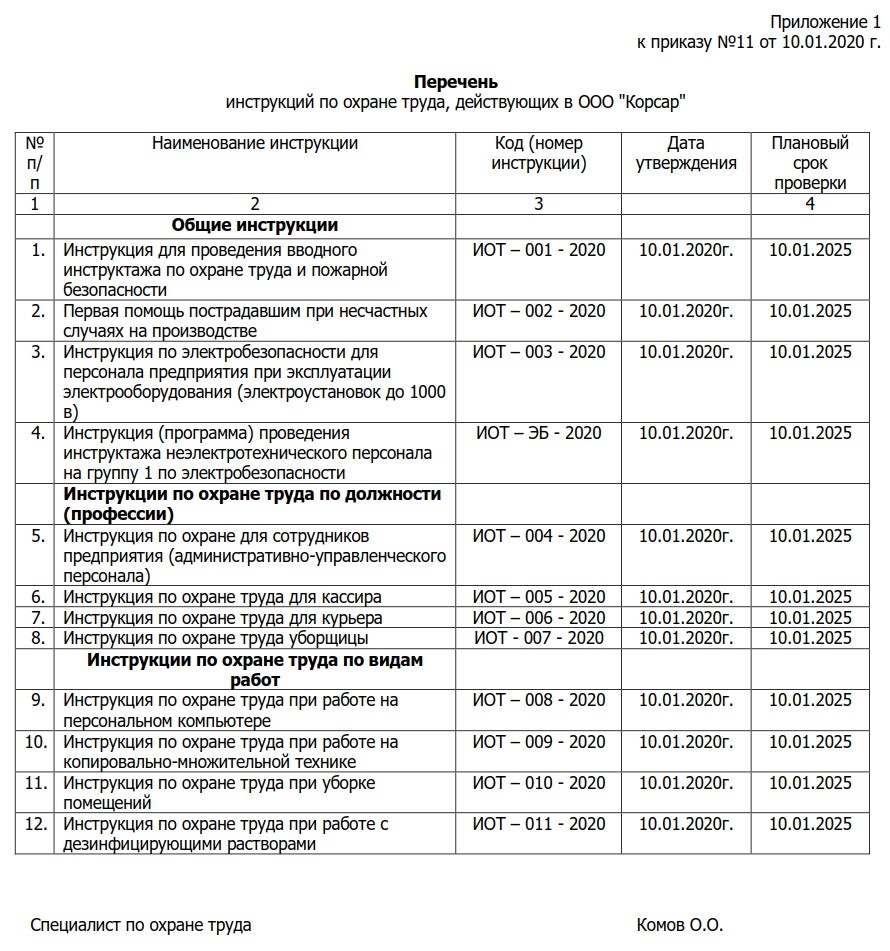 Все стороны, участвующие в приобретении или передаче, должны заполнить форму отдельно.
Все стороны, участвующие в приобретении или передаче, должны заполнить форму отдельно. Индийские племена или племенные единицы могут выбрать самофинансирование.
Индийские племена или племенные единицы могут выбрать самофинансирование.
 Некоторые примеры включают, помимо прочего, Кооперативную службу распространения знаний, некоммерческие организации и учреждения, Межплеменной сельскохозяйственный совет и другие подобные организации; и
Некоторые примеры включают, помимо прочего, Кооперативную службу распространения знаний, некоммерческие организации и учреждения, Межплеменной сельскохозяйственный совет и другие подобные организации; и Такие расходы, как еда, одежда, ипотека или аренда, страховка, налоги, медицинские расходы, платежи по кредитным картам, расходы на образование и другие потребительские долги, являются частью расчетов плана фермы.Знайте свои расходы. Возьмите с собой свои записи.
Такие расходы, как еда, одежда, ипотека или аренда, страховка, налоги, медицинские расходы, платежи по кредитным картам, расходы на образование и другие потребительские долги, являются частью расчетов плана фермы.Знайте свои расходы. Возьмите с собой свои записи. FCRA способствует точности и конфиденциальности информации в файлах национальных кредитных компаний. Федеральная торговая комиссия (FTC), национальное агентство по защите прав потребителей, обеспечивает соблюдение FCRA в отношении компаний, предоставляющих кредитную отчетность.
FCRA способствует точности и конфиденциальности информации в файлах национальных кредитных компаний. Федеральная торговая комиссия (FTC), национальное агентство по защите прав потребителей, обеспечивает соблюдение FCRA в отношении компаний, предоставляющих кредитную отчетность.


 Комитет соберется на открытом заседании, чтобы обсудить запрос на внесение поправок в разрешение на использование в чрезвычайных ситуациях Pfizer-BioNTech. (EUA) для введения своей мРНК-вакцины COVID-19 детям в возрасте от 5 до 11 лет.
Комитет соберется на открытом заседании, чтобы обсудить запрос на внесение поправок в разрешение на использование в чрезвычайных ситуациях Pfizer-BioNTech. (EUA) для введения своей мРНК-вакцины COVID-19 детям в возрасте от 5 до 11 лет. COVID-19 и вакцины Janssen Biotech Inc. COVID-19 для введения дополнительной дозы или «бустерной» дозы после завершения первичной серии, лицам от 18 лет и старше.Смотрите прямую трансляцию от 14 октября. Смотрите прямую трансляцию от 15 октября.
COVID-19 и вакцины Janssen Biotech Inc. COVID-19 для введения дополнительной дозы или «бустерной» дозы после завершения первичной серии, лицам от 18 лет и старше.Смотрите прямую трансляцию от 14 октября. Смотрите прямую трансляцию от 15 октября.
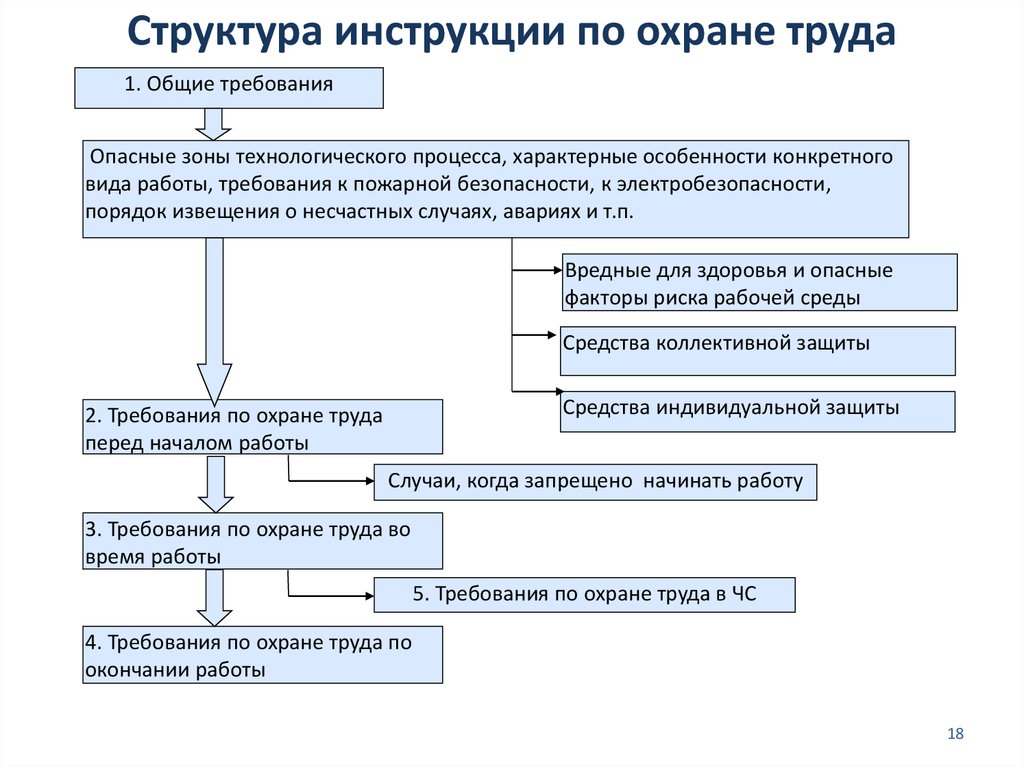 персонал на время чрезвычайной ситуации в области общественного здравоохранения, связанной с COVID-19; и санкционировал использование в рамках EUA для вакцины Janssen COVID-19 двух дополнительных партий вакцинного лекарственного вещества, произведенного на предприятии Emergent.
персонал на время чрезвычайной ситуации в области общественного здравоохранения, связанной с COVID-19; и санкционировал использование в рамках EUA для вакцины Janssen COVID-19 двух дополнительных партий вакцинного лекарственного вещества, произведенного на предприятии Emergent. FDA также опубликовало заявление под названием «FDA будет следить за научными данными о вакцинах против COVID-19 для детей младшего возраста».
FDA также опубликовало заявление под названием «FDA будет следить за научными данными о вакцинах против COVID-19 для детей младшего возраста». S. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов объявило о проведении виртуального собрания своего Консультативного комитета по вакцинам и сопутствующим биологическим продуктам для обсуждения вопроса о дополнительных дозах вакцин против COVID-19 и, в частности, для обсуждения заявки на получение дополнительной лицензии на биологические препараты Pfizer-BioNTech для введения третьей (« бустерная») доза Комирнати (вакцина против COVID-19, мРНК) у лиц в возрасте 16 лет и старше.
S. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов объявило о проведении виртуального собрания своего Консультативного комитета по вакцинам и сопутствующим биологическим продуктам для обсуждения вопроса о дополнительных дозах вакцин против COVID-19 и, в частности, для обсуждения заявки на получение дополнительной лицензии на биологические препараты Pfizer-BioNTech для введения третьей (« бустерная») доза Комирнати (вакцина против COVID-19, мРНК) у лиц в возрасте 16 лет и старше. вакцинация.
вакцинация. Вакцина AstraZeneca не разрешена для использования в США, но FDA понимает, что эти партии AstraZeneca или вакцина, изготовленная из этих партий, теперь будут экспортироваться для использования.
Вакцина AstraZeneca не разрешена для использования в США, но FDA понимает, что эти партии AstraZeneca или вакцина, изготовленная из этих партий, теперь будут экспортироваться для использования.
 FDA, CDC и NIH участвуют в строгом научно обоснованном процессе, чтобы рассмотреть вопрос о том, может ли быть необходим бустер.
FDA, CDC и NIH участвуют в строгом научно обоснованном процессе, чтобы рассмотреть вопрос о том, может ли быть необходим бустер.

 Посмотреть прямую трансляцию
Посмотреть прямую трансляцию
 S. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов расширило разрешение на экстренное использование (EUA) вакцины Pfizer-BioNTech COVID-19 для профилактики коронавирусной болезни 2019 года (COVID-19), вызванной коронавирусом тяжелого острого респираторного синдрома 2 (SARS-CoV-2). включая подростков от 12 до 15 лет. Посмотреть пресс-брифинг.
S. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов расширило разрешение на экстренное использование (EUA) вакцины Pfizer-BioNTech COVID-19 для профилактики коронавирусной болезни 2019 года (COVID-19), вызванной коронавирусом тяжелого острого респираторного синдрома 2 (SARS-CoV-2). включая подростков от 12 до 15 лет. Посмотреть пресс-брифинг. Во время встречи агентство представит обновленную информацию о нашем подходе к разрешению на экстренное использование (EUA) вакцин против COVID-19, предназначенных для использования у лиц в возрасте от 12 до 17 лет.
Во время встречи агентство представит обновленную информацию о нашем подходе к разрешению на экстренное использование (EUA) вакцин против COVID-19, предназначенных для использования у лиц в возрасте от 12 до 17 лет. С. следует поднять.
С. следует поднять.



 Вакцина против COVID-19 для активной иммунизации для предотвращения COVID-19, вызванного SARS-CoV-2, у лиц в возрасте 18 лет и старше. Посмотреть прямую трансляцию
Вакцина против COVID-19 для активной иммунизации для предотвращения COVID-19, вызванного SARS-CoV-2, у лиц в возрасте 18 лет и старше. Посмотреть прямую трансляцию

 для обсуждения запроса на разрешение на экстренное использование (EUA) вакцины против COVID-19 от Janssen Biotech Inc.
для обсуждения запроса на разрешение на экстренное использование (EUA) вакцины против COVID-19 от Janssen Biotech Inc.

 COVID-19 Вакцина для профилактики COVID-19 у лиц в возрасте 18 лет и старше. Посмотреть запись прямой трансляции
COVID-19 Вакцина для профилактики COVID-19 у лиц в возрасте 18 лет и старше. Посмотреть запись прямой трансляции

 Мы позаботимся о том, чтобы они были безопасными и эффективными.
Мы позаботимся о том, чтобы они были безопасными и эффективными. 

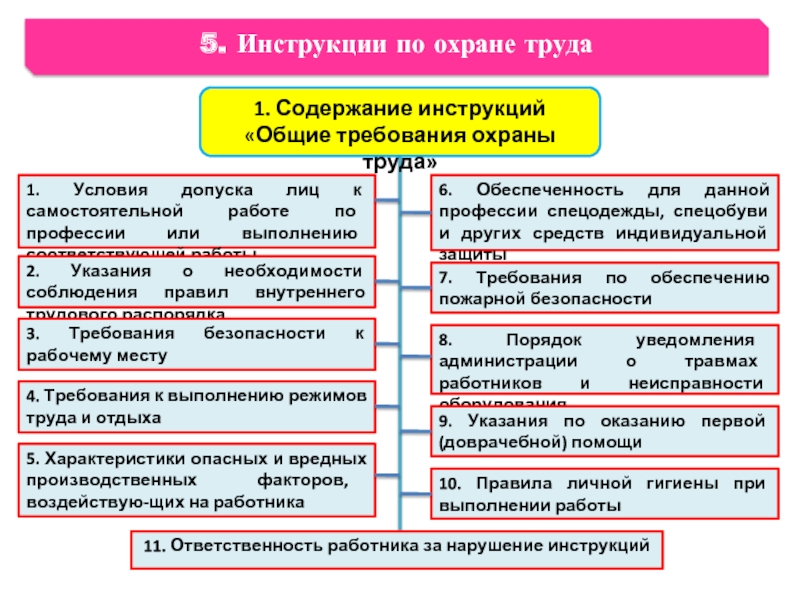
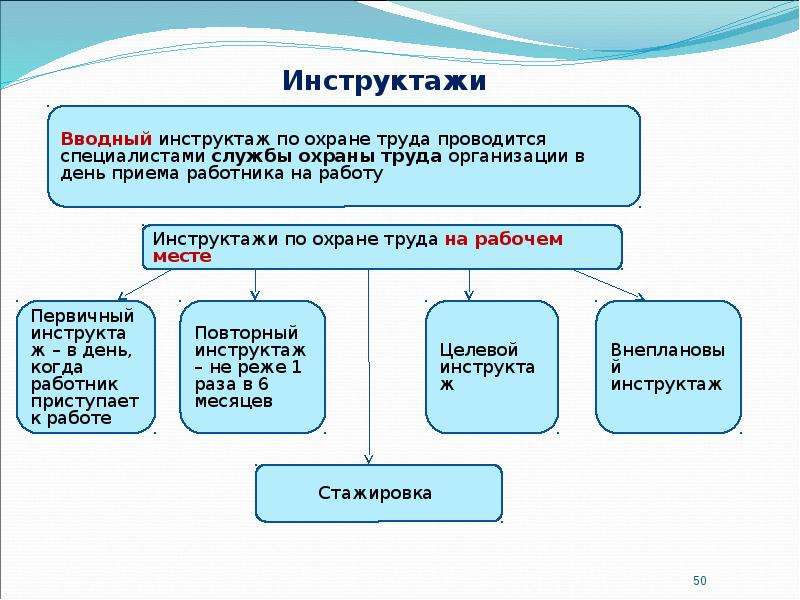 Хана, доктора медицины, подготовленные для видеобеседы с медицинскими работниками.
Хана, доктора медицины, подготовленные для видеобеседы с медицинскими работниками.