Рсв 2019 инструкция по заполнению: Расчет по страховым взносам (РСВ) — Контур.Экстерн — СКБ Контур
инструкция, сроки сдачи, образец заполнения и бланки| Контур.НДС+
С IV квартала 2020 года все компании должны использовать новую форму Расчёт по страховым взносам (РСВ). Форма по КНД 1151111 — расчёт по страховым взносам. Когда нужно сдать расчёт, образец заполнения и наша подробная инструкция помогут корректно заполнить форму с учётом новых изменений.
Периодичность представления — ежеквартально. Отчитываться по форме РСВ должны все компании и ИП, если они являются страхователями в части пенсионного, медицинского и социального страхования наёмного персонала. Бланк РСВ за 2020 год утверждён приказом ФНС от 18 сентября 2019 года № ММВ-7-11/470 в редакции приказа ФНС от 15 октября 2020 года № ЕД-7-11/751.
Срок сдачи отчёта по форме РСВ
Ежеквартальный расчёт по страховым взносам предоставляется в налоговые органы не позднее 30 числа месяца, который следует за отчётным периодом. Если установленный день сдачи отчёта выпадает на выходной, то в соответствии с законодательством он переносится на первый рабочий день (п.
На 2021 год установлены следующие сроки предоставления ежеквартальных расчётов:
- за 2020 год до 30 января (1 февраля) 2021 года
- за I квартал до 30 апреля 2021 года
- за полугодие до 30 июля 2021 года
- за 9 месяцев до 30 октября (1 ноября) 2021 года
Предприниматели, ведущие крестьянско-фермерское хозяйство, ежеквартальную отчётность не представляют, срок сдачи годового отчёта установлен как и для прочих организаций не позднее 30 января, следующего года. Но поскольку 30 число выпадает на субботу, то крайний срок переносится на ближайший рабочий день 1 февраля 2021 года.
Способ сдачи отчёта — на бумаге или через интернет
С 2020 года правила, по которым определялась возможность сдачи декларации в электронном или бумажном виде, изменились. С 1 квартала 2020 года в соответствии с п. 4 ст.80, п. 10 ст. 431 НК РФ устанавливается новый предел численности сотрудников
:- компании, численность сотрудников которых превышает 10 человек, обязаны предоставлять отчёт в электронном виде, ранее этот параметр составлял 25 человек
- компании, созданные в отчётном периоде, в том числе путём реорганизации, обязаны отчитываться в электронном виде при численности сотрудников, превышающей 10 человек, а не 25, как было ранее
Юридические лица и ИП, у которых численность сотрудников менее 10 человек, могут выбирать способ сдачи отчёта самостоятельно: предоставить расчёт на бумажном носителе лично, отправить его заказным письмом с описью вложения по почте или сдать по электронным каналам связи.
Контрольные соотношения при проверке расчёта
Налоговая служба изменила правила проверки контрольных соотношений (КС) начисленных сумм в расчёте по страховым взносам. Теперь действия проверяющих органов регламентированы письмом ФНС № БС-4-11/2002@ от 07.02.2020 г. В документе все изменения представлены в виде подробной таблицы. Новые КС позволяют более качественно сравнивать начисленные в рамках трудовых договоров суммы выплат сотрудникам не только с размером установленного регионом МРОТ, но и со средними показателями заработной платы в определённых отраслях за предыдущий период. Такая методика позволит более эффективно выявлять «чёрные» зарплаты. В общей сложности список контрольных соотношений сократился, но при это стал более эффективным.
В Контур.Экстерне проверки на новые контрольные соотношения уже встроены: если обнаружится ошибка, система не даст отправить расчёт.
Большинство контрольных соотношений отчёта оценивается в соответствии с кодом тарифа. При обнаружении ошибки проверяющий высылает уведомление о несоответствии, которое нужно устранить в указанные сроки.
При обнаружении ошибки проверяющий высылает уведомление о несоответствии, которое нужно устранить в указанные сроки.
Обособленные подразделения и филиалы с отдельными р-сч
Обособленные подразделения и филиалы, у которых открыт отдельный расчётный счёт, должны предоставлять расчёт по страховым взносам в местный налоговый орган (п. 11 ст. 431 НК РФ). С 2020 года наличие счёта в банке стало определяющим условием. Благодаря такой доработке было достигнуто соответствие НК РФ с законом о пенсионном страховании, в котором постановка подразделения на учёт в качестве страхователя возможно только при наличии отдельного расчётного счёта.
Для компаний, имеющих обособленные подразделения без расчётного счёта, которые в период 2017—2019 гг. имели право сдавать отчётность по страховым взносам в местную налоговую, предусмотрено два варианта действий:
- Открыть расчётный счёт и продолжить отчитываться по старой схеме.
- Предоставить в налоговые органы заявление о лишении подразделения полномочий предоставлять консолидированную отчётность, в которую входят сведения о начислениях филиала, по месту нахождения.

Таким образом, в соответствии с пп. «а», «в» п. 85 ст. 2, ч. 3 ст. 3 закона № 325-ФЗ с 1 января 2020 г. перечислять страховые взносы и предоставлять по ним декларацию могут только те обособленные подразделения, которые осуществляют выплаты в пользу сотрудников и имеют отдельный расчётный счёт.
Форма расчёта и порядок заполнения формы РСВ
Для того чтобы отчитаться по социальным взносам за IV квартал 2020 придется использовать новую форму, утвержденную Приказом ФНС РФ от 15.10.2020 N ЕД-7-11/751@.
Читайте подробнее Новая форма РСВ 2020 года
Форма расчёта стала более простой, однако новые изменения нельзя назвать кардинальными. Заполнять документ наиболее удобно в следующем порядке: сначала оформляется титульный лист, затем Раздел 3 и остальные приложения, и только в самом конце переходить к заполнению первого раздела.
Титульный лист
Главным новшеством титульного листа является появление поля для отражения информации о среднесписочной численности персонала. Подобное новшество освободило компании и ИП от представления в органы ФНС самостоятельного отчёта о численности.
Подобное новшество освободило компании и ИП от представления в органы ФНС самостоятельного отчёта о численности.
Разберём построчное заполнение.
ИНН — 10-значный номер налогоплательщика (12-значный для ИП)
КПП — 9-значный код, который присвоен инспекцией, куда подается декларация
Номер корректировки — при первичной подаче отчета «0–», при уточненном отчете — порядковый номер корректировки.
Расчётный период — указывается код периода (см. таблицу)
| Налоговый период | Для юридических лиц и ИП | В случае реорганизации (ликвидации) |
| I квартал | 21 | 51 |
| полугодие | 31 | |
| 9 месяцев | 33 | 53 |
| год | 34 | 90 |
По месту нахождения (учёта) (код) — полный перечень приведён в Приложении № 4 к Порядку заполнения, наиболее распространёнными являются « 120» для ИП и «214» для организаций.
Наименование организации — полное наименование налогоплательщика из учредительных документов.
Среднесписочная численность — указывается численность персонала, которая рассчитывается в соответствии п. 76—79.11 приказа Росстата от 27 ноября 2019 года № 711.
Код по ОКВЭД2 — значение из классификатора ОКВЭД2, соответствующее виду осуществляемой деятельности.
Далее представлен блок, заполняемый в случае реорганизации (ликвидации) организации.
Номер контактного телефона
отражается с кодом страны и города. Все цифры прописываются подряд без пропусков и иных символов.Отражается количество листов декларации, а при наличии — количество листов подтверждающих документов.
В завершении указывается ФИО лица, удостоверяющего достоверность и полноту представленных сведений.
Подпись и дата.
Титульный лист
Раздел 1
Если компания в отчётном периоде проводила выплаты своим сотрудникам, то по строке 001 «Тип плательщика (код)» указывается цифра 1, для тех кто не производил выплаты предусмотрен код 2. Соответственно, в первом случае в строках 031-033 должны быть указаны соответствующие начисления, во втором – проставлены нулевые значения.
Соответственно, в первом случае в строках 031-033 должны быть указаны соответствующие начисления, во втором – проставлены нулевые значения.
Для строк 111-113 предусмотрены исключения. Это сделано для возможности отражения в расчёте возмещения расходов в связи с временной нетрудоспособностью сотрудников, даже в том случае, когда заработная плата не начислялась.
Нулевая отчётность должна состоять из титульного листа, Раздела 1 без приложений, в котором будет указан код 2, и Раздел 3 без таблицы 3.2.
Раздел 1 состоит из 9 приложений.
Если в отчётном периоде компанией применялось несколько тарифов, то Приложение 1 к Разделу 1, как и прежде заполняется в нескольких экземплярах. Код тарифа указывается в соответствии с проведёнными изменениями в классификаторе. Обратите внимание, что в новой форме исключены коды 02 и 03. Для тех, кто применяет основной тариф начисления страховых платежей, предусмотрен код 01, который указывается независимо от выбранной системы налогообложения.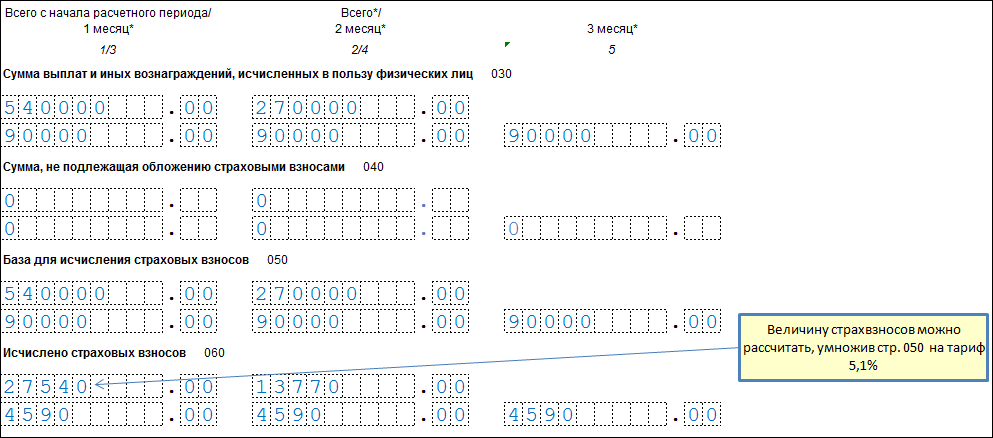 Также из реестра убраны коды 04 и 05, которые проставлялись в случае использования пониженных тарифных ставок. В связи с внесёнными изменениями в законодательство действие таких льгот прекращено.
Также из реестра убраны коды 04 и 05, которые проставлялись в случае использования пониженных тарифных ставок. В связи с внесёнными изменениями в законодательство действие таких льгот прекращено.
В реестр в течение года были введены следующие коды:
| Новый код | Кто указывает |
| 17 | Организации из единого реестра резидентов Особой экономической зоны в Калининградской области (Федеральный закон от 10.01.2006 № 16-ФЗ) |
| 18 | Российские компании, которые производят и продают свою анимационную аудиовизуальную продукцию независимо от вида договора и (или) оказание услуг (выполнение работ) по созданию анимационной аудиовизуальной продукции |
| 19 | Плательщики взносов со статусом участника специального административного района (Федеральный закон от 03.08.2018 № 291-ФЗ), которые платят членам экипажа судна за исполнение трудовых обязанностей. |
В Подразделе 1.1 и 1.2 Приложения 1 присутствует строка 045, которая предназначена для формирования суммы расходов, принимаемых к вычету, которые имеют отношение к получению дохода по договорам, перечисленным в п. 8 ст. 421 НК РФ. В данной строке отражаются расходы, которые имеют документальное подтверждение, а также те, что принимаются к вычету в установленных размерах, независимо от наличия документального подтверждения.
В новой форме Расчёт по страховым взносам в Приложении 2 появилась новая строка «Код тарифа плательщика». Теперь, при одновременном использовании разных тарифов данный раздел нужно будет заполнять на нескольких листах, по аналогии с Приложением 1. Также в форму добавлена новая строка 015 для отражения количества людей, с выплат которых начислены страховые платежи.
Блок строк 001-006 предназначен для указания начислений по каждому отдельному тарифу. В строках 070-090 указываются общие суммы по всем применяемым тарифам. Строка 055 предназначена для указания налоговой базы, с которой начисляются взносы лицам без гражданства по ставке 1,8%.
В строках 070-090 указываются общие суммы по всем применяемым тарифам. Строка 055 предназначена для указания налоговой базы, с которой начисляются взносы лицам без гражданства по ставке 1,8%.
Приложение 5 разработано для расчёта соответствия условий применения IT-компаниями пониженного тарифа в соответствии с пп. 3 п. 1 ст. 427 НК РФ. При заполнении раздела в новой РСВ нужно использовать новые коды тарифов. В таблицу также добавлена новая строка 060 для отражения сведений о регистрации компании в форме резидента особой зоны.
Добавлено Приложение № 5.1, которое заполняется в случае применения пониженного тарифа.
Приложение 6 также предназначено для определения правомерности применения пониженного тарифа для некоммерческих организаций, применяющих УСН и тарифы, установленные пп. 3 п. 2 ст. 427 НК РФ.
Приложение 7 заполняют организации, которые заняты производством анимационной и аудиовизуальной продукции с применением пониженного тарифа, установленного пп. 6 п. 2 ст. 427 НК РФ. В новой редакции расширен перечень кодов (см. Приложение № 7 РСВ)
6 п. 2 ст. 427 НК РФ. В новой редакции расширен перечень кодов (см. Приложение № 7 РСВ)
Приложение 8 предназначено для информации по временно пребывающим иностранным гражданам, которые уплачивают взносы по ставке 1,8%. Ранее такие сведения отражались в приложении 9.
Приложение 9 заполняют страхователи, имеющие сотрудников, которые проходят обучение или работают в студенческих отрядах. Пенсионные взносы с данных выплат не начисляются. В предыдущей редакции для таких страхователей отводилось приложение 10.
Раздел 2
Данный раздел формы Расчёт по страховым взносам полностью предназначен для крестьянских и фермерских хозяйств. Новые изменения коснулись только Приложения 1, где при указании личных данных членов хозяйства теперь нужно будет прописывать паспортные данные, пол и дату рождения и полностью. Заполнение данного раздела не представляет особой сложности.
Раздел 3
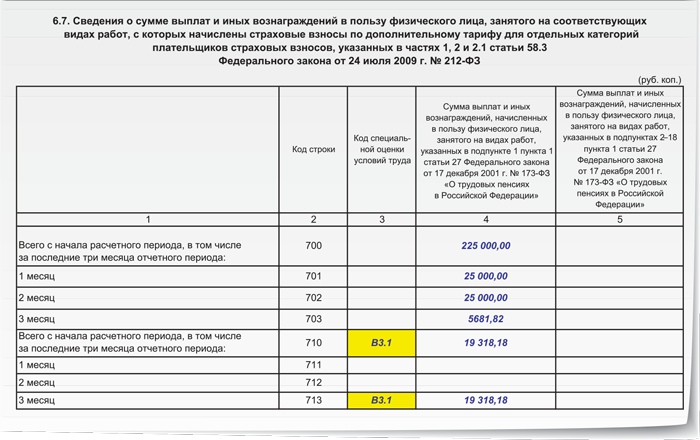
Рассматриваемая форма предназначена для отражения персонифицированных сведений. Для подраздела 3.2.2 разработана новая кодировка, устанавливающая основание начисления взносов по дополнительному тарифу и в соответствии с условиями труда.
Для подраздела 3.2.2 разработана новая кодировка, устанавливающая основание начисления взносов по дополнительному тарифу и в соответствии с условиями труда.
| Код | Наименование |
| 110 | Занятые на видах работ, указанных в п. 1 ч. 1 ст. 30 400-ФЗ, в отношении выплат которых применён доптариф (п. 1 ст. 428 НК РФ) |
| 120 | Занятые на видах работ, указанных в п. 2–18 ч. 1 ст. 30 400-ФЗ, в отношении выплат которых применён доптариф (п. 2 ст. 428 НК РФ) |
| 131 | Занятые на видах работ, указанных в п. 1 ч. 1 ст. 30 400-ФЗ, класс условий труда — вредный, подкласс условий труда — 3.1 |
| 132 | Занятые на видах работ, указанных в п. 1 ч. 1 ст. 30 400-ФЗ, класс условий труда — вредный, подкласс условий труда — 3.2 |
| 133 | Занятые на видах работ, указанных в п. 1 ч. 1 ст. 30 400-ФЗ, класс условий труда — вредный, подкласс условий труда — 3.3 1 ч. 1 ст. 30 400-ФЗ, класс условий труда — вредный, подкласс условий труда — 3.3 |
| 134 | Занятые на видах работ, указанных в п. 1 ч. 1 ст. 30 400-ФЗ, класс условий труда — вредный, подкласс условий труда — 3.4 |
| 140 | Занятые на видах работ, указанных в п. 1 ч. 1 ст. 30 400-ФЗ, класс условий труда — опасный, подкласс условий труда — 4 |
| 231 | Занятые на видах работ, указанных в п. 2–18 ч. 1 ст. 30 400-ФЗ, класс условий труда — вредный, подкласс условий труда — 3.1 |
| 232 | Занятые на видах работ, указанных в п. 2–18 ч. 1 ст. 30 400-ФЗ, класс условий труда — вредный, подкласс условий труда — 3.2 |
| 233 | Занятые на видах работ, указанных в п. 2–18 ч. 1 ст. 30 400-ФЗ, класс условий труда — вредный, подкласс условий труда — 3.3 |
| 234 | Занятые на видах работ, указанных в п. 2–18 ч. 1 ст. 30 400-ФЗ, класс условий труда — вредный, подкласс условий труда — 3. 4 4 |
| 240 | Занятые на видах работ, указанных в п. 2–18 ч. 1 ст. 30 400-ФЗ, класс условий труда — опасный, подкласс условий труда — 4 |
Раздел 3
Правила предоставления корректировочных сведений
При обнаружении ошибки в ранее предоставленном расчёте или при недоплате взносов обязательно сдаётся уточнённый расчёт. Он должен состоять из тех же приложений, которые были поданы ранее. В уточняющем документе обязательно указывается номер корректировки.
Если вам нужно отменить ранее предоставленные сведения, то в строке 010 Раздела 3 необходимо проставить признак аннулирования «1», а строки 130-170, 190-210 оставить незаполненными.
Если в ранее представленном расчёте обнаружена ошибка в личных данных застрахованного лица, то порядок заполнения коррекционного отчёта будет следующим:
- Страхователь заполняет Раздел 3 с ошибочными сведениями и указывает в нём признак аннулирования «1», в подразделе 3.
 2.1 ставятся прочерки.
2.1 ставятся прочерки. - Раздел 3 заполняется ещё раз, в него вносятся исправленные данные и заполняется подраздел 3.2.1. В этом случае признак аннулирования уже не указывается.
В итоге в состав уточнённого расчёта войдёт два листа: один с ошибочными сведениями, а второй правильный. Для уточнения других неточностей в Разделе 3 необходимо просто ещё раз подать документ с указанием верной информации. При этом в персонифицированный раздел должен быть заполнен полностью, а не только исправленные строки.
Бланк формы РСВ на 2021 год
Скачать бланк формы РСВ на 2020—2021 года в формате .xls
Образец заполнения РСВ за IV кв. 2020 года
Скачать образец заполнения РСВ за IV квартал 2020 года в формате .xls
Нормативно-правовая база
Пример заполнения РСВ за 1 квартал 2021 года
РСВ за 1 квартал 2021 – пример заполнения этого отчета приводим ниже – оформляйте на новом бланке. Рассмотрим, в чём состоят особенности его заполнения и какие изменения привнес 2020 год.
Рассмотрим, в чём состоят особенности его заполнения и какие изменения привнес 2020 год.
Расчет по страховым взносам: суть, форма и варианты отчета
Расчет по страховым взносам за 1 квартал 2021 года оформляйте на новом бланке, утвержденном приказом ФНС России от 18.09.2019 № ММВ-7-11/470@ в редакции приказа ФНС от 15.10.2020 № ЕД-7-11/751@.
Что изменилось в формуляре, см. здесь. Скачать бланк для заполнения можно у нас на сайте.
Бланк единого расчета по страховым взносам-2021 Скачать
Расчет по страховым взносам (РСВ) обязателен к формированию для всех работодателей, в т. ч. и тех, у кого временно отсутствуют данные для его составления. В последнем случае может возникать необходимость сдачи отчета с нулевыми показателями в основных разделах.
Как заполнить нулевой расчет по страхвзносам, читайте здесь.
Обязательными для заполнения большинством составителей РСВ являются титульный лист, разделы 1 и 3, посвященные, соответственно, общим данным об исчислении взносов и персональным сведениям о получателях доходов, на которые начисляются взносы. К разделу 1 предусмотрено 10 приложений, заполнить первое и второе из которых нужно непременно (они отведены начислениям по основным тарифам), а остальные — по мере необходимости. Раздел 2 предназначен для глав фермерских хозяйств и поэтому используется нечасто.
К разделу 1 предусмотрено 10 приложений, заполнить первое и второе из которых нужно непременно (они отведены начислениям по основным тарифам), а остальные — по мере необходимости. Раздел 2 предназначен для глав фермерских хозяйств и поэтому используется нечасто.
Об особенностях заполнения каждого из разделов РСВ читайте в статье «Единый расчет по страховым взносам – бланк».
На нашем форуме можно получить ответ на любой вопрос, возникший у вас в ходе заполнения и сдачи отчетности по взносам. Например, тут обсуждаем возможные причины несоответствия данных РСВ и СЗВ-М, а также способы исправления этого несоответствия.
Образец расчета по страховым взносам за 1 квартал 2021 года
РСВ — отчет, составляемый ежеквартально, но данные его формируются по-разному:
- в разделе 1 — нарастающим итогом в течение года с выделением данных, относящихся к месяцам последнего квартала отчетного периода;
- в разделе 3 — только за последний квартал отчетного периода.

В силу этого абсолютная корреляция данных между этими разделами имеет место только в отчете за 1 квартал. Соответственно, отчет за этот период проще всего заполнить и достаточно легко проверить.
Построчный алгоритм заполнения РСВ с 2021 года описан в Готовом решении от КонсультантПлюс. Если у вас еще нет доступа к этой правовой системе, пробный доступ можно получить бесплатно.
О способах, дающих возможность самостоятельной проверки сформированного отчета, читайте в материале «Как не запутаться в контрольных соотношениях к расчету по страховым взносам».
Составляя расчет страховых взносов за 1 квартал 2021 года, на его титульном листе нужно указать код периода, соответствующий 1 кварталу (21).
Образец заполнения РСВ за 1 квартал 2021 года можно скачать в КонсультантПлюс, получив бесплатный пробный доступ к системе:
Типичные ошибки в РСВ и возможность их исправления без санкций
Срок сдачи отчета установлен на 30-е число месяца, наступающего после окончания отчетного периода (п. 7 ст. 431 НК РФ). Однако на него влияют совпадения с выходными днями. Отчет за 1 квартал 2021 нужно сдать до 30.04.2021.
7 ст. 431 НК РФ). Однако на него влияют совпадения с выходными днями. Отчет за 1 квартал 2021 нужно сдать до 30.04.2021.
Способов сдачи существует два: электронный и бумажный. Последний доступен лицам, отчитывающимся за работников, общее количество которых не превышает 10.
Напомним! Ранее порог для бумажного отчета составлял 25 человек. Но с 2020 года он был снижен до 10. Подробности см. здесь.
Однако факт отправки РСВ в ИФНС еще не позволяет считать, что отчет сдан. В момент приемки налоговым органом осуществляется входной контроль на предмет наличия расхождений (п. 7 ст. 431 НК РФ):
- в рассчитываемых по каждому работнику суммах;
- в персональных данных, относящихся к застрахованному лицу;
- в сопоставимых цифрах разделов 1 и 3.
Если такие расхождения выявлены, ИФНС извещает подателя отчетности о непринятии отчета и обнаруженных несоответствиях. Оперативное уточнение РСВ дает возможность считать его сданным в дату подачи первого (оказавшегося непринятым) отчета.
О том, какие сроки действуют для такой корректировки, а также об особенностях оформления уточненного отчета читайте в этой статье.
Итоги
РСВ за 1 квартал 2021 года оформляйте на новом бланке, приказом ФНС России от 18.09.2019 № ММВ-7-11/470@ в редакции от 15.10.2020. Сдача его обязательна для всех работодателей, в т. ч. для тех, кто не осуществлял в отчетном периоде выплату доходов. Срок подачи отчета за 1 квартал 2021 года 30.04.2021.
Источники:
- Налоговый кодекс РФ
- приказ ФНС России от 18.09.2019 № ММВ-7-11/470@

Пробный бесплатный доступ к системе на 2 дня.
Как заполнить РСВ за полугодие 2020 года: рекомендации
Все работодатели, уплачивающие страховые взносы с выплат физлицам, обязаны ежеквартально подавать расчет по страховым взносам в отделения ФНС по месту своего нахождения. Срок сдачи РСВ за полугодие 2020 года – 30 июля.
Электронный формат подачи РСВ предусмотрен для компаний, численность сотрудников в которых больше 10 человек. Если работников меньше, можно отправлять отчет как в электронном виде, так и на бумаге.
Подробные инструкции по подготовке расчета по страховым взносам содержатся в приложении № 2 к Приказу ФНС России от 18.09.2019 N ММВ-7-11/470@.
Обязательными для заполнения являются:
- титульный лист,
- разделы 1 и 3,
- приложение 1 (подразделы 1.1 и 1.
 2) и приложение 2 к разделу 1.
2) и приложение 2 к разделу 1.
Остальные листы включаются в расчет плательщиками при наличии соответствующих условий и сведений. Например, если выплачивались пособия за счет ФСС, заполняется приложение 3 к первому разделу, а если страховые взносы на ОПС начислялись по дополнительным тарифам – подразделы 1.3.1, 1.3.2 приложения 1.
Если компания в течение последних трех месяцев не вела деятельность и не выплачивала доход работникам, следует подать нулевой РСВ, включающий титульный лист, разделы 1 (без приложений) и 3.
О порядке подачи и заполнения нулевого РСВ за полугодие 2020 года читайте в статье «Нулевой расчет по страховым взносам: как заполнить».
Рекомендации по заполнению РСВ за полугодие
В поле «Код расчетного периода» на титульном листе указывается «31», календарный год – 2020. Наименование организации или ФИО индивидуального предпринимателя нужно записать без сокращений. Номер контактного телефона вносится по следующему шаблону: «8», пробел, код, пробел, номер.
Номер контактного телефона вносится по следующему шаблону: «8», пробел, код, пробел, номер.
На каждого застрахованного сотрудника по данным за последние три месяца отдельно заполняется раздел 3. «Код вида документа, удостоверяющего личность» можно взять из Приложения 6 к порядку заполнения расчета. Коды стран указаны в Общероссийском классификаторе стран мира. Значения для поля «Код категории застрахованного лица»:
- НР – для граждан РФ;
- ВПНР – временно пребывающие иностранцы;
- ВЖНР – временно проживающие иностранцы.
В графе 140 раздела 3 отражаются все платежи работнику, включая необлагаемые выплаты сверх предельной базы. Выплаты, которые не являются объектом обложения по ст. 420 НК РФ, в расчете не указываются.
Пособия, начисленные за счет ФСС в период январь-июнь 2020 года (больничные, по уходу за ребенком, на погребение и т.д.), отражаются в приложении 3. При этом не важны дата платежа и период, за который пособие начислено, – только дата начисления суммы (Письмо Минфина от 20.11.2019 N 03-15-06/89513).
При этом не важны дата платежа и период, за который пособие начислено, – только дата начисления суммы (Письмо Минфина от 20.11.2019 N 03-15-06/89513).
Суммы взносов к уплате указываются в разделе 1 РСВ за полугодие. В приложениях 1 и 2 показываются выплаты по всей организации и начисленные с них взносы. Если организация-плательщик (на ОСН и УСН) начисляет взносы по основным тарифам, в поле «Код тарифа» вписывается «01».
РСВ за полугодие для МСП
Для представителей малого и среднего предпринимательства налоговая служба разработала временные коды и контрольные соотношения для РСВ, которые нужно учесть при подготовке расчета за полугодие.
Код тарифа плательщика в РСВ
Согласно письму ФНС России от 07.04.2020 N БС-4-11/5850@, компании, относящиеся к МПС и применяющие пониженные тарифы в отношении части выплат, превышающих МРОТ, должны указывать код тарифа плательщика страховых взносов – «20». Напомним, его надо указать в приложениях 1 и 2 по строке 001.
Напомним, его надо указать в приложениях 1 и 2 по строке 001.
Для компаний, которым в период апрель-июнь текущего года установлен нулевой тариф взносов ( ст. 3 Федерального закона от 08.06.20 № 172-ФЗ), введен другой код тарифа – «21». Его должны применять организации и ИП, включенные в реестр МСП и работающие в наиболее пострадавших из-за пандемии отраслях.
Код застрахованного лица в РСВ
Также для МСП предусмотрены новые коды категории застрахованного лица (строка 130 в подразделе 3.2.1 раздела 3):
- МС – физические лица;
- ВЖМС – застрахованные иностранцы и лица без гражданства, временно проживающие в РФ, а также те, которым предоставлено временное убежище;
- ВПМС – иностранные граждане и лица без гражданства, временно пребывающие в РФ (кроме высококвалифицированных специалистов).
Для работодателей, применяющих нулевой тариф, налоговики предлагают другие коды застрахованных лиц для работников, страховые взносы с выплат которым исчисляются в соответствии с законом № 172-ФЗ: КВ, ВЖКВ, ВПКВ.
Нововведения по кодам учтены в контрольных соотношениях к РСВ, которые ФНС дополнила и уточнила в письмах от 29 мая 2020 г. N БС-4-11/8821@ и от 10.06.2020 N БС-4-11/9607.
Документы:
Отчетность за полугодие 2020
Закажите бесплатный сборник материалов от КонсультантПлюс «Отчетность за 1 полугодие 2020 года»! Подборка содержит формы и образцы заполнения РСВ, 6-НДФЛ, деклараций по НДС, налогу на прибыль и т.д., а также информацию о «коронавирусных» изменениях в отчетности.
Что поменялось в порядке заполнения РСВ с I квартала 2021 года в связи с переходом на прямые выплаты
С 1 января 2021 года во всех регионах пособия больше не засчитываются в счет уплаты страховых взносов (ст. 6 Федерального закона от 29.12.2020 N 478-ФЗ). После перехода на прямые выплаты работодатели должны продолжать оплачивать первые три дня больничного, допвыходные для ухода за ребенком-инвалидом и перечислять пособие на погребение. Эти суммы нельзя зачесть в счет уплаты страховых взносов.
Эти суммы нельзя зачесть в счет уплаты страховых взносов.
В связи с этим ФНС России в Письме от 29.01.2021 N БС-4-11/1020@ направила разъяснения страхователям и нижестоящим налоговым органам о порядке заполнения РСВ до внесения соответствующих изменений в его форму.
Начиная с отчетного периода I квартал 2021 года при заполнении РСВ необходимо:
- строку 070 «Произведено расходов на выплату страхового обеспечения» приложения 2 к разделу 1 РСВ оставлять пустой;
- строку 080 «Возмещено ФСС расходов на выплату страхового обеспечения» приложения 2 к разделу 1 РСВ заполнять при возмещении ФСС расходов за периоды, истекшие до 1 января 2021 года;
- при заполнении строки 090 «Сумма страховых взносов, подлежащая уплате (сумма превышения произведенных расходов над исчисленными страховыми взносами)» приложения 2 к разделу 1 РСВ признак «2» больше не используется;
- приложение 3 «Расходы по ОСС на случай ВНиМ и расходы, осуществляемые в соответствии с законодательством РФ» к разделу 1 РСВ и Приложение 4 «Выплаты, произведенные за счет средств, финансируемых из федерального бюджета» к разделу 1 РСВ не заполнять.

На заметку: пошаговую инструкцию по заполнению РСВ за I квартал 2021 года смотрите в Готовом решении: Как заполнить и представить в налоговый орган расчет по страховым взносам за отчетные (расчетный) периоды 2021 г. (КонсультантПлюс, 2021).
Читайте подробнееНовая форма РСВ с 2020 года
Приказом ФНС от 15.10.2020 N ЕД-7-11/751@ утверждена новая форма РСВ, которая будет применяться, начиная с отчетности за 2020 г.
Новая форма РСВ с 2020 года
Новая РСВ реализована в ЗУП 3.1.14.334 и 3.1.16.77 и БП 3.0.84.46.
В новой форме на Титульный лист добавлен показатель среднесписочной численности организации.
В форму будут включены все произошедшие изменения в законодательстве по страховым взносам.
С 2021 г. для ИТ-компаний будет применяться пониженный тариф.
Подробнее см. — Подписан закон с новыми пониженными тарифами взносов для IT-компаний
Такой же тариф будет применяться для организаций-производителей радиоэлектроники.
Т.к. тариф одинаковый и условия применения очень похожи, то решено было добавить Приложение 5.1, которое будет заполняться с отчетности за 1 квартал 2021 г. ИТ-компаниями и производителями радиоэлектроники (в отчете за 2020 г. ИТ-компаниям нужно будет заполнить Приложение 5).
В Приложении 5.1 организации будут указывать Код плательщика:
- «1» — ИТ-компания
- «2» — производитель радиоэлектроники
Показатели Приложения 5.1 похожи на показатели Приложения 5.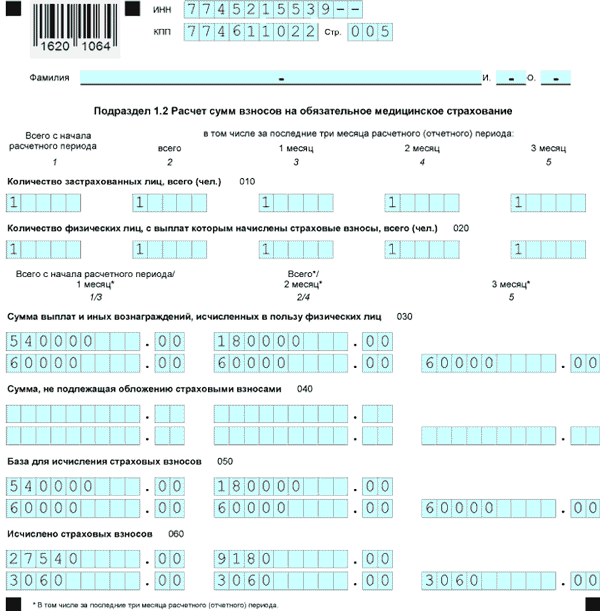
В 2020 г. добавлены новые коды тарифов, которые будут использоваться в новой форме РСВ:
- 20 – при льготном тарифе по страховым взносам для МСП
- 21 – при нулевом тарифе по страховым взносам для МСП из отраслей, наиболее пострадавших от пандемии
- 22 – для тарифа производителей радиоэлектроники
И соответствующие категории застрахованных лиц:
- МС — лица, которым с части выплат и вознаграждений, превышающей МРОТ, исчисляют взносы СМП
- КВ — лица, застрахованные в системе ОПС, при нулевом тарифе по страховым взносам
- ЭКБ — лица, с выплат и вознаграждений которым исчисляются страховые взносы по тарифу для производителей радиоэлектроники.
Как до наступления 2021 г. сформировать новую РСВ за 2020 г.
См. также:
Если Вы еще не подписаны:
Активировать демо-доступ бесплатно →
или
Оформить подписку на Рубрикатор →
После оформления подписки вам станут доступны все материалы по 1С:ЗУП, записи поддерживающих эфиров и вы сможете задавать любые вопросы по 1С.
Помогла статья?
Получите еще секретный бонус и полный доступ к справочной системе БухЭксперт8 на 14 дней бесплатно
Шлюз для приема расчетов по форме 4 ФСС РФ в электронном виде с использованием электронно-цифровой подписи Оценить качество госуслуг |
(237. |
|
ООО РСВ – что это за организация, пришло письмо
В последние годы люди всё реже получают «бумажные письма» – большинство уведомлений рассылается на электронную почту или приходит в смс-сообщениях на смартфон. Однако, иногда почтовый ящик человека всё же посещает кое-что кроме извещения о выплатах по квартплате, что действительно настораживает. Если вам пришло письмо от отправителя ООО РСВ, этот материал ответит на все интересующие вопросы.
Если вам пришло письмо от отправителя ООО РСВ, этот материал ответит на все интересующие вопросы.
Что за письмо пришло от ООО РСВ, что в них?
Чаще всего подобное извещение выглядит довольно странно – несколько печатей на конверте, неточный или вовсе отсутствующий адрес вызывают некоторую настороженность. В начале самого бланка указывается ФИО и точный адрес проживания получателя, после чего следует множество непонятного текста.
Основная мысль заключается в следующем – с первых предложений человека уведомляют о его долге перед банком, организацией или человеком. Далее следует смягчительное предложение оплатить неустойку в добровольной форме, во избежание последующих проблем и судебных тяжб.
Письмо уведомление от ООО “Кредитэкспресс Финанс”
Существует 2 варианта аргументирования столь неожиданного вмешательства:
- Долг человека был продан коллекторской организации ввиду долгой неуплаты, поэтому сейчас плательщик обязан выплачивать полную сумму (возможно, с накапливающимися процентами) уже не банку, человеку или компании, а агентству.

- Вопросом неуплаты устойчивого долга опять же занимается коллекторское агентство, но в этом случае является посредником в сложившейся ситуации. То есть, выступает своеобразным «переговорщиком» для урегулирования финансового конфликта.
Для того, чтобы составить полную картину сложившейся ситуации, стоит немного рассказать о самой мифической организации ООО РСВ.
Что это за компания и чем занимается?
На самом деле, за шестью непонятными буквами скрывается вполне обыденное для современного мира определение. Организация “ООО РСВ” – это общество с ограниченной ответственностью «Региональная служба взыскания», если описывать их просто – коллекторское агенство.
Генеральным директором организации является «Кредитэкспресс Финанс», выступающий в роли управляющей компании. Судя по юридическому адресу, организация располагается в Москве по адресу: улица Бутырский вал, дом 68/70 и занимает несколько помещений (уточнения могут прилагаться в письме, точной информации нет).
- Горячий телефон организации 8-800-775 76 23 (дополнительный 8-499-750 15 76). Однако, в случае чего, сотрудники сами позвонят вам, и далее мы поясним почему.
- Электронная почта [email protected], а официальный сайт rsvcollection.ru.
Согласно Законодательству РФ, подобные организации имеют право коммуницировать с должником посредством извещений (писем на почту), звонков и личных встреч. Осуществление перечисленных действий возможно с 8 утра до 22 вечера, кроме выходных и праздничных дней.
Организация “ООО РСВ” – это коллекторское агенство
Простыми словами – агентство занимается выбиванием долгов, хотя большинство получающих такие «письма счастья» скорее в курсе ситуации. Вышеупомянутые «рамки гнёта» предоставлены для ознакомления и предъявления в случае нарушения – грубо говоря, вы можете не отвечать на звонки и стук в двери, если вам звонят или приходят на порог в ночное время суток.
Если вы считаете, что вас преследуют несправделиво, или же ООО РСВ начинает переходить рамки дозволенного – обратитесь за консультацией к юристам или в полицию.
Отзывы о коллекторском агентстве ООО РСВ
Очевидно, что коллекторское агентство ООО РСВ имеет 95% отрицательных отзывов от пользователей сети, так как подтверждает чуть ли не все стереотипы о подобных организациях.
Согласно описаниям, к должникам приходят амбалы в возрасте от 50 лет, не соблюдающие нормы морали и нравственности. Частые угрозы родным и близким жертвам собственной глупости и безысходности – обычное дело.
По утверждению ООО РСВ, они работают в сотрудничестве с судебными приставами
Некоторые отзывы и вовсе написаны посторонними в ситуации людьми. К примеру, коллега одного из должников получает телефонный звонок, в котором грозный голос угрожает ему и его детям чуть ли не расправой, если знакомый в течение нескольких часов не вернёт деньги в банк.
Естественно, с подобной ситуацией хотя бы в теории знаком каждый житель России, поэтому при получении письма от ООО РСВ стоит насторожиться – начинайте искать необходимую сумму или предупредите родственников о предстоящих «неприятных звонках и визитах».
Заключение
Если вам на почту пришло письмо от организации ООО РСВ, то не стоит паниковать. Теперь вы знаете что это за агенство. Для начала обратитесь в ваш банк и проконсультируйтесь. Далее наберите телефон этих коллекторов и уточните всю законность их требований, обязательно проконсультируйтесь с юристами.
Если вы точно знаете, что никаких операций по кредитам за вами не числится – просто проигнорируйте письмо. Есть вероятность, что на базе имени этого агенства могут действовать мошенники, полагающиеся на испуг граждан и удачу. Пишите о вашем случае в комментариях ниже.
Симптомы и лечение RSV (респираторно-синцитиального вируса)
Симптомы
Люди, инфицированные RSV, обычно проявляют симптомы в течение 4-6 дней после заражения. Симптомы RSV-инфекции обычно включают
- Насморк
- Снижение аппетита
- Кашель
- Чихание
- Лихорадка
- Свистящее дыхание
Эти симптомы обычно проявляются поэтапно, а не сразу. У очень маленьких детей с RSV единственными симптомами могут быть раздражительность, снижение активности и затрудненное дыхание.
У очень маленьких детей с RSV единственными симптомами могут быть раздражительность, снижение активности и затрудненное дыхание.
Почти все дети будут инфицированы RSV к своему второму дню рождения.
медицинский значок
Позвоните своему врачу, если у вас или у вашего ребенка затрудненное дыхание, недостаточное потребление жидкости или ухудшение симптомов.
Уход
Большинство инфекций RSV проходят самостоятельно через неделю или две.
Специфического лечения RSV-инфекции не существует, хотя исследователи работают над разработкой вакцин и противовирусных препаратов (лекарств, которые борются с вирусами).
Принять меры для облегчения симптомов
- Снимайте лихорадку и боль с помощью безрецептурных жаропонижающих и болеутоляющих средств, таких как парацетамол или ибупрофен. (Никогда не давайте аспирин детям.)
- Пейте достаточно жидкости. Людям с RSV-инфекцией важно пить достаточно жидкости, чтобы предотвратить обезвоживание (потерю жидкости в организме).

- Поговорите со своим лечащим врачом , прежде чем давать ребенку лекарства от простуды, отпускаемые без рецепта.Некоторые лекарства содержат ингредиенты, которые не подходят для детей.
RSV может вызвать более серьезные проблемы со здоровьем
RSV также может вызывать более серьезные инфекции, такие как бронхиолит, воспаление мелких дыхательных путей в легких и пневмонию, инфекцию легких. Это наиболее частая причина бронхиолита и пневмонии у детей младше 1 года.
Здоровые взрослые и младенцы, инфицированные RSV, обычно не нуждаются в госпитализации. Но некоторые люди с RSV-инфекцией, особенно пожилые люди и дети младше 6 месяцев, могут нуждаться в госпитализации, если у них проблемы с дыханием или обезвоживание.В самых тяжелых случаях человеку может потребоваться дополнительный кислород или интубация (дыхательная трубка, вставленная через рот в дыхательные пути) с механической вентиляцией легких (аппарат, помогающий человеку дышать). В большинстве случаев госпитализация длится всего несколько дней.
В большинстве случаев госпитализация длится всего несколько дней.
Узнайте больше о людях с высоким риском тяжелой инфекции RSV.
SYNAGIS (паливизумаб) | Веб-сайт для родителей и опекунов
Кому не следует получать SYNAGIS?
Дети не должны получать SYNAGIS, если у них когда-либо была тяжелая аллергическая реакция на него.Признаки и симптомы тяжелой аллергической реакции могут включать зудящую сыпь; отек лица; Трудность глотания; затрудненное дыхание; синеватый цвет кожных покровов; мышечная слабость или вялость; и / или отсутствие ответа. Если у вашего ребенка появляются какие-либо из этих признаков или симптомов тяжелой аллергической реакции после приема SYNAGIS, немедленно обратитесь к лечащему врачу вашего ребенка или обратитесь за медицинской помощью.
Как дается SYNAGIS?
SYNAGIS вводится в виде ежемесячной инъекции, обычно в мышцу бедра (ноги), врачом вашего ребенка.Если у вашего ребенка есть проблемы с кровотечением или легкими синяками, инъекция может вызвать проблему. Ваш ребенок должен получить первую инъекцию SYNAGIS до начала сезона RSV, чтобы защитить его до того, как RSV станет активным. Сезон RSV обычно приходится на весну, но в некоторых регионах он может начаться раньше или длиться дольше. Когда RSV наиболее активен, вашему ребенку необходимо будет получать инъекции SYNAGIS каждые 28-30 дней, чтобы защитить его от тяжелого RSV-заболевания в течение примерно месяца. Ваш ребенок должен продолжать получать ежемесячные инъекции SYNAGIS до конца сезона RSV.После приема SYNAGIS ваш ребенок может по-прежнему заболеть тяжелой формой RSV. Если у вашего ребенка инфекция RSV, ему следует продолжать делать ежемесячные инъекции в течение всего сезона RSV, чтобы предотвратить тяжелое заболевание, вызванное новыми инфекциями RSV.
Ваш ребенок должен получить первую инъекцию SYNAGIS до начала сезона RSV, чтобы защитить его до того, как RSV станет активным. Сезон RSV обычно приходится на весну, но в некоторых регионах он может начаться раньше или длиться дольше. Когда RSV наиболее активен, вашему ребенку необходимо будет получать инъекции SYNAGIS каждые 28-30 дней, чтобы защитить его от тяжелого RSV-заболевания в течение примерно месяца. Ваш ребенок должен продолжать получать ежемесячные инъекции SYNAGIS до конца сезона RSV.После приема SYNAGIS ваш ребенок может по-прежнему заболеть тяжелой формой RSV. Если у вашего ребенка инфекция RSV, ему следует продолжать делать ежемесячные инъекции в течение всего сезона RSV, чтобы предотвратить тяжелое заболевание, вызванное новыми инфекциями RSV.
Эффективность инъекций SYNAGIS, вводимых реже одного раза в месяц в течение сезона RSV, не установлена.
Каковы возможные побочные эффекты SYNAGIS?
К серьезным побочным эффектам относятся тяжелые аллергические реакции, которые могут возникнуть после любой инъекции SYNAGIS и могут быть опасными для жизни или привести к смерти. Позвоните врачу вашего ребенка или немедленно обратитесь за медицинской помощью, если у вашего ребенка есть какие-либо признаки или симптомы серьезной аллергической реакции. См. «Кому не следует получать SYNAGIS?» для дополнительной информации.
Позвоните врачу вашего ребенка или немедленно обратитесь за медицинской помощью, если у вашего ребенка есть какие-либо признаки или симптомы серьезной аллергической реакции. См. «Кому не следует получать SYNAGIS?» для дополнительной информации.
Общие побочные эффекты SYNAGIS включают лихорадку и сыпь.
Это не все возможные побочные эффекты SYNAGIS.
РАЗРЕШЕНИЕ ДЛЯ ИСПОЛЬЗОВАНИЯ
SYNAGIS, 50 мг и 100 мг для инъекций, это лекарство, отпускаемое по рецепту, которое используется для предотвращения серьезного заболевания легких, вызываемого респираторно-синцитиальным вирусом (RSV) у детей:
- , рожденные недоношенными (в возрасте 35 недель или раньше) и которым на начало сезона RSV не исполнилось 6 месяцев
- с хроническим заболеванием легких, называемым бронхолегочной дисплазией (БЛД), которым требовалось лечение в течение последних 6 месяцев, и которым на момент начала сезона RSV возраст 24 месяца или меньше.
- , рожденные с определенными типами сердечных заболеваний и которым на начало сезона RSV не исполнилось 24 месяцев

Неизвестно, является ли SYNAGIS безопасным и эффективным:
- С
- по лечат симптомов RSV у ребенка, у которого уже есть RSV.SYNAGIS используется, чтобы помочь предотвратить болезнь RSV
- у детей старше 24 месяцев на момент начала приема препарата
Щелкните здесь, чтобы получить полную информацию о назначении для SYNAGIS, включая информацию о пациенте.
Чтобы сообщить о ПОДОЗРЕВАЕМЫХ ПОБОЧНЫХ РЕАКЦИЯХ, свяжитесь с 1-866-773-52741-866-773-5274.Респираторно-синцитиальный вирус (RSV) – Диагностика и лечение
Диагноз
Ваш врач может заподозрить респираторно-синцитиальный вирус на основании результатов медицинского осмотра и времени года, в котором возникают симптомы.Во время обследования врач будет прослушивать легкие с помощью стетоскопа, чтобы проверить, нет ли хрипов или других аномальных звуков.
Лабораторные тесты и визуализирующие исследования обычно не требуются. Тем не менее, они могут помочь диагностировать осложнения RSV или исключить другие состояния, которые могут вызывать аналогичные симптомы. Тесты могут включать:
- Анализы крови для проверки количества лейкоцитов или поиска вирусов, бактерий и других микробов
- Рентген грудной клетки для проверки воспаления легких
- Мазок секрета изо рта или носа для проверки на наличие вируса
- Пульсоксиметрия, безболезненный монитор кожи для определения уровня кислорода в крови ниже нормы
Лечение
Лечение респираторно-синцитиального вируса обычно включает меры самопомощи, чтобы вашему ребенку было комфортнее (поддерживающая помощь).Но при появлении серьезных симптомов может потребоваться стационарное лечение.
Поддерживающая терапия
Ваш врач может порекомендовать безрецептурные лекарства, такие как ацетаминофен (тайленол и другие), для снижения температуры. (Никогда не давайте аспирин ребенку.) Использование назальных капель с физиологическим раствором и отсасывание могут помочь очистить заложенный нос. Ваш врач может назначить антибиотики, если есть бактериальное осложнение, например бактериальная пневмония.
Сделайте так, чтобы вашему ребенку было как можно комфортнее.Предложите много жидкости и следите за признаками потери жидкости в организме (обезвоживанием), такими как сухость во рту, незначительное выделение мочи или его полное отсутствие, запавшие глаза, сильная суетливость или сонливость.
Больничная помощь
Если инфекция RSV тяжелая, может потребоваться пребывание в больнице. Лечение в больнице может включать:
- Внутривенные (в / в) жидкости
- Кислород увлажненный
- А дыхательный аппарат (ИВЛ), в редких случаях
Ингалятор (бронходилататор) или стероиды не доказали свою эффективность при лечении инфекции RSV .
Клинические испытания
Изучите исследования клиники Mayo Clinic, в которых тестируются новые методы лечения, вмешательства и тесты как средства предотвращения, обнаружения, лечения или контроля этого состояния.
Образ жизни и домашние средства
Возможно, вам не удастся сократить продолжительность респираторно-синцитиальной вирусной инфекции, но вы можете попытаться облегчить некоторые признаки и симптомы.
Если у вашего ребенка есть RSV , сделайте все возможное, чтобы успокоить или отвлечь его или ее – обнимитесь, почитайте книгу или поиграйте в тихую игру. Другие советы по облегчению симптомов:
- Создавайте влажный воздух для дыхания. Сохраняйте в комнате тепло, но не перегревайте. Если воздух сухой, увлажнитель или испаритель с прохладным туманом могут увлажнить воздух и помочь облегчить заложенность носа и кашель. Обязательно поддерживайте увлажнитель в чистоте, чтобы предотвратить рост бактерий и плесени.
- Пейте жидкости. Продолжайте кормить ребенка грудью или из бутылочки, как обычно. Для детей старшего возраста и взрослых держите постоянный запас прохладной воды у постели больного. Предложите теплые жидкости, например суп, чтобы разжижить сгущенные выделения. Ледяной лед также может успокаивать.
- Попробуйте солевые капли для носа. Капли, отпускаемые без рецепта (OTC) – безопасный и эффективный способ облегчить застойные явления даже у маленьких детей. Следуйте рекомендациям врача и инструкциям на продукте.
- Используйте безрецептурные обезболивающие. OTC болеутоляющие средства, такие как парацетамол (тайленол и др.), Могут помочь снизить температуру и облегчить боль в горле. Посоветуйтесь с врачом, чтобы подобрать дозу, соответствующую возрасту вашего ребенка.
- Держитесь подальше от сигаретного дыма. Пассивное курение может усугубить симптомы.
Подготовка к приему
Если серьезные симптомы не приводят к обращению в отделение неотложной помощи (ER), вы, скорее всего, начнете с посещения семейного врача или врача вашего ребенка.Вот некоторая информация, которая поможет вам подготовиться к приему и узнать, чего ожидать от врача.
Что вы можете сделать
Перед встречей вы можете составить список из:
- Любые симптомы, которые вы заметили и когда они появились, , даже если они кажутся не связанными с инфекцией верхних дыхательных путей.
- Основная медицинская информация, , например, если ваш ребенок родился преждевременно или у него проблемы с сердцем или легкими.
- Подробная информация об уходе за детьми, с учетом других мест, где ваша семья могла быть подвержена респираторным инфекциям.
- Вопросы, которые следует задать врачу. Перечислите свои вопросы от наиболее важных до наименее важных на случай, если время истечет.
Вопросы, которые следует задать своему врачу, могут включать:
- Что, вероятно, вызывает эти симптомы? Есть ли другие возможные причины?
- Какие тесты могут потребоваться?
- Как долго обычно длятся симптомы?
- Какое лечение лучше всего?
- Нужны ли лекарства? Если вы прописываете фирменное лекарство, есть ли альтернатива дженерику?
- Что я могу сделать, чтобы моему ребенку стало лучше?
- Есть ли какие-нибудь брошюры или другие печатные материалы, которые я могу забрать домой? Какие сайты вы рекомендуете?
- В какой степени я должен изолировать своего ребенка, когда он инфицирован?
Не стесняйтесь задавать любые дополнительные вопросы, которые могут у вас возникнуть во время приема.
Чего ожидать от врача
Ваш врач может задать вам ряд вопросов, например:
- Когда вы впервые заметили симптомы?
- Симптомы приходят и уходят или продолжаются?
- Насколько серьезны симптомы?
- Что может улучшить симптомы?
- Что может ухудшить симптомы?
- Кто-нибудь еще в семье болен? Какие у него симптомы?
Ваш врач задаст дополнительные вопросы в зависимости от ваших ответов, симптомов и потребностей.Подготовка и упреждение вопросов помогут вам максимально эффективно проводить время с врачом.
09 января 2021 г.
Респираторно-синцитиальный вирус (РСВ) и метапневмовирусные инфекции человека – Педиатрия
Меры предосторожности при контакте (например, мытье рук, перчатки, изоляция) важны, особенно в больницах.
Пассивная профилактика паливизумабом снижает частоту госпитализаций по поводу RSV у младенцев из группы высокого риска.Это экономически выгодно только для младенцев с высоким риском госпитализации, включая тех, кто
Возраст менее 1 года с гемодинамически значимым врожденным пороком сердца
Менее 1 года с хроническим заболеванием легких недоношенных (срок беременности <32 недель и 0 дней с необходимостью кислородной терапии в течение как минимум 28 дней после рождения)
Родились на сроке <29 недель беременности и младше 1 года на момент начала сезона RSV
Имеют хроническое заболевание легких недоношенных на 2-м году жизни и получали лечение (хроническое лечение кортикостероидами или диуретиками или постоянная потребность в кислородной терапии) в течение 6 месяцев после сезона RSV
Профилактика также может быть рассмотрена для
Младенцы первого года жизни с анатомическими аномалиями легких, нарушающими способность эффективно очищать верхние дыхательные пути
Младенцы с нервно-мышечными расстройствами
Дети <24 месяцев с выраженным иммунодефицитом
Доза паливизумаба составляет 15 мг / кг в / м.Первая доза вводится непосредственно перед обычным началом сезона RSV (начало ноября в Северной Америке). Последующие дозы вводятся с интервалом в 1 месяц в течение сезона RSV (обычно всего 5 доз). (См. Также обновленное заявление Американской академии педиатрии о профилактике паливизумабом детей грудного и раннего возраста, которые подвергаются повышенному риску госпитализации по поводу RSV.)
Несколько материнских, педиатрических и взрослых вакцин против RSV находятся в стадии разработки в клинических испытаниях (1).(См. Также Библиотеку ресурсов по вакцинам PATH.)
Проникновение респираторно-синцитиального вируса и способы его блокирования
Блаунт, Р. Э. мл., Моррис, Дж. А. и Сэвидж, Р. Е. Извлечение цитопатогенного агента из шимпанзе с ринитом. Proc. Soc. Exp. Биол. Med. 92 , 544–549 (1956).
PubMed Статья Google Scholar
Чанок Р., Ройзман Б. и Майерс Р.Выздоровление младенцев с респираторным заболеванием от вируса, связанного с возбудителем ринита шимпанзе (CCA). I. Изоляция, свойства и характеристика. Am. J. Hyg. 66 , 281–290 (1957). В этом исследовании сообщается о первом выделении RSV у младенцев .
CAS PubMed Google Scholar
Чанок, Р. и Финберг, Л. Излечение младенцев с респираторным заболеванием вируса, связанного с возбудителем ринита шимпанзе (CCA).II. Эпидемиологические аспекты инфекции у детей грудного и раннего возраста. Am. J. Hyg. 66 , 291–300 (1957).
CAS PubMed Google Scholar
Глезен, В. П., Табер, Л. Х., Франк, А. Л. и Касел, Дж. А. Риск первичного и повторного заражения респираторно-синцитиальным вирусом. Am. J. Dis. Детский 140 , 543–546 (1986).
CAS PubMed Google Scholar
Shi, T. et al. Глобальные, региональные и национальные оценки бремени острых респираторных инфекций нижних дыхательных путей, вызванных респираторно-синцитиальным вирусом, у детей младшего возраста в 2015 г .: систематический обзор и исследование на основе моделирования. Ланцет 390 , 946–958 (2017).
PubMed PubMed Central Статья Google Scholar
Falsey, A. R., Hennessey, P. A., Formica, M. A., Cox, C. & Walsh, E. E. Инфекция респираторно-синцитиальным вирусом у пожилых людей и взрослых из группы высокого риска. N. Engl. J. Med. 352 , 1749–1759 (2005).
CAS PubMed Статья Google Scholar
van den Hoogen, B.G. et al. Недавно обнаруженный пневмовирус человека, выделенный у детей раннего возраста с заболеваниями дыхательных путей. Нат. Med. 7 , 719–724 (2001). Эта работа описывает первое выделение метапневмовируса человека от детей .
PubMed Статья CAS Google Scholar
Панда, С., Мохакуд, Н. К., Пена, Л., Кумар, С. Метапневмовирус человека: обзор важного респираторного патогена. Внутр. J. Infect. Дис. 25 , 45–52 (2014).
PubMed Статья Google Scholar
Холл, К. Б. Респираторно-синцитиальный вирус: его передача в больничных условиях. Yale J. Biol. Med. 55 , 219–223 (1982).
CAS PubMed PubMed Central Google Scholar
Хаас, Л. Е., Тийсен, С. Ф., ван Элден, Л. и Хемстра, К. А. Метапневмовирус человека у взрослых. Вирусы 5 , 87–110 (2013).
PubMed PubMed Central Статья Google Scholar
Грейсон, С. А., Гриффитс, П. С., Перес, М. К. и Пьедимонте, Г. Обнаружение респираторно-синцитиального вируса, передающегося по воздуху, в педиатрической клинике неотложной помощи. Pediatr. Пульмонол. 52 , 684–688 (2017).
PubMed Статья Google Scholar
Коллинз П. Л. и Грэм Б. С. Вирусные факторы и факторы хозяина в патогенезе респираторно-синцитиального вируса человека. J. Virol. 82 , 2040–2055 (2008).
CAS PubMed Статья Google Scholar
Peebles, R. S. Jr & Graham, B. S. Патогенез респираторно-синцитиальной вирусной инфекции на мышиной модели. Proc. Являюсь. Thorac Soc. 2 , 110–115 (2005).
CAS PubMed PubMed Central Статья Google Scholar
Kim, H. W. et al. Респираторно-синцитиальное вирусное заболевание у младенцев, несмотря на предварительное введение антигенной инактивированной вакцины. Am. J. Epidemiol. 89 , 422–434 (1969).
CAS PubMed Статья Google Scholar
Капикян А. З., Митчелл Р. Х., Чанок Р. М., Шведофф Р. А. и Стюарт С. Е. Эпидемиологическое исследование измененной клинической реактивности к респираторно-синцитиальной (RS) вирусной инфекции у детей, ранее вакцинированных вакциной на основе инактивированного RS-вируса. Am. J. Epidemiol. 89 , 405–421 (1969).
CAS PubMed Статья Google Scholar
Fulginiti, V.A. et al. Иммунизация респираторным вирусом.I. Полевые испытания двух вакцин против инактивированных респираторных вирусов; водная трехвалентная вакцина против вируса парагриппа и вакцина против респираторно-синцитиального вируса, осажденного квасцами. Am. J. Epidemiol. 89 , 435–448 (1969).
CAS PubMed Статья Google Scholar
Чин, Дж., Магоффин, Р. Л., Ширер, Л. А., Шибл, Дж. Х. и Леннетт, Э. Х. Полевая оценка вакцины против респираторно-синцитиального вируса и трехвалентной вакцины против вируса парагриппа в педиатрической популяции. Am. J. Epidemiol. 89 , 449–463 (1969).
CAS PubMed Статья Google Scholar
Принс, Г. А., Кертис, С. Дж., Йим, К. К. и Портер, Д. Д. Усиленное вакциной респираторно-синцитиальное вирусное заболевание у хлопковых крыс после иммунизации партией 100 или недавно приготовленной контрольной вакциной. J. Gen. Virol. 82 , 2881–2888 (2001).
CAS PubMed Статья Google Scholar
Polack, F. P. et al. Роль иммунных комплексов в усилении респираторно-синцитиального вирусного заболевания. J. Exp. Med. 196 , 859–865 (2002). Эта рукопись демонстрирует, что болезнь, усиленная вакциной, опосредуется иммунными комплексами .
CAS PubMed PubMed Central Статья Google Scholar
Хомаира, Н., Роулинсон, В., Снеллинг, Т. Л. и Джаффе, А. Эффективность паливизумаба в предотвращении госпитализации по поводу РСВ у детей высокого риска: реальная перспектива. Внутр. J. Pediatr. 2014 , 571609 (2014).
PubMed PubMed Central Статья Google Scholar
Фирнс Р. и Коллинз П. Л. Роль антитерминационного белка транскрипции M2-1 респираторно-синцитиального вируса в последовательной транскрипции. J. Virol. 73 , 5852–5864 (1999).
CAS PubMed PubMed Central Google Scholar
Коллинз, П. Л., Хилл, М. Г., Кристина, Дж. И Гросфельд, Х. Фактор удлинения транскрипции респираторно-синцитиального вируса, несегментированного РНК-вируса с отрицательной цепью. Proc. Natl Acad. Sci. USA 93 , 81–85 (1996).
CAS PubMed Статья Google Scholar
Bermingham, A. & Collins, P. L. Белок M2-2 респираторно-синцитиального вируса человека является регуляторным фактором, участвующим в балансе между репликацией РНК и транскрипцией. Proc. Natl Acad. Sci. США 96 , 11259–11264 (1999).
CAS PubMed Статья Google Scholar
Bitko, V. et al. Неструктурные белки респираторно-синцитиального вируса подавляют преждевременный апоптоз с помощью NF-κB-зависимого, интерферон-независимого механизма и способствуют росту вируса. J. Virol. 81 , 1786–1795 (2007).
CAS PubMed Статья Google Scholar
Спанн, К. М., Тран, К. и Коллинз, П. Л. Влияние неструктурных белков NS1 и NS2 респираторно-синцитиального вируса человека на фактор регуляции интерферона 3, NF-κB и провоспалительные цитокины. J. Virol. 79 , 5353–5362 (2005).
CAS PubMed PubMed Central Статья Google Scholar
Gan, S. W. et al. Небольшой гидрофобный белок респираторно-синцитиального вируса человека образует пентамерные ионные каналы. J. Biol. Chem. 287 , 24671–24689 (2012).
CAS PubMed PubMed Central Статья Google Scholar
Fuentes, S., Tran, K. C., Luthra, P., Teng, M. N. & He, B. Функция малого гидрофобного белка респираторно-синцитиального вируса. J. Virol. 81 , 8361–8366 (2007).
CAS PubMed PubMed Central Статья Google Scholar
Baviskar, P. S., Hotard, A. L., Moore, M. L. и Oomens, A. G. Слитый белок респираторно-синцитиального вируса нацеливается на периметр телец включения и способствует образованию филаментов за счет цитоплазматического хвостового механизма. J. Virol. 87 , 10730–10741 (2013).
CAS PubMed PubMed Central Статья Google Scholar
Shaikh, F. Y. et al. Важный остаток фенилаланина в цитоплазматическом хвосте слитого белка респираторно-синцитиального вируса опосредует сборку внутренних вирусных белков в вирусные филаменты и частицы. мБио 3 , e00270-11 (2012).
CAS PubMed PubMed Central Статья Google Scholar
Oomens, A. G., Bevis, K. P. & Wertz, G. W. Цитоплазматический хвост белка F респираторно-синцитиального вируса человека играет критическую роль в клеточной локализации белка F и продукции инфекционного потомства. J. Virol. 80 , 10465–10477 (2006).
CAS PubMed PubMed Central Статья Google Scholar
Марти А., Минджер Дж., Миллс Дж., Шилдс Б. и Гильдиал Р. Ассоциация матричного белка респираторно-синцитиального вируса с клеточной мембраной инфицированных клеток. Arch. Virol. 149 , 199–210 (2004).
CAS PubMed Статья Google Scholar
Kiss, G. et al. Структурный анализ респираторно-синцитиального вируса показывает положение M2-1 между матриксным белком и рибонуклеопротеидным комплексом. J. Virol. 88 , 7602–7617 (2014).
PubMed PubMed Central Статья CAS Google Scholar
Tawar, R.G. et al. Кристаллическая структура нуклеокапсидоподобного комплекса нуклеопротеин-РНК респираторно-синцитиального вируса. Наука 326 , 1279–1283 (2009).
CAS PubMed Статья Google Scholar
Rixon, H. W. et al. Небольшой гидрофобный (SH) белок накапливается в структурах липидного рафта комплекса Гольджи во время респираторно-синцитиальной вирусной инфекции. J. Gen. Virol. 85 , 1153–1165 (2004).
CAS PubMed Статья Google Scholar
Букреев А., Уайтхед С.С., Мерфи, Б.Р. и Коллинз, П.Л. Рекомбинантный респираторно-синцитиальный вирус, из которого был удален весь ген SH, эффективно растет в культуре клеток и проявляет сайт-специфическое ослабление в дыхательных путях. мыши. J. Virol. 71 , 8973–8982 (1997).
CAS PubMed PubMed Central Google Scholar
Левин, С., Клайбер-Франко, Р. и Парадизо, П. Р. Демонстрация того, что гликопротеин G является белком прикрепления респираторно-синцитиального вируса. J. Gen. Virol. 68 , 2521–2524 (1987).
CAS PubMed Статья Google Scholar
Хендрикс Д. А., Барадаран К., Макинтош К. и Паттерсон Дж. Л. Появление растворимой формы G-белка респираторно-синцитиального вируса в жидкостях инфицированных клеток. J. Gen. Virol. 68 , 1705–1714 (1987).
CAS PubMed Статья Google Scholar
Wertz, G. W. et al. Нуклеотидная последовательность гена G-белка респираторно-синцитиального вируса человека обнаруживает необычный тип вирусного мембранного белка. Proc. Natl Acad. Sci. США 82 , 4075–4079 (1985).
CAS PubMed Статья Google Scholar
Коллинз П. Л. и Моттет Г. Олигомеризация и посттрансляционный процессинг гликопротеина G респираторно-синцитиального вируса человека: измененное О-гликозилирование в присутствии брефельдина А. J. Gen. Virol. 73 , 849–863 (1992).
CAS PubMed Статья Google Scholar
Сатаке, М., Колиган, Дж. Э., Эланго, Н., Норрби, Э. и Венкатесан, С. Гликопротеин оболочки респираторно-синцитиального вируса (G) имеет новую структуру. Nucleic Acids Res. 13 , 7795–7812 (1985).
CAS PubMed PubMed Central Статья Google Scholar
Garcia-Beato, R. et al. Влияние клетки-хозяина на гликозилирование и антигенность гликопротеина G респираторно-синцитиального вируса человека. Вирусология 221 , 301–309 (1996).
CAS PubMed Статья Google Scholar
Kwilas, S. et al. Респираторно-синцитиальный вирус, выращенный в клетках Vero, содержит усеченный белок прикрепления, который изменяет его инфекционность и зависимость от гликозаминогликанов. J. Virol. 83 , 10710–10718 (2009).
CAS PubMed PubMed Central Статья Google Scholar
Робертс, С. Р., Лихтенштейн, Д., Болл, Л. А. и Вертц, Г. В. Ассоциированные с мембраной и секретируемые формы гликопротеина G прикрепления респираторно-синцитиального вируса синтезируются из альтернативных инициирующих кодонов. J. Virol. 68 , 4538–4546 (1994).
CAS PubMed PubMed Central Google Scholar
Хендрикс Д. А., Макинтош К. и Паттерсон Дж. Л. Дальнейшая характеристика растворимой формы гликопротеина G респираторно-синцитиального вируса. J. Virol. 62 , 2228–2233 (1988).
CAS PubMed PubMed Central Google Scholar
Букреев А., Янг Л. и Коллинз П. Л. Секретируемый G-белок респираторно-синцитиального вируса человека противодействует опосредованному антителами ограничению репликации с участием макрофагов и комплемента. J. Virol. 86 , 10880–10884 (2012).
CAS PubMed PubMed Central Статья Google Scholar
Букреев А. и др. Секретируемая форма гликопротеина G респираторно-синцитиального вируса помогает вирусу избежать опосредованного антителами ограничения репликации, действуя как ловушка для антигена и воздействуя на лейкоциты, несущие рецептор Fc. J. Virol. 82 , 12191–12204 (2008).
CAS PubMed PubMed Central Статья Google Scholar
Горман, Дж. Дж., Фергюсон, Б. Л., Спилман, Д. и Миллс, Дж.Определение расположения дисульфидных связей в белке прикрепления (G) респираторно-синцитиального вируса человека с помощью масс-спектрометрии с времяпролетной лазерной десорбцией / ионизацией с использованием матрицы. Protein Sci. 6 , 1308–1315 (1997).
CAS PubMed PubMed Central Статья Google Scholar
Langedijk, J. P., Schaaper, W. M., Meloen, R.H. & van Oirschot, J. T. Предложили трехмерную модель для белка присоединения G респираторно-синцитиального вируса. J. Gen. Virol. 77 , 1249–1257 (1996).
CAS PubMed Статья Google Scholar
Doreleijers, J. F. et al. Структура раствора иммунодоминантной области белка G респираторно-синцитиального вируса крупного рогатого скота. Биохимия 35 , 14684–14688 (1996). Это исследование определяет первую трехмерную структуру цистиновой петли RSV G .
CAS PubMed Статья Google Scholar
Sugawara, M. et al. Исследования взаимосвязи структура-антигенность центральной консервативной области белка G респираторно-синцитиального вируса человека. J. Pept. Res. 60 , 271–282 (2002).
CAS PubMed Статья Google Scholar
Langedijk, JP, de Groot, BL, Berendsen, HJ & van Oirschot, JT Структурная гомология центральной консервативной области белка прикрепления G респираторно-синцитиального вируса с четвертым субдоменом фактора некроза опухоли 55 кДа рецептор. Вирусология 243 , 293–302 (1998).
CAS PubMed Статья Google Scholar
Jones, H.G. et al. Структурная основа распознавания центральной консервативной области G RSV путем нейтрализации человеческих антител. PLOS Pathog. 14 , e1006935 (2018).
PubMed PubMed Central Статья CAS Google Scholar
Федечкин, С.О., Джордж, Н.Л., Вольф, Дж. Т., Каувар, Л. М. и Дюбуа, Р. М. Структуры антигена G респираторно-синцитиального вируса, связанного с широко нейтрализующими антителами. Sci. Иммунол. 3 , eaar3534 (2018).
PubMed PubMed Central Статья Google Scholar
Пангести К. Н., Абд Эль Гани М., Уолш М. Г., Кессон А. М. и Хилл-Коуторн Г. А. Молекулярная эпидемиология респираторно-синцитиального вируса. Rev. Med. Virol. 28 , e1968 (2018).
Артикул Google Scholar
Муфсон М.А., Орвелл К., Рафнар Б. и Норрби Е. Два различных подтипа респираторно-синцитиального вируса человека. J. Gen. Virol. 66 , 2111–2124 (1985).
CAS PubMed Статья Google Scholar
Anderson, L.J. et al.Антигенная характеристика штаммов респираторно-синцитиального вируса с помощью моноклональных антител. J. Infect. Дис. 151 , 626–633 (1985).
CAS PubMed Статья Google Scholar
Hall, C. B. et al. Распространенность респираторно-синцитиального вируса группы A и B в течение 15 лет: связанные эпидемиологические и клинические характеристики у детей, находящихся в стационаре и амбулаторно. J. Infect. Дис. 162 , 1283–1290 (1990).
CAS PubMed Статья Google Scholar
Trento, A. et al. Основные изменения в G-белке изолятов респираторно-синцитиального вируса человека, вызванные дупликацией 60 нуклеотидов. J. Gen. Virol. 84 , 3115–3120 (2003).
CAS PubMed Статья Google Scholar
Trento, A. et al. Естественная история респираторно-синцитиального вируса человека, выведенная из филогенетического анализа прикрепленного (G) гликопротеина с дупликацией 60 нуклеотидов. J. Virol. 80 , 975–984 (2006).
CAS PubMed PubMed Central Статья Google Scholar
Trento, A. et al. Десять лет глобальной эволюции генотипа BA респираторно-синцитиального вируса человека с 60-нуклеотидной дупликацией в гене G-белка. J. Virol. 84 , 7500–7512 (2010).
CAS PubMed PubMed Central Статья Google Scholar
Eshaghi, A. et al. Генетическая изменчивость штаммов респираторно-синцитиального вируса человека, циркулирующих в Онтарио: новый генотип с дупликацией гена G. PLOS ONE 7 , e32807 (2012).
CAS PubMed PubMed Central Статья Google Scholar
Duvvuri, V. R. et al. Генетическое разнообразие и эволюционное понимание генотипа респираторно-синцитиального вируса A ON1: глобальная и локальная динамика передачи. Sci. Отчет 5 , 14268 (2015).
CAS PubMed PubMed Central Статья Google Scholar
Hirano, E. et al. Молекулярная эволюция гена гликопротеина (G) прикрепления респираторно-синцитиального вируса человека нового генотипа ON1 и предка NA1. Заражение. Genet. Evol. 28 , 183–191 (2014).
CAS PubMed Статья Google Scholar
Hotard, A. L., Laikhter, E., Brooks, K., Hartert, T. V. & Moore, M. L. Функциональный анализ дупликации 60 нуклеотидов в гликопротеине прикрепления штамма Buenos Aires респираторно-синцитиального вируса. J. Virol. 89 , 8258–8266 (2015).
CAS PubMed PubMed Central Статья Google Scholar
Лейрат, К., Паесен, Г.С., Чарльстон, Дж., Реннер, М. и Граймс, Дж. М. Структурное понимание эктодомена гликопротеина метапневмовируса человека. J. Virol. 88 , 11611–11616 (2014).
PubMed PubMed Central Статья CAS Google Scholar
Yin, H. S., Wen, X., Paterson, R. G., Lamb, R. A. & Jardetzky, T. S. Структура белка 5 F вируса парагриппа в его метастабильной префузионной конформации. Nature 439 , 38–44 (2006).
CAS PubMed Статья Google Scholar
Yin, H. S., Paterson, R. G., Wen, X., Lamb, R. A. & Jardetzky, T. S. Структура нерасщепленного эктодомена слитого белка парамиксовируса (hPIV3). Proc. Natl Acad. Sci. США 102 , 9288–9293 (2005).
CAS PubMed Статья Google Scholar
Collins, P. L., Huang, Y. T. & Wertz, G. W. Нуклеотидная последовательность гена, кодирующего слитый (F) гликопротеин респираторно-синцитиального вируса человека. Proc. Natl Acad. Sci. США 81 , 7683–7687 (1984).
CAS PubMed Статья Google Scholar
Циммер Г., Будз Л. и Херрлер Г. Протеолитическая активация слитого белка респираторно-синцитиального вируса. Расщепление по двум консенсусным последовательностям фурина. J. Biol. Chem. 276 , 31642–31650 (2001).
CAS PubMed Статья Google Scholar
Gonzalez-Reyes, L. et al. Расщепление слитого белка респираторно-синцитиального вируса человека в двух разных сайтах необходимо для активации слияния мембран. Proc. Natl Acad. Sci. США 98 , 9859–9864 (2001).
CAS PubMed Статья Google Scholar
Bolt, G., Pedersen, L.O. & Birkeslund, H.H. Для его поверхностной экспрессии требуется расщепление слитого белка респираторно-синцитиального вируса: роль фурина. Virus Res. 68 , 25–33 (2000).
CAS PubMed Статья Google Scholar
Коллинз П. Л. и Моттет Г. Посттрансляционный процессинг и олигомеризация слитого гликопротеина респираторно-синцитиального вируса человека. J. Gen. Virol. 72 , 3095–3101 (1991).
CAS PubMed Статья Google Scholar
Day, N. D. et al. Вклад остатков цистеина во внеклеточном домене белка F респираторно-синцитиального вируса человека в его функцию. Virol. J. 3 , 34 (2006).
PubMed PubMed Central Статья CAS Google Scholar
Gilman, M. S. et al. Характеристика префузионного антитела, которое распознает четвертичный, зависимый от расщепления эпитоп на слитом гликопротеине RSV. PLOS Pathog. 11 , e1005035 (2015).
PubMed PubMed Central Статья CAS Google Scholar
Krarup, A. et al. Высокостабильная вакцина перед слиянием RSV F, полученная в результате структурного анализа механизма слияния. Нат.Commun. 6 , 8143 (2015).
PubMed PubMed Central Статья Google Scholar
McLellan, J. S. et al. Структура тримерного гликопротеина слияния RSV, связанного с нейтрализующим антителом, специфичным для предварительного слияния. Наука 340 , 1113–1117 (2013). Эта работа обеспечивает первую трехмерную структуру конформации RSV F перед слиянием и определяет главный антигенный сайт, распознаваемый специфическими антителами до слияния.
CAS PubMed PubMed Central Статья Google Scholar
Liljeroos, L., Krzyzaniak, M. A., Helenius, A. & Butcher, S. J. Архитектура респираторно-синцитиального вируса, выявленная с помощью электронной криотомографии. Proc. Natl Acad. Sci. США 110 , 11133–11138 (2013). Эта рукопись раскрывает организацию и морфологию вирионов RSV с помощью криоэлектронной томографии .
CAS PubMed Статья Google Scholar
Килликелли, А. М., Канекиё, М. и Грэхэм, Б. С. Предварительное слияние F отсутствует на поверхности инактивированного формалином респираторно-синцитиального вируса. Sci. Отчет 6 , 34108 (2016).
CAS PubMed PubMed Central Статья Google Scholar
Kim, Y.H. et al. Захват и визуализация промежуточного соединения прешпильчатого слияния парамиксовируса PIV5. Proc. Natl Acad. Sci. США 108 , 20992–20997 (2011).
CAS PubMed Статья Google Scholar
Чжао, X., Сингх, М., Малашкевич, В. Н. и Ким, П. С. Структурная характеристика ядра слитого белка респираторно-синцитиального вируса человека. Proc. Natl Acad. Sci. США 97 , 14172–14177 (2000).
CAS PubMed Статья Google Scholar
Маклеллан, Дж.S., Yang, Y., Graham, B. S. & Kwong, P. D. Структура гликопротеина слияния респираторно-синцитиального вируса в постфузионной конформации показывает сохранение нейтрализующих эпитопов. J. Virol. 85 , 7788–7796 (2011).
CAS PubMed PubMed Central Статья Google Scholar
Swanson, K. A. et al. Структурная основа иммунизации постфузионным гликопротеином F слияния респираторно-синцитиального вируса (RSV F) для получения высоких титров нейтрализующих антител. Proc. Natl Acad. Sci. США 108 , 9619–9624 (2011).
CAS PubMed Статья Google Scholar
Джонсон, Дж. Э., Гонсалес, Р. А., Олсон, С. Дж., Райт, П. Ф. и Грэм, Б. С. Гистопатология фатальной нелеченой респираторно-синцитиальной вирусной инфекции человека. Мод. Патол. 20 , 108–119 (2007).
CAS PubMed Статья Google Scholar
Xu, L. et al. Смертельный случай, связанный с инфекцией респираторно-синцитиального вируса у маленького ребенка. BMC Infect. Дис. 18 , 217 (2018).
PubMed PubMed Central Статья Google Scholar
Pitkaranta, A., Virolainen, A., Jero, J., Arruda, E. & Hayden, FG Выявление риновирусов, респираторно-синцитиальных вирусов и коронавирусных инфекций при остром среднем отите с помощью полимеразной цепной реакции с обратной транскриптазой . Педиатрия 102 , 291–295 (1998).
CAS PubMed Статья Google Scholar
Rohwedder, A. et al. Обнаружение РНК респираторно-синцитиального вируса в крови новорожденных методом полимеразной цепной реакции. J. Med. Virol. 54 , 320–327 (1998).
CAS PubMed Статья Google Scholar
Эскрибано-Ромеро, Э., Rawling, J., Garcia-Barreno, B. & Melero, J. A. Растворимая форма белка прикрепления респираторно-синцитиального вируса человека отличается от мембраносвязанной формы своим олигомерным состоянием, но все же способна связываться с протеогликанами клеточной поверхности. J. Virol. 78 , 3524–3532 (2004).
CAS PubMed PubMed Central Статья Google Scholar
Krusat, T. & Streckert, H.J. Гепарин-зависимое прикрепление респираторно-синцитиального вируса (RSV) к клеткам-хозяевам. Arch. Virol. 142 , 1247–1254 (1997).
CAS PubMed Статья Google Scholar
Фельдман С. А., Хендри Р. М. и Билер Дж. А. Идентификация линейного гепарин-связывающего домена для гликопротеина прикрепления респираторно-синцитиального вируса человека G. J. Virol. 73 , 6610–6617 (1999).
CAS PubMed PubMed Central Google Scholar
Халлак, Л. К., Спиллманн, Д., Коллинз, П. Л. и Пиплс, М. Е. Требования сульфатирования гликозаминогликанов при респираторно-синцитиальной вирусной инфекции. J. Virol. 74 , 10508–10513 (2000).
CAS PubMed PubMed Central Статья Google Scholar
Мартинес И. и Мелеро Дж. А. Связывание респираторно-синцитиального вируса человека с клетками: влияние протеогликанов сульфатированной клеточной поверхности. J. Gen. Virol. 81 , 2715–2722 (2000).
CAS PubMed Статья Google Scholar
Халлак, Л. К., Коллинз, П. Л., Кнудсон, В. и Пиплс, М. Е. Гликозаминогликаны, содержащие идуроновую кислоту, на клетках-мишенях необходимы для эффективной респираторно-синцитиальной вирусной инфекции. Вирусология 271 , 264–275 (2000).
CAS PubMed Статья Google Scholar
Чиркова Т. и др. CX3CR1 является важной поверхностной молекулой для респираторно-синцитиальной вирусной инфекции в эпителиальных клетках дыхательных путей человека. J. Gen. Virol. 96 , 2543–2556 (2015).
CAS PubMed PubMed Central Статья Google Scholar
Zhang, L. et al. Инфекция реснитчатых клеток вирусом парагриппа человека типа 3 на модели эпителия дыхательных путей человека in vitro. J. Virol. 79 , 1113–1124 (2005).
CAS PubMed PubMed Central Статья Google Scholar
Zhang, L., Peeples, M. E., Boucher, R. C., Collins, P. L. & Pickles, R. J. Респираторно-синцитиальная вирусная инфекция эпителиальных клеток дыхательных путей человека поляризована, специфична для мерцательных клеток и не имеет очевидной цитопатологии. J. Virol. 76 , 5654–5666 (2002).
CAS PubMed PubMed Central Статья Google Scholar
Johnson, S. M. et al. Респираторно-синцитиальный вирус использует CX3CR1 в качестве рецептора на первичных культурах эпителия дыхательных путей человека. PLOS Pathog. 11 , e1005318 (2015).
PubMed PubMed Central Статья CAS Google Scholar
Tripp, R.A. et al. Мимикрия хемокина CX3C гликопротеином G респираторно-синцитиального вируса. Нат. Иммунол. 2 , 732–738 (2001). Это исследование идентифицирует CX 3 мотив C в RSV G и демонстрирует, что CX 3 CR1 облегчает ввод RSV .
CAS PubMed Статья Google Scholar
Bazan, J. F. et al. Новый класс мембраносвязанных хемокинов с мотивом CX3C. Nature 385 , 640–644 (1997).
CAS PubMed Статья PubMed Central Google Scholar
Jeong, K. I. et al. CX3CR1 экспрессируется в дифференцированных клетках ресничных дыхательных путей человека и совместно с респираторно-синцитиальным вирусом локализуется на ресничках G-белком. PLOS ONE 10 , e0130517 (2015).
PubMed PubMed Central Статья CAS Google Scholar
Karron, R.A. et al. Белки SH и G респираторно-синцитиального вируса (RSV) не являются существенными для вирусной репликации in vitro: клиническая оценка и молекулярная характеристика пересаженного холодом аттенуированного мутанта подгруппы B RSV. Proc. Natl Acad. Sci. США 94 , 13961–13966 (1997). Эта работа демонстрирует, что инфекционный RSV требует только белка F на своей поверхности .
CAS PubMed Статья Google Scholar
Techaarpornkul, S., Barretto, N. & Peeples, M. E. Функциональный анализ рекомбинантных мутантов с делецией респираторно-синцитиального вируса, у которых отсутствует небольшой гидрофобный ген и / или ген гликопротеина присоединения. J. Virol. 75 , 6825–6834 (2001).
CAS PubMed PubMed Central Статья Google Scholar
Feldman, S. A., Audet, S. & Beeler, J. A. Слитый гликопротеин респираторно-синцитиального вируса человека облегчает прикрепление вируса и инфекционность посредством взаимодействия с клеточным гепарансульфатом. J. Virol. 74 , 6442–6447 (2000).
CAS PubMed PubMed Central Статья Google Scholar
Behera, A. K. et al. Блокирование молекулы-1 межклеточной адгезии на эпителиальных клетках человека снижает инфекцию респираторно-синцитиального вируса. Biochem. Биофиз. Res. Commun. 280 , 188–195 (2001).
CAS PubMed Статья Google Scholar
Currier, M. G. et al. EGFR взаимодействует со слитым белком штамма респираторно-синцитиального вируса 2–20 и опосредует инфекцию и экспрессию муцина. PLOS Pathog. 12 , e1005622 (2016).
PubMed PubMed Central Статья CAS Google Scholar
Tayyari, F. et al. Идентификация нуклеолина как клеточного рецептора респираторно-синцитиального вируса человека. Нат. Med. 17 , 1132–1135 (2011). Эта рукопись идентифицирует нуклеолин как фактор клетки-хозяина, который взаимодействует с белком F и способствует проникновению RSV .
CAS PubMed Статья Google Scholar
Бозе, С., Басу, М. и Банерджи, А. К. Роль нуклеолина в инфицировании эпителиальных клеток легких человека вирусом парагриппа 3 типа. J. Virol. 78 , 8146–8158 (2004).
CAS PubMed PubMed Central Статья Google Scholar
Su, P. Y. et al. Нуклеолин клеточной поверхности способствует связыванию энтеровируса 71 и инфицированию. J. Virol. 89 , 4527–4538 (2015).
CAS PubMed PubMed Central Статья Google Scholar
Xiao, X., Feng, Y., Zhu, Z. & Dimitrov, D. S. Идентификация предполагаемого фактора проникновения вируса крымско-конголезской геморрагической лихорадки. Biochem. Биофиз. Res. Commun. 411 , 253–258 (2011).
CAS PubMed PubMed Central Статья Google Scholar
Qiu, J. & Brown, K. E. A. Ядерный челночный белок массой 110 кДа, нуклеолин, специфически связывается с капсидом аденоассоциированного вируса типа 2 (AAV-2). Вирусология 257 , 373–382 (1999).
CAS PubMed Статья Google Scholar
Callebaut, C. et al. Идентификация белков, связывающих петлю V3, как потенциальных рецепторов, участвующих в связывании частиц ВИЧ с клетками CD4 + . J. Biol. Chem. 273 , 21988–21997 (1998).
CAS PubMed Статья Google Scholar
Сринивасакумар, Н., Огра, П. Л. и Фланаган, Т. Д. Характеристики слияния респираторно-синцитиального вируса с клетками HEp-2, измеренные с помощью анализа ослабления флуоресценции R18. J. Virol. 65 , 4063–4069 (1991).
CAS PubMed PubMed Central Google Scholar
Kahn, J. S., Schnell, M. J., Buonocore, L. & Rose, J. K. Рекомбинантный вирус везикулярного стоматита, экспрессирующий гликопротеины респираторно-синцитиального вируса (RSV): слитый белок RSV может опосредовать инфекцию и слияние клеток. Вирусология 254 , 81–91 (1999).
CAS PubMed Статья Google Scholar
Уайт, Дж. М. и Уиттакер, Г. Р. Слияние оболочечных вирусов в эндосомах. Трафик 17 , 593–614 (2016).
CAS PubMed PubMed Central Статья Google Scholar
San-Juan-Vergara, H. et al.Богатые холестерином микродомены как стыковочные платформы для респираторно-синцитиального вируса в нормальных эпителиальных клетках бронхов человека. J. Virol. 86 , 1832–1843 (2012).
CAS PubMed PubMed Central Статья Google Scholar
Krzyzaniak, M. A., Zumstein, M. T., Gerez, J. A., Picotti, P. & Helenius, A. Попадание респираторно-синцитиального вируса в клетки-хозяева включает макропиноцитоз с последующей протеолитической активацией белка F. PLOS Pathog. 9 , e1003309 (2013).
CAS PubMed PubMed Central Статья Google Scholar
Schlender, J., Zimmer, G., Herrler, G. & Conzelmann, K. K. Субъединица F2 слитого белка респираторно-синцитиального вируса (RSV), а не белок присоединения G, определяет специфичность инфекции RSV. J. Virol. 77 , 4609–4616 (2003).
CAS PubMed PubMed Central Статья Google Scholar
Yuan, P. et al. Структурные исследования тетрамера гемагглютинин-нейраминидазы вируса парагриппа 5 в комплексе с его рецептором сиалиллактозой. Структура 13 , 803–815 (2005).
CAS PubMed Статья Google Scholar
Креннелл, С., Такимото, Т., Портнер, А. и Тейлор, Г. Кристаллическая структура многофункциональной парамиксовирусной гемагглютинин-нейраминидазы. Нат. Struct.Биол. 7 , 1068–1074 (2000).
CAS PubMed Статья Google Scholar
Bose, S., Jardetzky, T. S. & Lamb, R. A. Время решает все: точно настроенные молекулярные машины организуют проникновение парамиксовирусов. Вирусология 479–480 , 518–531 (2015).
PubMed Статья CAS Google Scholar
Юнус, А.S. et al. Повышенная температура вызывает образование шестиспирального пучка белка F респираторно-синцитиального вируса человека. Вирусология 396 , 226–237 (2010).
CAS PubMed Статья Google Scholar
Фирнс Р. и Деваль Дж. Новые противовирусные подходы к респираторно-синцитиальному вирусу и другим мононегавирусам: ингибирование РНК-полимеразы. Antiviral Res. 134 , 63–76 (2016).
CAS PubMed Статья Google Scholar
Falsey, A. R. & Walsh, E. E. Связь сывороточных антител с риском респираторно-синцитиальной вирусной инфекции у пожилых людей. J. Infect. Дис. 177 , 463–466 (1998).
CAS PubMed Статья Google Scholar
Холл, К. Б., Уолш, Э. Э., Лонг, К. Э. и Шнабель, К.C. Иммунитет к респираторно-синцитиальному вирусу и частота повторного заражения. J. Infect. Дис. 163 , 693–698 (1991).
CAS PubMed Статья Google Scholar
Американская педиатрическая академия. Иммуноглобулин респираторно-синцитиального вируса для внутривенного введения: показания к применению. Комитет по инфекционным болезням, Комитет по плодам и новорожденным. Педиатрия 99 , 645–650 (1997).
Артикул Google Scholar
Исследовательская группа IMpact-RSV. Паливизумаб, гуманизированное моноклональное антитело к респираторно-синцитиальному вирусу, снижает количество госпитализаций в связи с инфекцией респираторно-синцитиального вируса у младенцев из группы высокого риска. Педиатрия 102 , 531–537 (1998).
Артикул Google Scholar
Beeler, J. A. & Coelingh, K.V. Нейтрализация эпитопов F-гликопротеина респираторно-синцитиального вируса – влияние мутации на функцию слияния. J. Virol. 63 , 2941–2950 (1989).
CAS PubMed PubMed Central Google Scholar
Kwakkenbos, M. J. et al. Создание стабильных моноклональных антител, продуцирующих B-клеточные рецепторы B-клеток памяти человека, путем генетического программирования. Нат. Med. 16 , 123–128 (2010). В этом исследовании сообщается о выделении и характеристике первых F-специфичных моноклональных антител перед слиянием, хотя их специфичность в то время не была известна, .
CAS PubMed Статья Google Scholar
Goodwin, E. et al. Младенцы, инфицированные респираторно-синцитиальным вирусом, вырабатывают мощные нейтрализующие антитела, в которых отсутствует соматическая гипермутация. Иммунитет 48 , 339–349 (2018).
CAS PubMed PubMed Central Статья Google Scholar
Gilman, M. S. et al. Быстрое профилирование репертуаров антител к RSV из В-клеток памяти естественно инфицированных взрослых доноров. Sci. Иммунол . 1 (2016).
Collarini, E.J. et al. Мощные высокоаффинные антитела для лечения и профилактики респираторно-синцитиального вируса, полученные из В-клеток инфицированных пациентов. J. Immunol. 183 , 6338–6345 (2009).
CAS PubMed Статья Google Scholar
Mousa, J. J., Kose, N., Matta, P., Gilchuk, P. & Crowe, J. E. Jr. Новый нейтрализующий эпитоп, специфичный для конформации перед слиянием, на гибридном белке респираторно-синцитиального вируса. Нат. Microbiol. 2 , 16271 (2017).
CAS PubMed PubMed Central Статья Google Scholar
Corti, D. et al. Перекрестная нейтрализация четырех парамиксовирусов человеческим моноклональным антителом. Природа 501 , 439–443 (2013).
CAS PubMed Статья Google Scholar
Zhu, Q. et al. Высокоэффективное антитело с увеличенным периодом полужизни в качестве потенциального заменителя вакцины против RSV для всех младенцев. Sci. Transl Med. 9 , eaaj1928 (2017).
PubMed Статья Google Scholar
Национальная медицинская библиотека США. ClinicalTrials.gov https://clinicaltrials.gov/ct2/show/NCT02878330 (2018).
Национальная медицинская библиотека США. ClinicalTrials.gov https://clinicaltrials.gov/ct2/show/NCT02325791 (2018).
Костелло, Х. М., Рэй, В. К., Чайватпонгсакорн, С. и Пиплс, М. Е. Нацеливание на РСВ с помощью вакцин и низкомолекулярных препаратов. Заражение. Disord. Drug Targets 12 , 110–128 (2012).
CAS PubMed PubMed Central Статья Google Scholar
Хейлен, Э., Нейтс, Дж. И Джохманс, Д. Лекарственные препараты-кандидаты и модельные системы в открытии противовирусных препаратов для респираторно-синцитиального вируса. Biochem. Pharmacol. 127 , 1–12 (2017).
CAS PubMed Статья Google Scholar
Cianci, C. et al. Нацеливание на связывающий карман в тримере шпильки: низкомолекулярное ингибирование слияния вирусов. Proc. Natl Acad. Sci. США 101 , 15046–15051 (2004).
CAS PubMed Статья Google Scholar
Roymans, D. et al. Связывание мощного низкомолекулярного ингибитора образования пучка из шести спиралей требует взаимодействия с обоими гептадными повторами слитого белка RSV. Proc. Natl Acad. Sci. США 107 , 308–313 (2010).
CAS PubMed Статья Google Scholar
Yan, D. et al. Механизм перекрестной резистентности респираторно-синцитиального вируса против структурно разнообразных ингибиторов проникновения. Proc. Natl Acad. Sci. США 111 , E3441 – E3449 (2014).
CAS PubMed Статья Google Scholar
Battles, M. B. et al. Молекулярный механизм ингибиторов слияния респираторно-синцитиального вируса. Нат. Chem. Биол. 12 , 87–93 (2016). Эта работа описывает сайт связывания и механизм действия для ингибиторов слияния малых молекул .
CAS PubMed Статья Google Scholar
Samuel, D. et al. GS-5806 ингибирует пре- и постфузионные конформационные изменения слитого белка респираторно-синцитиального вируса. Антимикробный. Агенты Chemother. 59 , 7109–7112 (2015).
CAS PubMed PubMed Central Статья Google Scholar
Де Винченцо, Дж.P. et al. Оральная активность GS-5806 в исследовании заражения респираторно-синцитиальным вирусом. N. Engl. J. Med. 371 , 711–722 (2014).
PubMed Статья CAS Google Scholar
Stevens, M. et al. Противовирусная активность перорального JNJ-53718678 у здоровых взрослых добровольцев, зараженных респираторно-синцитиальным вирусом: плацебо-контролируемое исследование. J. Infect. Дис. 218 , 748–756 (2018).
PubMed Статья Google Scholar
Mazur, N. I. et al. Пейзаж вакцин против респираторно-синцитиального вируса: уроки с кладбища и многообещающие кандидаты. Lancet Infect. Дис. 18 , e295 – e311 (2018).
PubMed Статья Google Scholar
Грэм Б.С. Разработка вакцины против респираторно-синцитиального вируса. Curr. Opin. Virol. 23 , 107–112 (2017).
CAS PubMed PubMed Central Статья Google Scholar
Magro, M. et al. Нейтрализующие антитела против преактивной формы слитого белка респираторно-синцитиального вируса открывают уникальные возможности для клинического вмешательства. Proc. Natl Acad. Sci. США 109 , 3089–3094 (2012). Это исследование является первым доказательством существования F-специфичных антител перед слиянием и их доминирующего вклада в нейтрализующую RSV активность сывороток человека .
CAS PubMed Статья Google Scholar
Ngwuta, J. O. et al. F-специфические антитела перед слиянием определяют степень нейтрализующей активности RSV в сыворотке крови человека. Sci. Transl Med. 7 , 309ра162 (2015).
PubMed PubMed Central Статья CAS Google Scholar
McLellan, J. S. et al. Конструкция на основе структуры гибридной гликопротеиновой вакцины против респираторно-синцитиального вируса. Наука 342 , 592–598 (2013). В этой рукописи сообщается о первом структурном дизайне вакцинного антигена F до слияния и демонстрируется его превосходная иммуногенность по сравнению с антигенами F после слияния .
CAS PubMed PubMed Central Статья Google Scholar
Национальная медицинская библиотека США. ClinicalTrials.gov https://clinicaltrials.gov/ct2/show/NCT03049488 (2018).
Национальная медицинская библиотека США. ClinicalTrials.gov https://clinicaltrials.gov/ct2/show/NCT03529773 (2018).
Falloon, J. et al. Постфузионная вакцина на основе F-белка с адъювантом не предотвращала респираторно-синцитиальный вирус у пожилых людей. J. Infect. Дис. 216 , 1362–1370 (2017).
CAS PubMed PubMed Central Статья Google Scholar
Национальная медицинская библиотека США. ClinicalTrials.gov https://clinicaltrials.gov/ct2/show/NCT02608502 (2017).
Национальная медицинская библиотека США. ClinicalTrials.gov https://clinicaltrials.gov/ct2/show/NCT02508194 (2017).
Национальная медицинская библиотека США. ClinicalTrials.gov https://clinicaltrials.gov/ct2/show/NCT02624947 (2018).
Каррон, Р. А., Бухгольц, У. Дж. И Коллинз, П.L. Живые аттенуированные вакцины против респираторно-синцитиального вируса. Curr. Вершина. Microbiol. Иммунол. 372 , 259–284 (2013).
CAS PubMed PubMed Central Google Scholar
Karron, R.A. et al. Делеция гена, которая активирует экспрессию вирусного гена, дает аттенуированную вакцину против RSV с улучшенными реакциями антител у детей. Sci. Transl Med. 7 , 312ра175 (2015).
PubMed PubMed Central Статья CAS Google Scholar
Liang, B. et al. Улучшенная стабильность перед слиянием, оптимизированное использование кодонов и расширенная упаковка вирионов повышают иммуногенность слитого белка респираторно-синцитиального вируса в кандидате с векторной вакциной. J. Virol. 91 , e00189-17 (2017).
CAS PubMed PubMed Central Статья Google Scholar
Stobart, C.C. et al. Несмотря на высокую аттенуацию, живая вакцина против RSV с модифицированной термостабильностью является иммуногенной для хлопковых крыс. Нат. Commun. 7 , 13916 (2016).
CAS PubMed PubMed Central Статья Google Scholar
Национальная медицинская библиотека США. ClinicalTrials.gov https://clinicaltrials.gov/ct2/show/NCT03303625 (2018).
Национальная медицинская библиотека США. ClinicalTrials.gov https://clinicaltrials.gov/ct2/show/NCT02927873 (2018).
Национальная медицинская библиотека США. ClinicalTrials.gov https://clinicaltrials.gov/ct2/show/NCT02873286 (2018).
Левин С. Полипептиды респираторно-синцитиального вируса. J. Virol. 21 , 427–431 (1977).
CAS PubMed PubMed Central Google Scholar
Уолш Э. Э. и Хруска Дж. Моноклональные антитела к белкам респираторно-синцитиального вируса: идентификация слитого белка. J. Virol. 47 , 171–177 (1983).
CAS PubMed PubMed Central Google Scholar
Гарсия, Дж., Гарсия-Баррено, Б., Виво, А. и Мелеро, Дж. А. Цитоплазматические включения инфицированных респираторно-синцитиальным вирусом клеток: образование телец включения в трансфицированных клетках, которые коэкспрессируют нуклеопротеин, фосфопротеин и белок 22К. Вирусология 195 , 243–247 (1993).
CAS PubMed Статья Google Scholar
Гарсия-Баррено, Б., Дельгадо, Т. и Мелеро, Дж. А. Идентификация участков белка, участвующих во взаимодействии фосфопротеина и нуклеопротеина респираторно-синцитиального вируса человека: значение для сборки нуклеокапсида и образования цитоплазматических включений. J. Virol. 70 , 801–808 (1996).
CAS PubMed PubMed Central Google Scholar
Rincheval, V. et al. Функциональная организация цитоплазматических телец включения в клетках, инфицированных респираторно-синцитиальным вирусом. Нат. Commun. 8 , 563 (2017).
PubMed PubMed Central Статья CAS Google Scholar
Noton, S. L. & Fearns, R. Инициирование и регуляция транскрипции и репликации парамиксовирусов. Вирусология 479–480 , 545–554 (2015).
PubMed Статья CAS Google Scholar
Gower, T. L. et al. Передача сигналов RhoA необходима для индуцированного респираторно-синцитиальным вирусом образования синцития и морфологии нитевидного вириона. J. Virol. 79 , 5326–5336 (2005).
CAS PubMed PubMed Central Статья Google Scholar
Ke, Z. et al. Морфология и сборка респираторно-синцитиального вируса, выявленная с помощью криоэлектронной томографии. Вирусы 10 , E446 (2018). Эта работа убедительно демонстрирует, что RSV является нитчатым вирусом после отпочкования из инфицированных клеток .
PubMed Статья Google Scholar
Mehedi, M. et al. Связанный с актином белок 2 (ARP2) и индуцированные вирусом филоподии способствуют распространению респираторно-синцитиального вируса человека. PLOS Pathog. 12 , e1006062 (2016).
PubMed PubMed Central Статья CAS Google Scholar
Vanover, D. et al. Динамика гликопротеина RSV и геномной РНК выявляет сборку филаментов до плазматической мембраны. Нат. Commun. 8 , 667 (2017).
PubMed PubMed Central Статья CAS Google Scholar
Форстер А., Мартенс Г. Н., Фаррелл П. Дж. И Байорек М. Димеризация матриксного белка необходима для отпочкования респираторно-синцитиального вируса. J. Virol. 89 , 4624–4635 (2015).
CAS PubMed PubMed Central Статья Google Scholar
Робертс, С. Р., Компанс, Р. В. и Вертц, Г. В. Респираторно-синцитиальный вирус созревает на апикальных поверхностях поляризованных эпителиальных клеток. J. Virol. 69 , 2667–2673 (1995).
CAS PubMed PubMed Central Google Scholar
Ярдецки Т.С. и Лэмб, Р. А. Активация слияния мембран парамиксовируса и проникновение вируса. Curr. Opin. Virol. 5 , 24–33 (2014).
CAS PubMed Статья Google Scholar
Yuan, P. et al. Структура эктодомена гемагглютинин-нейраминидазы (HN) вируса болезни Ньюкасла обнаруживает стебель пучка из четырех спиралей. Proc. Natl Acad. Sci. США 108 , 14920–14925 (2011).
CAS PubMed Статья Google Scholar
Welch, B.D. et al. Структура эктодомена гемагглютинин-нейраминидазы (HN) вируса парагриппа 5 (PIV5). PLOS Pathog. 9 , e1003534 (2013).
CAS PubMed PubMed Central Статья Google Scholar
Bose, S. et al. Активация слияния с помощью стебля гемагглютинин-нейраминидазы вируса парагриппа без головы 5 предполагает модульный механизм запуска. Proc. Natl Acad.Sci. США 109 , E2625 – E2634 (2012).
CAS PubMed Статья Google Scholar
Brindley, M. A. et al. Стабилизированный стебель прикрепляющего белка вируса безголовой кори эффективно запускает слияние мембран. J. Virol. 87 , 11693–11703 (2013).
CAS PubMed PubMed Central Статья Google Scholar
Liu, Q. et al. Раскрытие трехступенчатого пространственно-временного механизма запуска индуцированного рецептором слияния вируса Нипах и проникновения в клетки. PLOS Pathog. 9 , e1003770 (2013).
PubMed PubMed Central Статья CAS Google Scholar
Иорио Р. М., Мелансон В. Р. и Махон П. Дж. Взаимодействия гликопротеинов при слиянии парамиксовирусов. Future Virol. 4 , 335–351 (2009).
CAS PubMed PubMed Central Статья Google Scholar
Маклеллан, Дж. С. Нейтрализующие эпитопы на гликопротеине слияния респираторно-синцитиального вируса. Curr. Opin. Virol. 11 , 70–75 (2015).
CAS PubMed PubMed Central Статья Google Scholar
Динамика эпидемии респираторно-синцитиального вируса в текущем и будущем климате
Данные
Набор данных RSV на уровне округов США основан на данных о госпитализации, первоначально полученных из государственных баз данных стационарных пациентов (SID) Проекта затрат и использования здравоохранения (HCUP) поддерживается Агентством медицинских исследований и качества (AHRQ).Данные HCUP SID представляют в среднем 96% выписанных из стационаров общественных больниц в отчетных штатах, хотя не все штаты участвуют в сборе данных. Количество местных больниц, отчитывающихся с течением времени, колеблется в зависимости от штата. Стандартное отклонение в процентах отчетности в среднем составляет 2%. Были включены записи о госпитализации, которые включали 9-й пересмотр Международной классификации болезней, код клинической модификации (ICD-9-CM) для RSV (079.6, 466.11, 480.1) в пределах 15 диагнозов при выписке.Данные о госпитализации были доступны на еженедельном уровне. Данные о госпитализации доступны с 1989 года, однако изменение кодов отчетности в 1996 году привело к значительному увеличению числа случаев в настоящее время. Чтобы избежать возможной предвзятости из-за смены отчетности, мы берем все наблюдения на уровне округов, начиная с 1997 года. Самый длинный временной ряд охватывает 1997–2011 годы. Мы удаляем округа с очень редкими наблюдениями (максимальная частота <10 случаев), а также удаляем серию нулевых наблюдений с начала временного ряда.Мы удаляем все округа, которые имеют <5 лет последовательных наблюдений из-за возможной ошибочной подгонки модели для этого более короткого временного ряда, хотя эти округа сохраняются при построении пространственных средних значений.
Данные о госпитализации на уровне штата в Мексике поступают из Subsistema Automatizado de Egresos Hospitalarios (SAEH), собираются Sistema Nacional de Información en Salud (SINAIS) и контролируются Secretaría de Salud. Мы берем данные по всем случаям бронхиолита (коды МКБ-10 J21.0, J21.1, J21.8, J21.9), серьезная инфекция дыхательных путей, в первую очередь вызываемая RSV 38 (дополнительная таблица 8). Данные были суммированы за неделю, чтобы соответствовать данным США и отразить время генерации RSV. Данные по Мексике охватывают все годы с 2000 по 2014 год.
Данные о температуре и удельной влажности взяты из набора данных с привязкой к сетке 39 Регионального реанализа Северной Америки (NARR), подготовленного Национальными центрами прогнозирования окружающей среды (NCEP). Этот набор данных с высоким разрешением (32 км, ежедневные наблюдения) охватывает географические и временные рамки наших данных о состоянии здоровья.Данные об осадках поступают от Группы климатических опасностей по инфракрасным осадкам со станционными данными (CHIRPS) 40 . Пространственные средние значения строятся с использованием шейп-файлов для округов США из Бюро переписи населения США и для штатов Мексики.
Данные климатических прогнозов поступают из Фазы 5 Проекта взаимного сравнения связанных моделей (CMIP5). Прогнозы осадков берутся из всех моделей CMIP5, работающих по сценарию «Репрезентативный путь концентрации» 8.5. Удельная влажность рассчитывается на основе прогнозов температуры и относительной влажности на основе многомодельного среднего значения, доступного через KNMI Climate Explorer (https: // climexp.knmi.nl/start.cgi).
Данные о населении США были получены из общедоступных объединенных файлов данных Бюро переписи населения США, доступных через Национальное бюро экономических исследований. Данные о рождении в США были загружены из Центров по контролю за заболеваниями. Демографические данные по Мексике были получены от Instituto Nacional de Estadística y Geografía. Годовые оценки численности населения округов (США) и штата (Мексика) из этих источников были интерполированы на недельном уровне с использованием кубического сплайна, чтобы избежать скачков при смене года.
Данные на уровне округов в США более шумные, чем средние значения на уровне штата, используемые в исх. 27 , однако они дают некоторые преимущества. Например, временные ряды на уровне штата для Калифорнии демонстрируют динамичный переход от двухгодичных вспышек к ежегодным вспышкам в 1999 г. На уровне округов мы наблюдаем двухгодичные циклы, сохраняющиеся с 1999 г. и далее в Калифорнии, но при этом северные округа и южные округа не совпадают по фазе ( Дополнительный рис. 4). Это говорит о том, что использование данных на уровне округа может дать более точную картину динамики в зависимости от местоположения.
Определения
Мы определяем три типа динамических паттернов, наблюдаемых во временных рядах для конкретного местоположения в наборе данных. Динамика мелководья определяется как когда среднегодовая минимальная заболеваемость для конкретного местоположения превышает 5% от средней максимальной заболеваемости. Двухлетние местоположения определяются с использованием значимости двухлетнего сигнала с использованием периодограммы Ломба-Скаргла. Мы используем значение значимости 1% (все значения p ниже 5% показаны на дополнительном рис.3а, а также отношение двухгодичных и годовых амплитуд Фурье на дополнительном рис. 3b 27 ). При моделировании для рис. 3 мы определяем хаотические области как места, где постоянная Ляпунова положительна.
Для расчета средней начальной недели мы сначала вычисляем среднюю заболеваемость за неделю (т. Е. Каждую неделю, усредненную за все годы для данного местоположения), а затем нормализуем эти значения между 0 и 1. Мы определяем начало эпидемического периода как 26-е число. неделя года, примерно первая неделя июля.Этот период выбран, поскольку он охватывает все эпидемии в пределах наших данных (дополнительный рисунок 6). Мы определяем начало болезни, когда нормализованная частота превышает 0,2, предполагая, что это значение достаточно низкое, чтобы составлять начало, но достаточно высокое, чтобы превысить случайные колебания в данных. Использование нормализованной заболеваемости, в отличие от пороговых значений заболеваемости / популяции, позволяет создать единообразную меру для наборов данных как в США, так и в Мексике, несмотря на различия в выборках между двумя местоположениями.
Подход к моделированию
Наш подход к моделированию состоит из двух этапов 29 .Сначала мы используем модель TSIR временных рядов, дискретную временную адаптацию модели SIR 14,41 , чтобы оценить ненаблюдаемую восприимчивую популяцию для каждого местоположения с течением времени. Затем мы используем оценочные временные ряды восприимчивости для построения эмпирической скорости передачи. Скорость передачи используется в качестве зависимой переменной в панельной регрессии, где оценивается влияние климата.
Модель TSIR
Модель TSIR описывает количество инфицированных и восприимчивых людей в виде набора разностных уравнений.Число восприимчивых людей определяется выражением:
$$ {S} _ {t + 1} = {S} _ {t} + {B} _ {t} – {I} _ {t} + {u} _ {t} $$
(1)
где \ ({S} _ {t} \) и \ ({I} _ {t} \) – количество восприимчивых людей и количество инфицированных, соответственно, и период времени \ (t \ ), время генерации RSV составляет примерно 1 неделю. \ ({B} _ {t} \) – рождения, а \ ({u} _ {t} \) – аддитивный шум, с \ (E [{u} _ {t}] = 0 \). Восприимчивая популяция на каждом временном шаге может быть записана как \ ({S} _ {t} = \ bar {S} + {Z} _ {t} \), где \ (\ bar {S} \) – среднее число восприимчивых особей в популяции, а \ ({Z} _ {t} \) – неизвестное отклонение от среднего числа восприимчивых особей на каждом временном шаге.{t-1} I {r} _ {k} + {Z} _ {t} + {u} _ {t} $$
(2)
, где \ (\ rho \) – частота регистрации, учитывающая как занижение количества госпитализаций, связанных с РСВ, так и инфекций, которые не привели к госпитализации, а \ (I {r} _ {k} \) – зарегистрированная частота. . Используя это уравнение, \ ({Z} _ {t} \) оценивается как остатки линейной регрессии совокупных рождений по совокупным случаям, предполагая, что \ ({u} _ {t} \) мало. Обратный наклон линии регрессии дает оценку уровня отчетности \ (\ rho \).{\ alpha} {S} _ {t}} {{N} _ {t}} $$
(3)
, который лог-линеаризуется как:
$$ {\ mathrm {ln}} (E [{I} _ {t + 1}]) = {\ mathrm {ln}} ({\ beta} _ {t }) + \ alpha {\ mathrm {ln}} ({I} _ {t}) + {\ mathrm {ln}} (\ bar {S} + {Z} _ {t}) – {\ mathrm {ln }} ({N} _ {t}) $$
(4)
где \ ({\ beta} _ {t} \) – двухнедельные коэффициенты, отражающие сезонный тренд скорости передачи, а \ (\ alpha \) – константа, которая фиксирует неоднородности при смешивании и дискретизацию непрерывного временного процесса.Мы зафиксировали \ (\ alpha \) на 0,97, чтобы соответствовать предыдущим исследованиям 42 . По оценкам, еженедельные сезонные бета-версии, в отличие от еженедельных, позволяют избежать переобучения параметров из-за высокой корреляции в скоростях передачи в течение последующих недель. Уравнение (4) подбирается с использованием регрессии Пуассона со связью журнала. Окончательные результаты устойчивы к использованию отрицательного бинома на этом этапе (дополнительная таблица 7). Среднее количество восприимчивых людей, \ (\ bar {S} \), затем может быть оценено с использованием предельных вероятностей профиля из оценки уравнения.{\ alpha} {S} _ {t}} $$
(5)
Чтобы избежать инфляции \ ({\ rm {Em}} {\ beta} _ {t} \), мы добавляем один к нулю наблюдения в инфицированном временном ряду, который представляет непрерывную фоновую передачу низкого уровня, приводящую к отсутствию эпидемии. вымирание мы наблюдаем в данных. Результаты модели также устойчивы к удалению нулевых наблюдений из зараженного временного ряда (дополнительная таблица 3). Для установки TSIR мы используем комплект tsiR 43 .{2} \) соответствия TSIR <0,5 (101 округ). Эти места, как правило, находятся в округах с очень низкой численностью населения, где стохастическая изменчивость низкого уровня в случаях становится пропорциональной размеру сезонной изменчивости. Наши результаты устойчивы к использованию полного набора данных и отсечения по населению (дополнительные таблицы 5 и 6). Временные ряды в наборе данных Мексики более шумные, чем в Соединенных Штатах, даже для штатов с большим населением, что, как мы предполагаем, связано со стохастической природой факторов, влияющих на количество осадков, которые доминируют в этом регионе, а также с проблемами выборки, такими как более высокий порог госпитализации .В Мексике мы удаляем данные из двух штатов, где модель TSIR не подходит из-за очень разреженных данных (не более 10 случаев во временном ряду): Колима и Керетаро. Наш окончательный набор данных, к которому мы подбираем основную регрессионную модель, включает 214 местоположений и в общей сложности 119 802 местоположения за неделю. Результаты модели устойчивы к включению данных из всех округов США и Мексики (дополнительная таблица 5).
Панельная регрессия
Мы подбираем модель линейной регрессии, используя эмпирическую скорость передачи в качестве зависимой переменной:
$$ {\ mathrm {ln}} ({\ rm {Em}} {\ beta} _ {t, l }) = {b} _ {1} (1 / {H} _ {t, l}) + {b} _ {2} {P} _ {t, l} + {\ gamma} _ {l, m } + {\ delta} _ {l, y} + {\ epsilon} _ {t, l} $$
(6)
где \ ({\ rm {Em}} {\ beta} _ {t, l} \) – эмпирическая передача во время \ (t \) и местоположении \ (l \), \ ({H} _ { {t} _ {l}} \) – влажность, а \ ({P} _ {t, l} \) – осадки.Мы включаем манекены по месяцам \ ({\ gamma} _ {l, m} \), которые устраняют зависящие от местоположения сезонные колебания передачи, которые могут быть сбиты с толку другими сезонно меняющимися факторами, такими как школьные семестры. Мы также включаем манекены по годам \ ({\ delta} _ {l, y} \), которые удаляют зависящие от места тенденции передачи или эпизодические события передачи, которые могут быть ложно коррелированы с климатом. Стандартные ошибки группируются на уровне местоположения, хотя стандартные ошибки Уайта дают аналогичные результаты (дополнительная таблица 4).
Непараметрические биновые модели и общие аддитивные модели также приспособлены для проверки точности подобранной функциональной формы зависимости удельной влажности и осадков (дополнительные рисунки 8 и 9). Запаздывающие осадки и влажность за неделю до передачи проверяются, но не оказываются значительными (дополнительная таблица 9).
Моделирование
Мы запускаем несколько различных моделей моделирования, чтобы проверить влияние климата на динамику эпидемии RSV.Чтобы позволить климату полностью охарактеризовать сезонные изменения в передаче и средней передаче, мы повторно оцениваем уравнение. (6) удаление фиктивных переменных управления как:
$$ {\ mathrm {ln}} ({\ rm {Em}} {\ beta} _ {t, l}) = {b} _ {1} (1 / {H} _ {t, l}) + {b} _ {2} {P} _ {t, l} + {\ epsilon} _ {t, l} $$
(7)
Эта модель может быть подвержена смещению из-за других сезонно меняющихся или зависящих от местности тенденций и, как таковая, представляет собой верхнюю границу климатического воздействия. Результаты этой модели показаны на дополнительном рис.11 и значимы (\ (p \ ll 0,001 \)).
Мы запускаем моделирование в пространстве параметров средней передачи и сезонного изменения значений передачи с целью оценки (1) местоположения бифуркаций (левый график рис. 3а) и (2) разницы между текущей и будущей прогнозируемой динамикой на 2100 год. (Рис. 3а правый график). Чтобы плавно изменять сезонное изменение передачи в пространстве параметров, мы используем функцию косинуса для представления сезонности влажности. Моделирование проводится в течение 50 лет, чтобы устранить влияние переходных процессов, и анализируются только последние 10 лет.Чтобы другие факторы оставались неизменными, демографические данные в этих симуляциях основаны на округе Кингс, штат Нью-Йорк. На рис. 3a (справа) мы нанесем стрелку для каждого местоположения в нашем наборе данных, где основание стрелки представляет собой расчетные текущие значения параметров, а точка стрелки представляет собой прогнозируемые будущие значения параметров.
Для создания рис. 3b мы запускаем моделирование, на этот раз позволяя сезонным колебаниям климата полностью определять сезонную и среднюю скорость передачи, удаляя косинусную структуру.Мы берем выходные данные для всех 23 климатических моделей, включенных в среднее значение CMIP5. Для каждой модели мы рассчитываем отношение среднего количества осадков за неделю в конце столетия к началу столетия (с использованием средней аномалии за 5 лет в каждом случае). Затем мы применяем это соотношение к наблюдаемым осадкам в нашем наборе данных, также усредненным за 5-летний период, чтобы минимизировать систематическую ошибку при сравнении результатов моделирования с данными наблюдений. Мы применяем тот же метод к средней удельной влажности. Прогнозируемые осадки и влажность вводятся в уравнение.(7) для расчета скорости передачи, изменяющейся в зависимости от сезона. Форвардное моделирование проводится на 50 лет, чтобы удалить переходные процессы, при этом на рис. 3b показаны только последние 5 лет.
Краткое изложение отчета
Дополнительная информация о дизайне исследования доступна в Резюме отчета об исследовании природы, связанном с этой статьей.
Респираторно-синцитиальная вирусная инфекция у взрослых
- Ханна Х. Нам, старший научный сотрудник,
- Майкл Дж. Изон, профессор
- Отделение инфекционных заболеваний и трансплантации органов, Медицинская школа им. Файнберга Северо-Западного университета, Чикаго, Иллинойс 60611, США
- Для корреспонденции: MG Ison MGison {at} северо-западный.edu
РЕФЕРАТ
Респираторно-синцитиальный вирус человека (RSV) принадлежит к недавно определенному семейству Pneumoviridae , роду Orthopneumovirus. Это одноцепочечный РНК-вирус отрицательного смысла, который вызывает эпидемии респираторных инфекций, пик которых обычно наступает зимой в умеренном климате и в сезон дождей в тропическом климате. Как правило, один из двух генотипов (A и B) преобладает в течение одного сезона, ежегодно меняясь, хотя и существуют региональные различия.RSV является причиной заболеваний и смерти у детей, пожилых людей и пациентов с ослабленным иммунитетом, и его клиническое влияние на взрослых, госпитализированных, проясняется благодаря расширенному использованию мультиплексных молекулярных анализов. У взрослых RSV вызывает широкий спектр клинических симптомов, включая инфекции верхних дыхательных путей, тяжелые инфекции нижних дыхательных путей и обострения основного заболевания. Здесь мы обсуждаем последние данные о бремени заболеваний, связанных с RSV, у взрослых, особенно у людей с иммунодефицитом или другими сопутствующими заболеваниями.Мы рассматриваем как текущие, так и разрабатываемые варианты лечения и профилактики.
Сноски
Объяснение серии: Обзоры современного состояния проводятся на основе их актуальности для ученых и специалистов в США и за рубежом. По этой причине они написаны преимущественно американскими авторами
Авторы: Оба автора внесли свой вклад в идею статьи, обзор первичной литературы и написание рукописи.


 2.1 ставятся прочерки.
2.1 ставятся прочерки.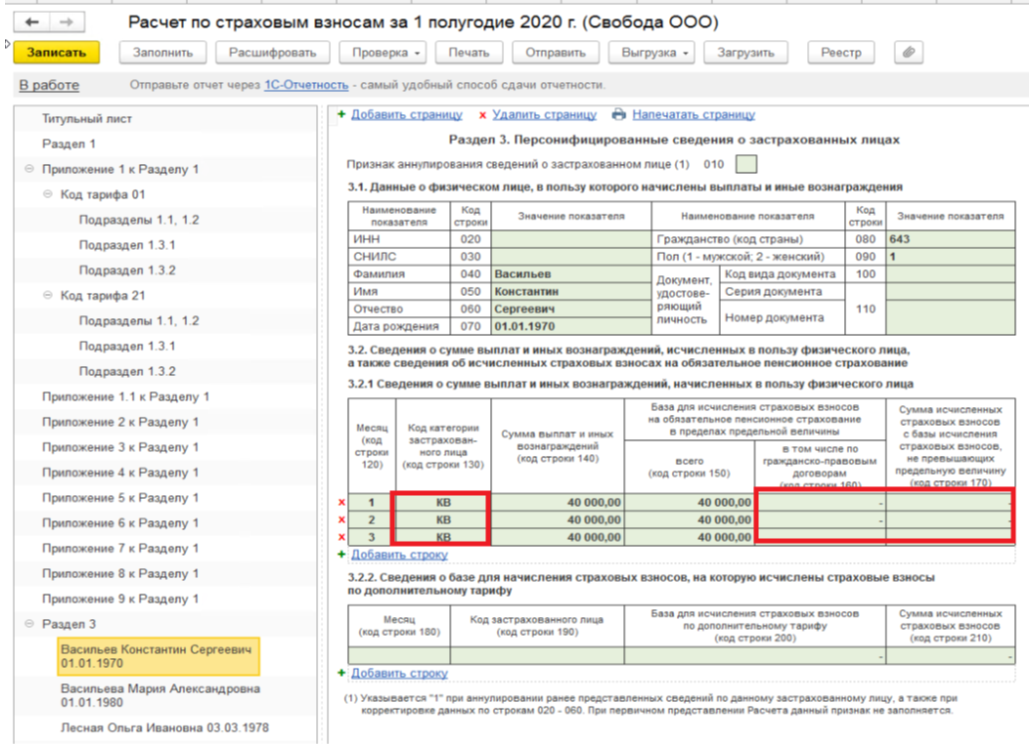
 2) и приложение 2 к разделу 1.
2) и приложение 2 к разделу 1.

 0 кб)
0 кб)